ГЕМАТОГЕННЫЙ ОСТЕОМИЕЛИТ У НОВОРОЖДЕННЫХ (опыт применения новой технологии) Текст научной статьи по специальности «Клиническая медицина»
УДК: 6616.-018.46-002-08-076.5 DOI: 10.24411/2075-4094-2019-16305
ГЕМАТОГЕННЫЙ ОСТЕОМИЕЛИТ У НОВОРОЖДЕННЫХ (опыт применения новой технологии)
А.А. ЦЫБИН , |А.Е. МАШКОВ| , А.В. ВАИС , П.Ю. ДЕГТЯРЕВ , МОХАММАД БАШИР ,
А.Н. ЯКУНОВ***
Тульский государственный университет, медицинский институт, ул. Болдина, д. 128, г. Тула, 300012, Россия Московский областной научно-исследовательский клинический институт им. М. Ф. Владимирского Минобрнауки РФ, Министерство здравоохранения Московской области, клиника хирургии детского возраста, ул. Щепкина, д. 61/2, стр. 10, г. Москва, 129110, Россия Тульская городская клиническая больница скорой медицинской помощи им.
Аннотация. Представлен опыт лечения острого гематогенного остеомиелита у 10 новорожденных детей. Мальчиков было 7 ч., девочек 3 ч. Всем детям проводилось комплексное клинико-лабораторное обследование. Трое из детей лечились консервативно. Большинство больных (7 детей) поступили на лечение в разной стадии деструкции костной ткани, что создавало особенности в выборе хирургической тактики. Комплексный анализ аспектов проблемы показал, что современная тенденция в лечении остеомиелита выражается в необоснованном консерватизме хирургической тактики. Выработана оптимальнная тактика хирургического лечения острого гематогенного остеомиелита новорожденных в гнойно-деструктивной стадии и применения методики длительного непрерывного аспирационного дренирования костного гнойного очага с соблюдением принципа: мягкие ткани, полость сустава и костный очаг дренировались раздельно в одновариантном режиме.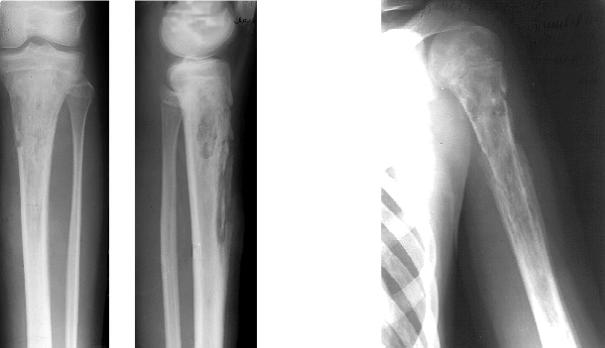
Ключевые слова: новорожденные, гематогенный остеомиелит, деструкция, дренирование, аспирация.
HEMATOGENOUS OSTEOMYELITIS IN NEWBORNS (new technology experience)
A.A. TSYBIN*, A.E. MASHKOV**, V.A. WEISS***, Y.P. DEGTYAREV***, MOHAMMAD BASHIR***,
Federal State Budgetary Educational Institution of Higher Education «Tula state University» of the Ministry of Education and Science of the Russian Federation, Medical Institute, Department of Surgical Diseases of Tula,
Boldin Str, 128, Tula, 300012, Russia State Budgetary Institution of Healthcare of the Moscow region «Moscow Regional M. F. Vladimirsky Research Clinical Institute» of the Ministry of Education and Science of the Russian Federation, Ministry of Health of the Moscow region, Moscow Pediatric Surgery Clinic, Schepkin Str., 61/2, p. 10, Moscow, 129110, Russia State Health Care Institution «Tula City Clinical P. Y. Anikin Hospital of Emergency» of the Ministry of Health, Tula region, Department of Pediatric Surgery, Pervomayskaya Str., 13, b. 1, Tula, 300035, Russia
F. Vladimirsky Research Clinical Institute» of the Ministry of Education and Science of the Russian Federation, Ministry of Health of the Moscow region, Moscow Pediatric Surgery Clinic, Schepkin Str., 61/2, p. 10, Moscow, 129110, Russia State Health Care Institution «Tula City Clinical P. Y. Anikin Hospital of Emergency» of the Ministry of Health, Tula region, Department of Pediatric Surgery, Pervomayskaya Str., 13, b. 1, Tula, 300035, Russia
Abstract. The experience of treatment of acute hematogenous osteomyelitis in 10 newborns, including 7 boys and 3 girls, is presented. All children underwent a comprehensive clinical and laboratory examination. Three children were treated conservatively. Most patients (7 children) received treatment at different stages of bone destruction, which created features in the choice of surgical tactics. A comprehensive analysis of the problems showed that the current trend in the treatment of CSOS is expressed in the unjustified conservatism of surgical tactics.
JOURNAL OF NEW MEDICAL TECHNOLOGIES, eEdition — 2019 — N 1
ciency. Regression of local signs of inflammation occurred at 5-6 days, in all cases there was no spread of destruction. In a short period, the centers of bone destruction were fully restored and the homeostasis of children was normalized, confirmed by dynamic X-ray and laboratory monitoring.
Key words: newborns, hematogenous osteomyelitis, destruction, drainage, aspiration.
Актуальность. Гематогенный остеомиелит (ГО) остается актуальной проблемой детского возраста [1]. Острый гематогенный остеомиелит новорожденных (ОГОН) в основном локализуется в ме-таэпифизарной зоне трубчатых костей, диагностика его в острой стадии имеет определенные трудности, как и в любом детском возрасте. Однако освещение в периодической литературе данной проблемы недостаточно. Клиническая картина заболевания может быть стертой, а симптоматика атипичной. По статистике, такая клиника болезни наблюдается у 22% новорожденных с первичными признаками остео-миелитического процесса. У мальчиков ОГОН встречается в 2 раза чаще, чем у девочек. Поражаются длинные трубчатые кости, бедренные и берцовые, кости верхних конечностей в 2 раза чаще, чем нижних конечностей [1-5]. Основными возбудителями ОГОН чаще являются: золотистый стафилококк, стрептококки группы B,E,Coli, кишечная палочка, палочка Пфейффера, сальмонелла, грамотрицатель-ные энтеробактерии.
Осложнения ОГОН проявляются в виде патологических переломов, деформаций, нарушения роста сегмента, контрактуры в суставах, нарушение функции опоры и ходьбы, ее своевременности с ростом ребенка. Летальность составляет 0,5-3,7%. Переход из острой в хроническую стадию при различной локализации наблюдается в 3,1-21,8% случаев. Хронизация при локализации в метаэпифизарной зоне отмечается у 23-58,3%. по данным различных авторов. По данным других исследователей переход ос-теомиелитического процесса перенесенного в новорожденном возрасте в хроническую стадию практически не наблюдается [4]. Однако это противоречит статистике осложнений и последствий, которые наблюдаются с возрастом у данной категории детей. Если считать, что с возрастом ребенка обострения в очаге локализации перенесенного остеомиелита становятся реже и к взрослому состоянию прекращаются, то последствия этого процесса бывают более негативны, чем рецидив заболевания.
Цель исследования — улучшение результатов лечения и прогноза комплексного лечения острого гематогенного остеомиелита (ОГО) у новорожденных.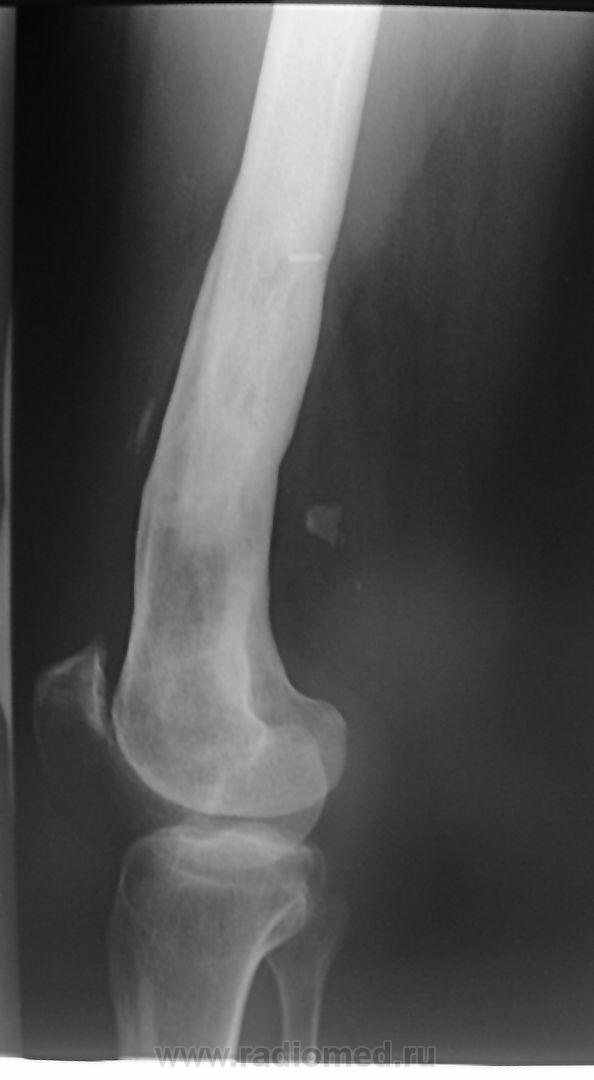 1. Анализ современной тактики лечения ОГОН. 2. Выработка оптимальной хирургической тактики лечения ОГОН 3. Изучение применения методики длительного непрерывного аспирационного дренирования костного гнойного очага (ДНАДКГО), как наиболее патогномоничного оперативного вмешательства в деструктивной стадии остеомиелитического процесса.
1. Анализ современной тактики лечения ОГОН. 2. Выработка оптимальной хирургической тактики лечения ОГОН 3. Изучение применения методики длительного непрерывного аспирационного дренирования костного гнойного очага (ДНАДКГО), как наиболее патогномоничного оперативного вмешательства в деструктивной стадии остеомиелитического процесса.
Материалы и методы исследования. Из 49-и детей разного возраста с ОГО, новорожденные составили 10 человек. Мальчиков было 7, девочек — 3 ч. Всем детям проводилось комплексное клинико-лабораторное обследование: биохимический и клинический анализ крови и мочи, обследование кала на дисбактериоз, консультация специалистов — педиатр, инфекционист, отоларинголог, окулист. Аппаратные методы исследования: УЗИ больного сегмента и смежного сустава, рентгенография легких, простая рентгенография в 2-х проекциях и компьютерная томография (КТ). Опыт лечения основывался на предыдущих данных исследования эффективности ДНАДКГО и применения его в лечении ГО у детей разного возраста от ^ года до 18 лет [5].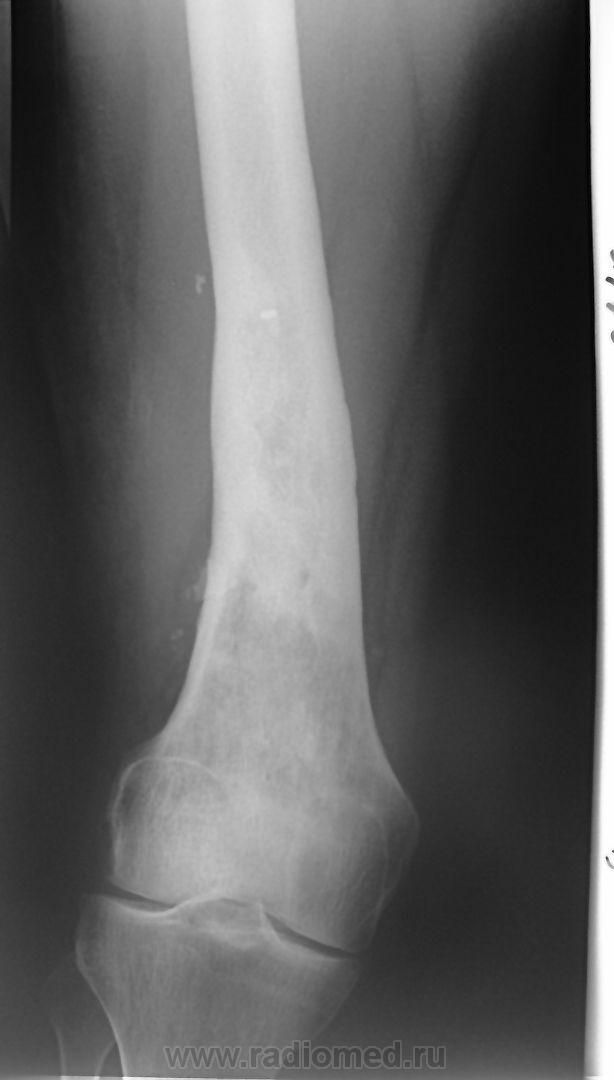
Операция проводилась под общей анестезией. Техника операции не отличалась от ранее применяемой нами методики у детей старшего возраста [5]. Из особенностей при ее проведении следует учитывать состояние тканей новорожденных и анатомию. При перфорации кости не требуется особых инструментов. Остеоперфорация наносилась сверлами малого диаметра с использованием обычной ручной дрели для трепанации. Для дренирования остеомиелитического очага применялись катетеры малого внутреннего диаметра 1,5-2,0 мм из пластика, с дополнительным нанесением перфорационных боковых отверстий. У 2-х детей для дренирования костного гнойного очага использовался стандартный мочеточ-никовый катетер. При наличии реактивного артрита дополнительно проводилось дренирование в аспирационном режиме полости сустава. Во время операции у всех детей проведено взятие экссудата из костномозгового канала и смежного сустава на бактериологическое исследование и чувствительность микрофлоры к антибиотикам, а также для прямой бактериоскопии и цитологического исследования методом мазка или отпечатка. Мягкие ткани так же дренировались послойно аспирационными дренажами. В по-
При перфорации кости не требуется особых инструментов. Остеоперфорация наносилась сверлами малого диаметра с использованием обычной ручной дрели для трепанации. Для дренирования остеомиелитического очага применялись катетеры малого внутреннего диаметра 1,5-2,0 мм из пластика, с дополнительным нанесением перфорационных боковых отверстий. У 2-х детей для дренирования костного гнойного очага использовался стандартный мочеточ-никовый катетер. При наличии реактивного артрита дополнительно проводилось дренирование в аспирационном режиме полости сустава. Во время операции у всех детей проведено взятие экссудата из костномозгового канала и смежного сустава на бактериологическое исследование и чувствительность микрофлоры к антибиотикам, а также для прямой бактериоскопии и цитологического исследования методом мазка или отпечатка. Мягкие ткани так же дренировались послойно аспирационными дренажами. В по-
слеоперационном периоде все дети в течение 1-2-х суток находились в отделении реанимации. У 4-х больных проводилось консервативное лечение.
У 4-х больных проводилось консервативное лечение.
Результаты и их обсуждение. У всех 10 новорожденных при появлении клинической картины (гипертермия свыше 38-39°С, нарушение функции сегмента, болевая контрактура в смежном суставе, отек, кожная гиперемия, изменения в общем состоянии) лечение было начато с консервативных мероприятий в отделении новорожденных. В последующем, при отсутствии стойкой положительной динамики дети переводились в отделение хирургии детского возраста. Все больные поступили в тяжелом состоянии и средней тяжести. Шестеро детей поступили в отделение детской хирургии позже 10 дней от начала заболевание в интрамедуллярной стадии процесса. Из них у 2-х отмечена экстрамедуллярная стадия, флегмона мягких тканей и признаки костной деструкцией. После установления диагноза все дети оперированы.
При предоперационном обследовании и в процессе лечения у 6 оперированных новорожденных детей по данным простой рентгенографии и КТ-исследования, имела место та или иная степень деструкции костной ткани.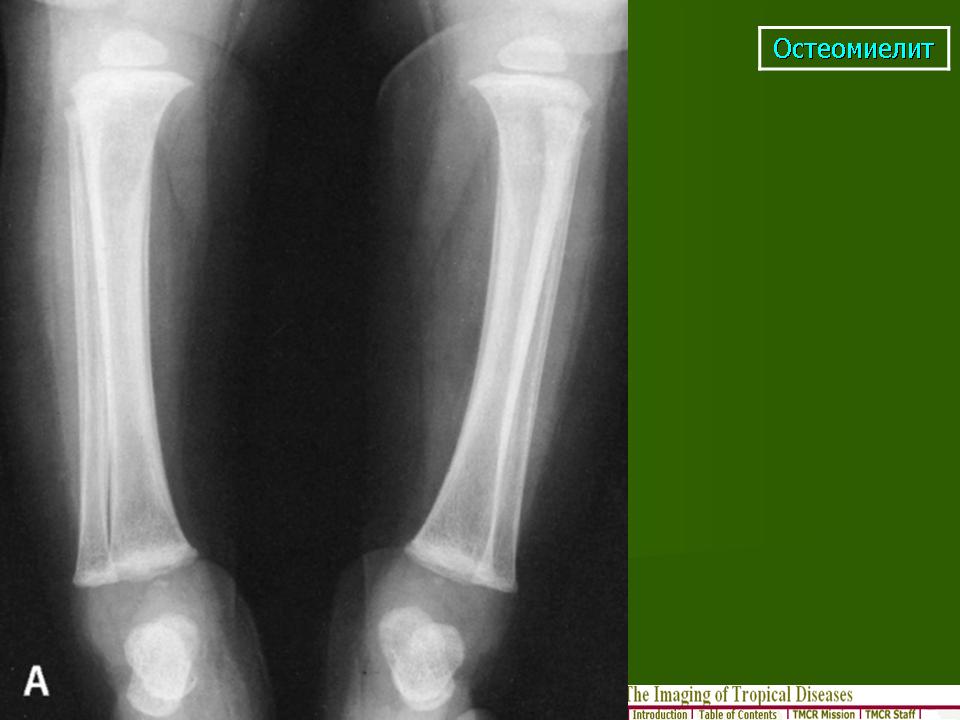 Из них, у 1 новорожденной девочки, заболевшей на 3-и сутки с момента рождения, поступившей на 12-й день от начала клинической картины диагностирована флегмона тыла правой кисти, причиной которой был редкий случай ОГО II-пястной фаланги. Больной проведено дренирование флегмоны ревизия тканей, при которой установлено, что источником флегмонозного гнойного воспаления является остеомиелитический гнойный свищ, исходящий из проксимального конца II пястной кости. Свищ расширен и через его наружное отверстие дренирован костномозговой канал (КМК) костного сегмента аспирационным дренажем (рис. 1, 2, 3, 4, 5).
Из них, у 1 новорожденной девочки, заболевшей на 3-и сутки с момента рождения, поступившей на 12-й день от начала клинической картины диагностирована флегмона тыла правой кисти, причиной которой был редкий случай ОГО II-пястной фаланги. Больной проведено дренирование флегмоны ревизия тканей, при которой установлено, что источником флегмонозного гнойного воспаления является остеомиелитический гнойный свищ, исходящий из проксимального конца II пястной кости. Свищ расширен и через его наружное отверстие дренирован костномозговой канал (КМК) костного сегмента аспирационным дренажем (рис. 1, 2, 3, 4, 5).
Рис. 1. Б-я Б. 15 дней. ОГОН второй пястной кости, флегмона кисти. Операция, ревизия мягких тканей,
дренирование флегмоны
Рис. 2. Б-я Б. 15 дней. ОГОН второй пястной кости, флегмона кисти. Стрелкой обозначен тыльный край основания пястной кости с мелким краевым дефектом, в зоне которого сформировался остеомиелитический внутренний свищ, явившийся причиной флегмоны кисти.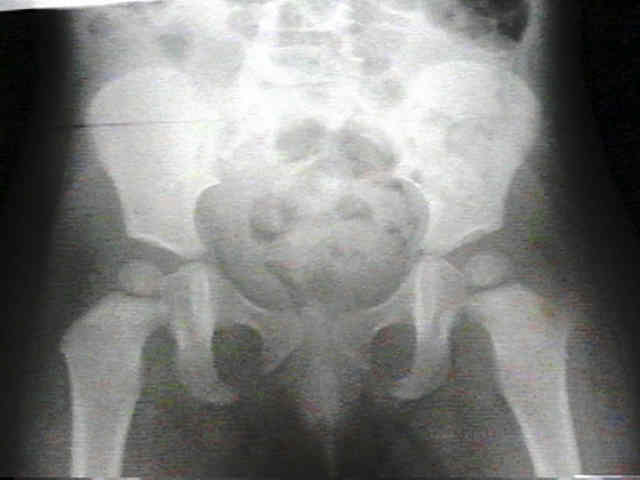 Виден уплотненный кортикальный слой кости (начало остеосклероза)
Виден уплотненный кортикальный слой кости (начало остеосклероза)
>
Щ
Рис. 3. Б-я Б. 15 дней. ОГОН второй пястной кости, флегмона кисти. Дренирование К М К пястной кости
аспирационным дренажем
Рис. 4. Б-я Б. 15 дней. ОГОН второй пястной кости, флегмона кисти. Завершение операции: дренирование КМК аспирационным дренажем II пястной кости и мягких тканей
Рис. 5. Б-я Б. 15 дней. ОГОН второй пястной кости, флегмона кисти. Завершение лечения дренированием. Нет деструкции кости, исчезло уплотнение кортикального слоя кости (начало склероза).
Функция кисти восстановлена
При этом простая рентгенография кисти отчетливо не выявила очагов деструкции в пястной костной фаланге.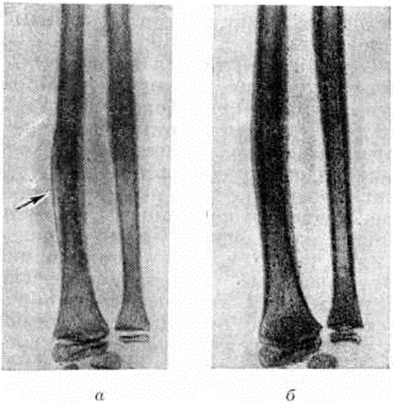 Очаг разряжения костной ткани и периостальная реакция были визуализированы только при КТ. Срок дренирования костного очага составил 3 недели. У ребенка на 6-й день купировались кли-
Очаг разряжения костной ткани и периостальная реакция были визуализированы только при КТ. Срок дренирования костного очага составил 3 недели. У ребенка на 6-й день купировались кли-
нические симптомы воспалительного процесса. Постепенно нормализовались лабораторные показатели крови.
У 2-го ребенка (рис. 6, 7), заболевшего на 2-е сутки с момента рождения и поступившего на 10-й день от начала заболевания диагностирован метаэпифизарный остеомиелит левой большеберцовой кости, гнойный артрит голеностопного сустава, параартикулярная флегмона мягких тканей.
Рис. 6. Б-й Н.,11 дней. ОГОН, метаэпифизарная локализация, острый гнойный артрит голеностопного сустава, параартикулярная флегмона. Дренирование К М К большеберцовой кости и полости г/ст.
сустава
Рис. 7. Б-й Н.,11 дней. ОГОН, метаэпифизарная локализация, острый гнойный артрит голеностопного сустава, параартикулярная флегмона. Рентгенограмма после дренирования К М К большеберцовой
7. Б-й Н.,11 дней. ОГОН, метаэпифизарная локализация, острый гнойный артрит голеностопного сустава, параартикулярная флегмона. Рентгенограмма после дренирования К М К большеберцовой
кости и полости г/ст. сустава
На простой рентгенографии определялся очаг деструкции в дистальном конце большеберцовой кости (разрежение, выраженная периостальная реакция). Произведена операция в день поступления в отделение детской хирургии, аспирационное дренирование КМК, полости голеностопного сустава и ин-цизионно-дренажная операция на параартикулярных тканях. Мягкие ткани и синовиальная полость требовали меньшей длительности наружного дренирования, по сравнению с костью. Данный принцип обоснован разными сроками наружной санации, и заживления тканей. Срок дренирования мягких тканей до эпителизации раны составил 9 дней. На 7-й день купировались клинические признаки воспалительной реакции, постепенно нормализовались лабораторные показатели. Срок дренирования костного очага продолжался в течение 4,5 месяцев до полного восстановления очага деструкции и исчезновения перио-стальной реакции.
Срок дренирования костного очага продолжался в течение 4,5 месяцев до полного восстановления очага деструкции и исчезновения перио-стальной реакции.
Два ребенка были с ОГО метадифизарной зоны бедренной кости, поступили на 11 и 10-е сутки от начала заболевания. По данным УЗИ отмечался незначительный отек тканей и синовит тазобедренного
JOURNAL OF NEW MEDICAL TECHNOLOGIES, eEdition — 2019 — N 1
сустава, при КТ-исследования, в вертельной зоне бедра отмечалось разрежение костных структур и пе-риостальная реакция с медиальной стороны указанной области. Оба новорожденных оперированы, произведено дренирование вертельной зоны по методике ДНАДКГО, лечебно-диагностическая пункционная санация тазобедренного сустава. Симптомы остеомиелитического процесса купировались на 9-е сутки, деструкции кости на фоне дренирования не наступило, нормализовалось общее состояние и лабораторные показатели крови.
У 1 новорожденной девочки (рис. 8, 9) развился ОГО метаэпифизарный, дистального конца левой бедренной кости с 3-х суток после рождения. В течение 25 дней проводилось консервативное лечение в отделении патологии новорожденных с частичным эффектом. Однако сохранялись признаки воспалительной реакции, отек бедра и контрактура в коленном суставе. На контрольных рентгенограммах, и КТ-исследовании отмечена деструкция дистального конца бедренной кости, с выраженной периостальной реакцией и умеренной угловой деформацией бедренной кости открыты углом кзади.
Рис. 8. Б-я Д.,29 дней. ОГОН, метаэпифизарная локализация, острый реактивный артрит коленного сустава,. Рентгенограмма до дренирования К М К бедренной кости и полости тазобедренного сустава
Рис. 9. Б-я Д., 29 дней. ОГОН, метаэпифизарная локализация, острый реактивный артрит коленного сустава. Рентгенограмма после дренирования К М К бедренной кости процесс дренирования. Видна перестройка кости, регенерация и исчезновение периостальной избыточной реакции надкостницы
Рентгенограмма после дренирования К М К бедренной кости процесс дренирования. Видна перестройка кости, регенерация и исчезновение периостальной избыточной реакции надкостницы
Ребенок продолжал температурить до субфебрильных цифр, отмечался фебрилитет при паузе в антибиотикотерапии и смене антибиотика. Больная была оперирована по методике на 29 день от начала заболевания. Во время операции при остеоперфорации в КМК экссудат серозно-геморрагического характера с большим количеством воспалительных элементов (нейтрофилы) и микрофлоры при интраопера-ционной микроскопии. Послеоперационый период протекал гладко. Температура нормализовалась без применения антибиотиков на 5-й день. Срок дренирования составил 5 месяцев. Полностью восстановилась костная структура в очаге поражения и функция сегмента.
Еще 1 ребенок наблюдался с метаэпифизарным ОГО проксимального конца правой плечевой кости. Заболел с 1-х суток после рождения, поступил в отделение детской хирургии на 15-й день от начала заболевания при отсутствии эффекта от консервативной терапии. При поступлении — состояние тяжелое отмечалась выраженная контрактура в плечевом суставе, отек, венозная гиперемия, нарушение функции конечности, парез верхней конечности. При рентгенографии выявлена деструкция проксимального конца
При поступлении — состояние тяжелое отмечалась выраженная контрактура в плечевом суставе, отек, венозная гиперемия, нарушение функции конечности, парез верхней конечности. При рентгенографии выявлена деструкция проксимального конца
JOURNAL OF NEW MEDICAL TECHNOLOGIES, eEdition — 2019 — N 1
плечевой кости с образованием полости и разрежением костных структур вокруг очага деструкции. Операция: остеоперфорация, в костной полости обнаружен густой гной до 1,0 мл, полость санирована, дренирована аспирационным дренажем. Послеоперационный период без осложнений. Срок дренирования костного гнойного очага составил 4,5 мес. В ближайших сроках наблюдения до 3-х месяцев у всех оперированных детей восстановилась функция больного сегмента и костная структура. Только у ребенка с остеомиелитом плечевой кости в конце лечения отмечена умеренная гипотрофия мышц плечевого пояса, за счет гиподинамии в конечности, которая купировалась к году.
При поступлении у всех больных отмечалась выраженная гнойно-воспалительная реакция со стороны крови с тенденцией к нарастанию: СОЭ (18-25 мм/ч), лейкоцитоз (19*103 — 64*103), соотношение количества нейтрофилов, палочкоядерных нейтрофилов и лимфоцитов указывало на задержку первого перекреста лейкоцитарной формулы. Изменения количества тромбоцитов сопровождались меньшими колебаниями. Отмечалась анемия (Hb от 119,0 г/л до 77,0 г/л), со снижением количества эритроцитов, Ht, повышенные показатели С-РБ к периоду развернутой картины воспаления и деструкции кости, щелочной фосфатазы, которые в короткие сроки после операции нормализовались.
Длительное дренирование, направленное на полную санацию костного гнойного очага и оптимизацию остеогенеза способствовало нормализации восстановительных процессов в кости. При бактериологическом посеве экссудата из остеомиелитического очага у оперированных больных высевался St. aureus — в 4 случаях, Str. Hemolyticus — в 1 случае посев роста не дал. Сроки стационарного лечения оперированных новорожденных составили от 12 до 30 дней. Родители малышей обучались уходу за дренажной системой. Далее дети лечились амбулаторно с контрольными осмотрами 1-2 раза в 2 недели, и наблюдаются до настоящего времени.
aureus — в 4 случаях, Str. Hemolyticus — в 1 случае посев роста не дал. Сроки стационарного лечения оперированных новорожденных составили от 12 до 30 дней. Родители малышей обучались уходу за дренажной системой. Далее дети лечились амбулаторно с контрольными осмотрами 1-2 раза в 2 недели, и наблюдаются до настоящего времени.
Из 4 детей с ОГО, лечившихся консервативно, у 3 больных процесс локализовался в области проксимального конца бедренной кости и у 1 в дистальном конце бедренной кости. У всех имело место вовлечение в воспаление тазобедренного сустава. У 4 новорожденных, которым проводилось консервативное лечение, в 3 случаях, по данным рентгенологического исследования, выраженной деструкции костной ткани не отмечалось. В начальной стадии воспаления отмечался очаговый воспалительный ос-теопороз в области вертельной зоны, отек мягких тканей и структур кости по данным УЗИ, выраженная клиническая картина заболевания, как и в группе оперированных детей. Тяжелое общее состояние сопровождалось воспалительной реакцией со стороны показателей крови. У 1 новорожденного, из двойни, наступила деструкция дистального конца бедренной кости с патологическим переломом на границе н/з и с/з бедра. В последующем это привело к угловой деформации бедра с углом кзади, укорочению сегмента на 2,5см, повреждению и задержке развития наружного мыщелка бедра, нарушению ходьбы, контрактуре в коленном суставе. У данной группы детей медленней наступало улучшение состояния в остром периоде болезни, показателей крови и активных и пассивных движений в смежном суставе. Контрактура отмечалась после года наблюдения. У всех 3 детей без деструкции кости сохранялся локальный умеренный остеопороз, контрактура в суставе и функциональное укорочение сегмента на 1 см, асимметрия кожных складок бедра.
Тяжелое общее состояние сопровождалось воспалительной реакцией со стороны показателей крови. У 1 новорожденного, из двойни, наступила деструкция дистального конца бедренной кости с патологическим переломом на границе н/з и с/з бедра. В последующем это привело к угловой деформации бедра с углом кзади, укорочению сегмента на 2,5см, повреждению и задержке развития наружного мыщелка бедра, нарушению ходьбы, контрактуре в коленном суставе. У данной группы детей медленней наступало улучшение состояния в остром периоде болезни, показателей крови и активных и пассивных движений в смежном суставе. Контрактура отмечалась после года наблюдения. У всех 3 детей без деструкции кости сохранялся локальный умеренный остеопороз, контрактура в суставе и функциональное укорочение сегмента на 1 см, асимметрия кожных складок бедра.
В литературных источниках часто нет четкого разделения на осложнения и последствия перенесенного остеомиелита у новорожденных. Под последствиями, как правило, описываются различные деформации, укорочения вследствие нарушения роста сегмента, контрактуры в суставах, нарушение функции опоры и ходьбы, что является чаще следствием глубокой деструкции костной ткани в активных функциональных зонах костных сегментов, недостаточной эффективности длительного противовоспалительного лечения и рецидивирующего течения, обострения хронической стадии ОГОН.
Под последствиями, как правило, описываются различные деформации, укорочения вследствие нарушения роста сегмента, контрактуры в суставах, нарушение функции опоры и ходьбы, что является чаще следствием глубокой деструкции костной ткани в активных функциональных зонах костных сегментов, недостаточной эффективности длительного противовоспалительного лечения и рецидивирующего течения, обострения хронической стадии ОГОН.
Современная тенденция в лечении ОГОН выражается в достаточно консервативной тактике. Распространенным мнением считается, что показанием к операции является наличие формирования флегмоны мягких тканей. Трудности диагностики в начальном периоде болезни диктуют необходимость начинать лечение с консервативных мероприятий: антибактериальная терапия (АБТ), инфузионная, противовоспалительная терапия и динамическое наблюдение. Причиной, по мнению разных исследователей, такому подходу служит опасность нанесения травмы кости операцией остеоперфорации, в зоне которой происходит, чаще наибольшая деструкция кости. А так же надежда на АБТ и интенсивную инфузион-ную терапию, высокую пластичность и репаративную регенерацию костной ткани у новорожденных. Однако, имеются данные, о необоснованном консервативном подходе в лечении такой сложной и тяжелой гнойно-септической патологии у новорожденных детей. Активный подход в лечении дает лучшие результаты. Поэтому данные вопросы требует дополнительного исследования и выработки хирургической тактики.
А так же надежда на АБТ и интенсивную инфузион-ную терапию, высокую пластичность и репаративную регенерацию костной ткани у новорожденных. Однако, имеются данные, о необоснованном консервативном подходе в лечении такой сложной и тяжелой гнойно-септической патологии у новорожденных детей. Активный подход в лечении дает лучшие результаты. Поэтому данные вопросы требует дополнительного исследования и выработки хирургической тактики.
Заключение. Комплексный анализ аспектов проблемы показал, что современная тенденция в лечении ОГО выражается в необоснованном консерватизме хирургической тактики, связанной с отказом от ранней остеоперфорации. Показанием к операции служит наличие признаков формирующейся флегмоны мягких тканей, с чем нельзя согласиться, несмотря на трудности диагностики. Применение методики аспирационного дренирования, ближайшие результаты, и прогноз показал, ее высокую эффективность.
JOURNAL OF NEW MEDICAL TECHNOLOGIES, eEdition — 2019 — N 1
Регрессия местных признаков воспаления наступала на 5-6 сутки, во всех случаях отсутствовало распространение деструкции, в ближайшем периоде полностью восстановились очаги разрушения кости и нормализовался гомеостаз детей, подтвержденные при комплексном контроле. Новый подход позволяет воздействовать на все основные звенья патогенеза заболевания. ДНАДКГО в лечении остеомиелита у детей патогномоничный, высокоэффективный способ и может служить базовой методикой для решения проблемы. Случаи относительно успешного консервативного лечения ОГОН требуют дальнейшего детального изучения и анализа ближайших и отдаленных результатов в сравнении с оперативным способом ДНАДКГО, как достаточно перспективной методикой лечения, доказавшей свою эффективность у старших детей.
Новый подход позволяет воздействовать на все основные звенья патогенеза заболевания. ДНАДКГО в лечении остеомиелита у детей патогномоничный, высокоэффективный способ и может служить базовой методикой для решения проблемы. Случаи относительно успешного консервативного лечения ОГОН требуют дальнейшего детального изучения и анализа ближайших и отдаленных результатов в сравнении с оперативным способом ДНАДКГО, как достаточно перспективной методикой лечения, доказавшей свою эффективность у старших детей.
Литература
1. Азизов А.А. Роль клебсиелезно-протейной инфекции в этиологии остеомиелита у новорожденных. Современные технологии в педиатрии и детской хирургии: мат. II Росс.конгр. Москва, 2003. С. 371.
2. Азизов А. А. Острый гематогенный эпифизарный остеомиелит у новорожденных. Неотложное состояние у детей: мат. II Росс.конгр. Москва, 2003. С. 215-216.
С. 215-216.
3. Азизов А.А. Отдаленные результаты комплексного лечения острого гематогенного метаэпифи-зарного остеомиелита у новорожденных. IV съезд педиатров Таджикистана: мат. съезда. Душанбе, 2008. С. 297-298.
4. Цыбин А.А. Новый подход в лечении остеомиелита. Доклады академии наук // Биофизика. 2008. Т. 419, № 3. С. 425-429.
5. Цыбин А. А., Коноваленко С.И., Бояринцев В. С. Патогенез остеомиелита // Вестник новых медицинских технологий. 2003. Т.10, № 1-2. С. 60-63.
References
1. Azizov AA. Rol’ klebsielezno-protejnoj infekcii v ehtiologii osteomielita u novorozhdennyh [the Role Klebsiella-proteaceae infection in the etiology of osteomyelitis in newborns]. Sovremennye tekhnologii v pedia-trii i detskoj hirurgii: mat. II Ross. kongr. Moscow; 2003. Russian.
kongr. Moscow; 2003. Russian.
2. Azizov AA. Ostryj gematogennyj ehpifizarnyj osteomielit u novorozhdennyh [Acute hematogenous epiphyseal osteomyelitis in newborns]. Neotlozhnoe sostoyanie u detej: mat. II Ross.kongr. Moscow; 2003. Russian.
3. Azizov AA. Otdalennye rezul’taty kompleksnogo lecheniya ostrogo gematogennogo metaehpifizarno-go osteomielita u novorozhdennyh [Long-Term results of complex treatment of acute hematogenous metaepi-physeal osteomyelitis in newborns]. IV s»ezd pediatrov Tadzhikistana: mat. s»ezda. Dushanbe; 2008. Russian.
4. Cybin AA. Novyj podhod v lechenii osteomielita [a New approach in the treatment of osteomyelitis. Reports of the Academy of Sciences]. Doklady akademii nauk. Biofizika. 2008;419(3):425-9. Russian.
5. Cybin AA, Konovalenko SI, Boyarincev VS. Patogenez osteomielita [pathogenesis of osteomyelitis]. Vestnik novyh medicinskih tekhnologij. 2003;10(1-2):60-3. Russian.
Patogenez osteomielita [pathogenesis of osteomyelitis]. Vestnik novyh medicinskih tekhnologij. 2003;10(1-2):60-3. Russian.
Библиографическая ссылка:
Цыбин А.А., |Машков А.Е. |, Вайс А.В., Дегтярёв П.Ю., Мохаммад Башир, Якунов А.Н. Гематогенный остеомиелит у новорожденных (опыт применения новой технологии) // Вестник новых медицинских технологий. Электронное издание. 2019. №1. Публикация 1-6. URL: http://www.medtsu.tula.ru/VNMT/Bulletin/E2019-1/1-6.pdf (дата обращения: 18.01.2019). DOI: 10.24411/2075-4094-2019-16305. *
* номера страниц смотреть после выхода полной версии журнала: URL: http://medtsu.tula.ru/VNMT/Bulletin/E2019-1/e2019-1.pdf
Остеомиелит: Симптомы, причины и лечение
Остеомиелит — это гнойная инфекция, поражающая костную ткань (остит), окружающую кость надкостницу (периостит) и костный мозг (миелит).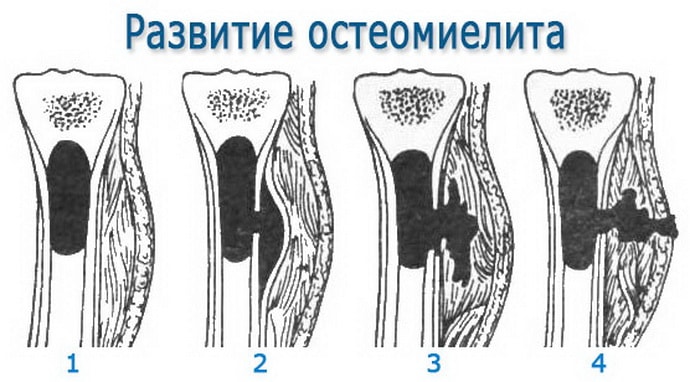 Впервые возникший остеомиелит называют острым. В случае длительного течения заболевания с периодами обострения и ремиссии говорят о развитии хронического остеомиелита.
Впервые возникший остеомиелит называют острым. В случае длительного течения заболевания с периодами обострения и ремиссии говорят о развитии хронического остеомиелита.
Причины
Остеомиелит развивается в результате попадания бактерий в костную ткань, надкостницу или костный мозг.
Инфицирование кости может произойти эндогенным (внутренним) путем, когда бактерии попадают в костную ткань с током крови по кровеносным сосудам. Такой остеомиелит принято называть гематогенным (в переводе с греческого языка — порожденный из крови). Острый гематогенный остеомиелит чаще встречается в грудном, детском и юношеском возрасте, взрослые болеют им редко.
Гнойное воспаление костей может возникнуть при проникновении микроорганизмов из окружающей среды – это экзогенный остеомиелит. Примером экзогенного остеомиелита является инфекция кости, развившаяся в результате открытого перелома, огнестрельного ранения или после травматологической операции (называют также посттравматический остеомиелит).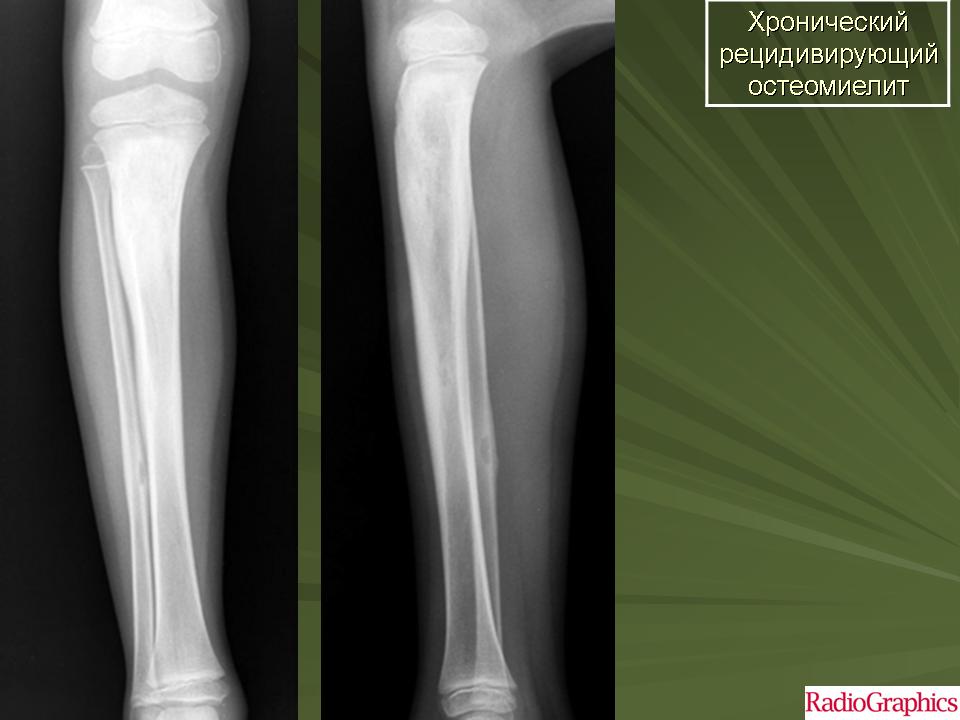 Другой разновидностью экзогенного остеомиелита является контактный остеомиелит, возникающий при переходе гнойного воспаления на кость с окружающих ее мягких тканей.
Другой разновидностью экзогенного остеомиелита является контактный остеомиелит, возникающий при переходе гнойного воспаления на кость с окружающих ее мягких тканей.
Способствуют развитию остеомиелита следующие состояния: злоупотребление алкоголем, курение, употребление внутривенных наркотических средств, атеросклероз сосудов, варикозная болезнь и хроническая венозная недостаточность, сахарный диабет, частые инфекции (3-4 раза в год), нарушение функции почек и печени, злокачественные заболевания (опухоли), перенесенная спленэктомия (удаление селезенки), пожилой и старческий возраст, низкая масса тела, плохое питание.
Симптомы
Клиническая картина обычно характеризуется сверхострым началом болезни с септическими, токсическими симптомами. Температура высокая, у детей старшего возраста остеомиелит начинается ознобом; пульс учащенный, ребенок очень вялый и производит впечатление тяжело больного. В первые дни местные симптомы остеомиелита иногда не выражены, тяжелое общее состояние полностью определяет клиническую картину.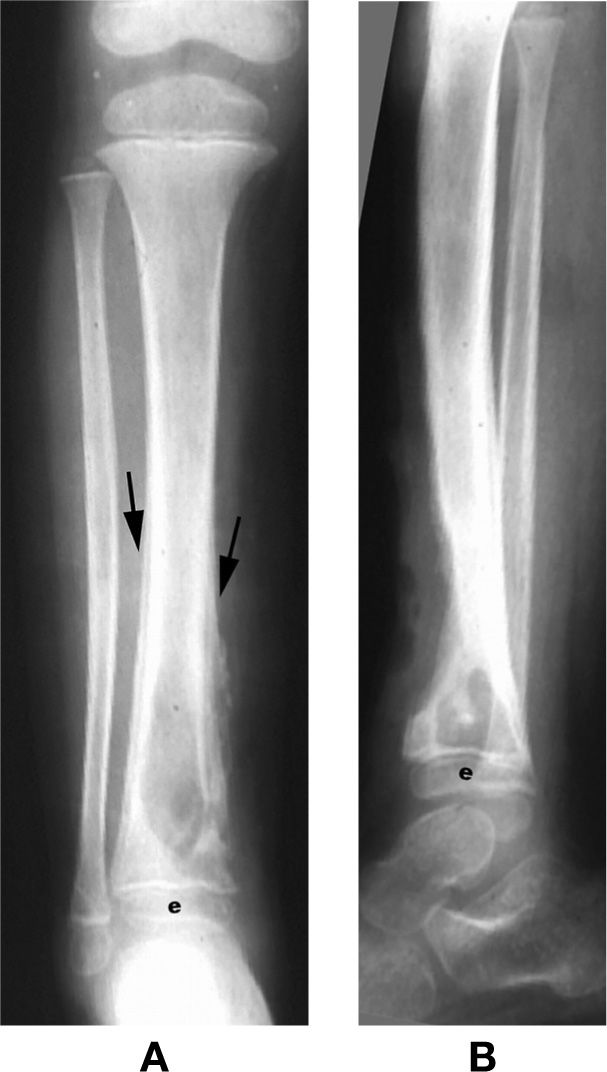 Больной обычно жалуется на боли в кости; боль усиливается, пораженная кость становится чувствительной к давлению. Местное покраснение и отек не являются ранними симптомами остеомиелита, но через 2-3 дня от начала при возникновении субпериостального абсцесса эти признаки бросаются в глаза.
Больной обычно жалуется на боли в кости; боль усиливается, пораженная кость становится чувствительной к давлению. Местное покраснение и отек не являются ранними симптомами остеомиелита, но через 2-3 дня от начала при возникновении субпериостального абсцесса эти признаки бросаются в глаза.
При прорыве абсцесса, расположенного под надкостницей, боли уменьшаются и выявляются покраснение, отек, флюктуация.
Диагностика
При осмотре проводят аккуратную пальпацию (ощупывание пальцами) болезненного участка, при этом отмечается состояние кожи (горячая, имеется покраснение и припухлость, образуются волнообразные движения тканей) и общий внешний вид поврежденной зоны (натянутые кожные покровы, «глянцевый» блеск, отечность). С помощью осторожной перкуссии (постукивания) определяют очаг инфекции по усилению боли в конкретном месте припухлости.
Помимо оценки клинических проявлений и ручного осмотра применяются лабораторные методы исследования. Общий анализ крови с лейкоцитарной формулой в развернутом виде показывает сдвиг влево.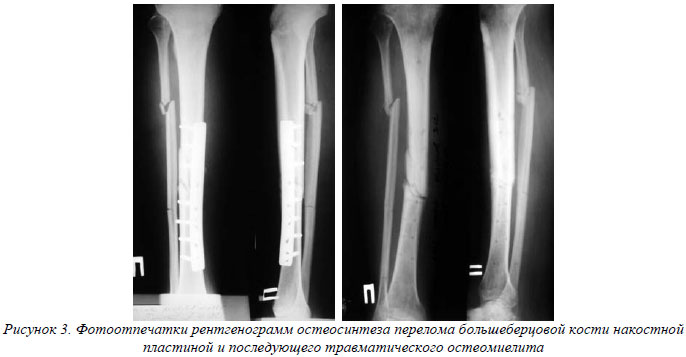 Это означает, что воспаление в организме вызвано бактериальной природой.
Это означает, что воспаление в организме вызвано бактериальной природой.
Общий анализ мочи показывает наличие воспаления и почечной недостаточности (при генерализованных формах болезни) путем появления белка, увеличения некоторых показателей.
Биохимический анализ крови показывает воспалительный процесс и отмечает почечную и печеночную недостаточность. При этом изменяются параметры билирубина, белка, снижается показатель глюкозы, а количество некоторых элементов увеличивается.
Наряду с лабораторными способами используются инструментальные методы обследования:
- Ультразвуковое исследование применяют для оценки размеров и формы мышечного поражения.
- Инфракрасное сканирование может показать наличие острых скрытых форм остеомиелита, определив участки с повышенной температурой.
- Рентгенография – самый распространенный вариант диагностирования остеомиелита. С помощью снимков можно определить локализацию некротических процессов, объем и степень выраженности инфекционного очага.
 С помощью рентгена можно выявить болезнь на ранних стадиях. По мере роста воспаления изменяется характер изображения на снимках, поэтому время протекания болезни можно обозначить с высокой точностью.
С помощью рентгена можно выявить болезнь на ранних стадиях. По мере роста воспаления изменяется характер изображения на снимках, поэтому время протекания болезни можно обозначить с высокой точностью. - Компьютерная томография – наиболее информативный способ диагностики остеомиелита в любых его проявлениях. С помощью объемных изображений можно получить не только данные о локализации и интенсивности инфекции, но и создать реконструкцию окружающих мышечных тканей и спрогнозировать течение болезни.
Для точного диагноза, который имеет определяющее значение в лечении остеомиелита, необходимо сочетание лабораторных и инструментальных способов исследования.
Лечение
Лечение острого остеомиелита проводится только в стационаре в отделении травматологии. Выполняют иммобилизацию конечности. Проводят массивную антибиотикотерапию с учетом чувствительности микроорганизмов. Для уменьшения интоксикации, восполнения объема крови и улучшения местного кровообращения переливают плазму, гемодез, 10% раствор альбумина. При сепсисе применяют методы экстракорпоральной гемокоррекции.
При сепсисе применяют методы экстракорпоральной гемокоррекции.
Обязательным условием успешного лечения острого остеомиелита является дренирование гнойного очага. На ранних стадиях в кости делают трепанационные отверстия с последующим промыванием растворами антибиотиков и протеолитических ферментов.
При гнойных артритах выполняют повторные пункции сустава для удаления гноя и введения антибиотиков, в некоторых случаях показана артротомия. При распространении процесса на мягкие ткани образовавшиеся гнойники вскрывают с последующим открытым промыванием.
В лечении хронического остеомиелита операция показана при наличии остеомиелитических полостей и язв, гнойных свищей, секвестров, ложных суставах, частых рецидивах с интоксикацией, выраженной болью и нарушением функции конечности, малигнизации, нарушении деятельности других органов и систем вследствие хронической гнойной инфекции.
Выполняют некрэктомию – удаление секвестров, грануляций, остеомиелитических полостей вместе с внутренними стенками и иссечение свищей с последующим промывным дренированием. После санации полостей проводят костную пластику.
После санации полостей проводят костную пластику.
Диагностика и комплексное лечение метаэпифизарного остеомиелита у детей
1. Абаев Ю.К., Аринчин В.Н., Телятицкий Н.И. Острофазные белки при остеомиелите и артритах у доношенных и недоношенных новорожденных // Детская хирургия. — 2007. — №6. — С. 32-35.
2. Абаев Ю.К. Пренатальный остеомиелит // Детская хирургия. 2005. -№3. — С. 53-54.
3. Абаев Ю.К., Кепеть В.А., Телятицкий Н.И. Остеомиелит у недоношенных детей // Детская хирургия. 2008. — №2. — С. 39-42.
4. Абушкин И.А., Привалов В.А., Крочек И.В. Ранняя неинвазивная диагностика острого гематогенного остеомиелита у детей // Детская хирургия. 2001. — №1. — С. 31-34.
5. Акжигитов Г.Н., Юдин Я.Б. Гематогенный остеомиелит М.: Медицина, 1998. — С. 286.
6. Акопов Р.Х. Лечение остеомиелита у детей // Детская хирургия. -2000. №6.-С. 15-18.
7. Андронов СВ., Дмитриенков Б.И., Варламов Е.В., Губов Ю.П. Радионуклидная диагностика острого гематогенного остеомиелита длинных трубчатых костей у детей // Медицинская радиология. 1984. -№ 7. — С. 35 -39.
1984. -№ 7. — С. 35 -39.
8. Арестова С.В. Особенности диагностики и лечения острого гематогенного остеомиелита у детей первых месяцев жизни Авт. диссс.канд. мед. наук. Москва. 2005.
9. Ахмедов М.А., Рахимов А.У., Шаев Х.О. О лечении гнойных поражений суставов у детей при остеомиелите // Вестник хирургии. -1981. №7. — С. 91 -93.
10. Аюпов Р.Х. Лечение остеомиелита у детей // Казанский медицинский журнал. 1994. — № 2. — С. 118-122.
11. Багу И.С., Лаврищева Г.И., Оноприенко Г.И. Функциональная внутрикостная микроциркуляция Кишинев, 1981. — С. 19-23.
12. Баиров Г.А. Срочная хирургия детей СПб.: «Питер», 1997. — С. 428-442.
13. Баиров Г.А., Рошаль JI.M. Гнойная хирургия детей Ленинград, 1991.-С. 267.
14. Байдин С.А. Гипербарическая оксигенация у детей // Гипербарическая физиология и медицина. 1998. — № 4.
15. Белобородова Н.В. Антибактериальная защита при реконструктивных операциях высокого риска у детей // Детская хирургия. 1997.-№1.-С. 17-23.
16. Блинов Б.В. Реконструктивно-восстановительные операции на тазобедренном суставе с применением гомопластики вертлужной впадины // Ортопедия, травматология и протезирование. 1970. — №10. — С. 26-31.
17. Бойчук Н.В. и др. Гистология М., 1997. — С. 960.
18. Босин В.Ю., Ватолин К.В., Нечволодова О.Л. Рентгенодиагностика в педиатрии: Руководство для врачей Т. 2. — М.: Медицина, 1988. — С. 368.
19. Бушанская Н.А., Николаева Н.Г. Способ экспресс-диагностики острого гематогенного остеомиелита у детей, Украина, 2000042188, UAA, 17.04.2000
20. Бушмелев В.А., Стрелков Н.С. Организационные вопросы ранней диагностики и лечения острого гематогенного остеомиелита у детей // Материалы III объединенного съезда акушеров-гинекологов и детских врачей Чувашии, Чебоксары. 1992. — С. 64-65.
21. Бушмелев В.А., Стрелков Н.С. Острый гематогенный остеомиелит у детей. Учебное пособие Ижевск. — 1998. — С. 62.
22. Варламов Е.В. Ранняя топическая и дифференциальная диагностика гематогенного остеомиелита у детей Авт. дисс.канд. мед. наук. Москва. 1984.
дисс.канд. мед. наук. Москва. 1984.
23. Венгеровский И.С. Остеомиелит у детей М., 1964. — С. 270.
24. Верин В.М. К вопросу о ранней диагностике острого гематогенного остеомиелита у детей // Сб.: «Первый Белорусский международный конгресс хирургов», Витебск. 1996. — С. 67-69.
25. Вовченко А .Я., Куценок М.Б., Мельник В.В. Ультразвуковое исследование в клинике детской травматологии и ортопедии // Материалы симпозиума детских ортопедов-травматологов, С.-Пб. 1998. — С. 43-44.
26. Волкова В.В. Оперативное течение патологического вывиха бедра // В кн.: Труды I конференции молодых ученых по вопросам травматологии и ортопедии, М. 1963 — С. 182-184.
27. Гайворонский Г.И. Клинико-биохимическое обоснование течения патологического вывиха бедра у детей. Авт. дисс. . канд. мед. наук. Л. -1970.
28. Гайко Г.В. Раннее выявление, профилактика и лечение деформаций тазобедренного сустава после гематогенного остеомиелита Киев, 1984 -С. 41.
29. Гисак Н.С, Руднев В.И. , Голощаков A.M. и др. Рациональный способ дренирования и санации гнойной полости сустава при остром гематогенном остеомиелите у детей // Материалы симпозиума детских ортопедов-травматологов, СПб. 1998. — С. 39-41.
, Голощаков A.M. и др. Рациональный способ дренирования и санации гнойной полости сустава при остром гематогенном остеомиелите у детей // Материалы симпозиума детских ортопедов-травматологов, СПб. 1998. — С. 39-41.
30. Грановская Н.И., Мазурова В.К. Клинико-рентгенологическая диагностика острого гематогенного остеомиелита у детей // Клиническая рентгенология и радиология. Киев. — 1984. — Выпуск 16. — С. 27-30.
31. Григоровский В.В., Ляскина И.В., Боер В.А. Внутрикостное давление и внутрикостное кровообращение при гематогенномостеомиелите в эксперименте // Детский гематогенный остеомиелит: Тезисы республиканской научной конфкренции, Киев. 1989. — С. 7-8.
32. Гринев М.В. Остеомиелит Ленинград: Медицина, 1977. — С. 152.
33. Державин В.М. Эпифизарный остеомиелит М.: Медицина, 1965. -С. 172.
34. Дженалаев Б.К. Патогенетические основы лечения гнойной хирургической инфекции у детей первых 3 лет жизни: Авт. дисс.канд. мед. наук. Актюбинск. 1996.
35. Долганова Т. И., Куфрытев Л.М., Щуров В.А., Пожарищенский К.Э. УЗИ костной и мягких тканей у больных при опухолях и опухолеподобных поражениях длинных трубчатых костей // Гений ортопедии. 1997. -№1.- С. 5-10.
И., Куфрытев Л.М., Щуров В.А., Пожарищенский К.Э. УЗИ костной и мягких тканей у больных при опухолях и опухолеподобных поражениях длинных трубчатых костей // Гений ортопедии. 1997. -№1.- С. 5-10.
36. Долецкий С.Я., Филлипкин М;А., Хуторецкий М.Б., Самойлович Э.Ф. Электрорентгенография в педиатрии. М., 1978. — С. 168.
37. Дэвис П.А., Готефорс Л.А. Бактериальные инфекции плода и новорожденного -М.: Медицина, 1987. С. 9-105, 335-351.
38. Дяшкевич В.М. Хирургическое лечение патологического вывиха бедра у детей. Патология позвоночника и крупных суставов // Сб. научных трудов молодых ученых и спец. института, Минск. 1986. — С. 59-61.
39. Закревский Л.К. Костная гомопластика при патологических вывихах бедра // Ортопедия, травматология. — 1960. № 5. — С. 89-90.
40. Ибрагимов У.С., Шамсиев A.M., Ибрагимов С.Ю., Уринбаев П.У. Устройство для профилактики патологического вывиха бедра при остром гематогенном эпифизарном остеомиелите проксимального конца бедренной кости у детей, Узбекистан, 2005 0050, UZU, 30.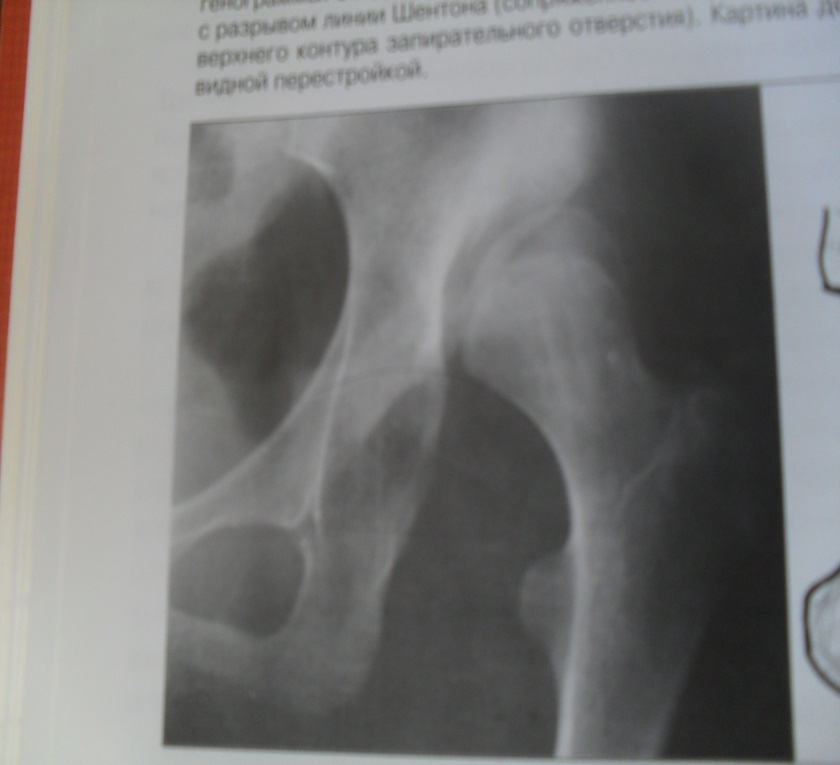 12.2005.
12.2005.
41. Исаков Ю.Ф., Белобородова Н.В. Сепсис у детей М., 2001. — С. 368.
42. Кадурина Т.И., Куликова И.С., Грачева И.Г., Ярцева З.П. Ошибки клинической диагностики при артритах у детей // Педиатрия. 1987. — № 7.-С. 62-65.
43. Кадурина Т.И., Ледащева Т.А., Куликова И.С., Грачева И.Г., Чухонина Г.Т., Белувштейн В.Р. Клинические особенности реактивного артрита у детей раннего возраста // Педиатрия. 1988. — № 3. — С. 49-53.
44. Катько В.А. Острый гематогенный остеомиелит костей, образующих тазобедренный сустав у детей // Сб.: «Первый Белорусский международный конгресс хирургов», Витебск. 1996. — С. 46-47.
45. Катько В.А. Цитологическое исследование костного мозга как метод ранней диагностики острого гематогенного остеомиелита у детей // Здравоохранение Белоруссии. 1978. — №4. — С. 48-52.
46. Катько В.А., Альхимович В.И., Абаев Ю.К., Кепеть В.А. Остеомиелит у детей: пятнадцатилетний опыт лечения // Сб.: «Первый Белорусский международный конгресс хирургов», Витебск. 1996. — С. 48-50.
1996. — С. 48-50.
47. Кепеть В.А. Регионарное кровообращение у детей с острым гематогенным остеомиелитом // Здравоохранение. 2001. — № 7. — С. 9-13.
48. Кирьянов Н.А., Стрелков Н.С., Бушмелев В.А. и др. Клинико-анатомическая характеристика острого гематогенного остеомиелита у детей // Вопросы детской хирургии и пограничных областей: Материалы межрегиональной конференции, Ижевск. 1998. — С. 115-118.
49. Кирьянов Н.А., Стрелков Н.С., Шараев П.Н. Патологоанатомическая картина ранних стадий острого гематогенного остеомиелита у детей. Экспериментальное и клиническое исследование // Российские морфологические ведомости. 1998. — №1-2. — С. 66-73.
50. Клейменов В.Н., Кузнечихин Е.П., Лактаева Л.Е. Патологический вывих бедра у детей // Проблемы детской хирургии., М. 1972. — С. 109113.
51. Ковальчук В.И. К классификации острого гематогенного остеомиелита у детей раннего возраста // Здравоохранение. 1999. — №2. -С. 38-39.
52. Ковальчук В.И. Лечение вторичных артритов у детей раннего возраста с острым гематогенным остеомиелитом // Медицинские новости. -2000. -№1. -С. 61-62.
-2000. -№1. -С. 61-62.
53. Ковальчук В.И. Ранняя внутриочаговая декомпрессия и закрытый лаваж в лечении острого гематогенного остеомиелита у детей раннего возраста // Здравоохранение. 2000. — № 1. — С. 40 — 51.
54. Ковальчук В.И., Мацкевич Б.И. Мембранодеструктивные процессы и их коррекция при остром гематогенном остеомиелите у детей // Здравоохранение Беларуси. 1994. — №10. — С. 12-15.
55. Ковальчук В.И., Мацкевич Б.И. Хирургическое лечение острого гематогенного остеомиелита у новорожденных // Детская хирургия. — 1998.-№4.-С. 14-17.
56. Ковальчук В.И., Мацкевич Б.И. Этиопатогенез острого гематогенного остеомиелита у детей раннего возраста // Медицинские новости. 1998.-№11.-С. 16-18.
57. Коптева Е.В., Машков А.Е., Верещагина В.М., Цуман В.Г., Щербина В.И. Значение белков острой фазы в оценке динамики воспалительного процесса у детей с острым гематогенным остеомиелитом // Детская хирургия. 2006. — №4. — С. 33-36.
58. Копытов Л.Ф., Батров Г.Г., Соколов Ю. Ю. Эпифизарный остеомиелит у детей раннего возраста // Новые технологии в педиатрии: Материалы конгресса педиатров России, М. 1995. — С. 153.
Ю. Эпифизарный остеомиелит у детей раннего возраста // Новые технологии в педиатрии: Материалы конгресса педиатров России, М. 1995. — С. 153.
59. Корж А.А. Доля Г Л Оперативное лечение больных, перенесших гематогенный остеомиелит Детский гематогенный остеомиелит // Тезисы докл. Респ. научной конф. 16-17 ноября, Киев-Хмельницкий. 1989. — С. 53-64.
60. Красовская В.П., Юрчук В.А. Цитологический метод исследования в ранней диагностике острого гематогенного остеомиелита у детей // Хирургия. 1997. -№11. -С. 77-81.
61. Красовская В.П., Юрчук В.А., Нерсесянц И.В. Метод ангиографии в ранней диагностике острого гематогенного остеомиелита трубчатых костей в детском возрасте // Хирургия. — 1978. — № 2. С. 103-106.
62. Красовская Т.В., Белобородова Н.В. Хирургическая инфекция у новорожденных-М.: Медицина, 1993. С. 9 — 24, 102-113.
63. Красовская Т.В., Сафонова М.В. Комплексная ультразвуковая и рентгенологическая диагностика воспалительных заболеваний костей и суставов у детей первого года жизни // Медицинская визуализация. 2000. -№3.-С. 41-46.
2000. -№3.-С. 41-46.
64. Крестьяшин В.М., Выборнов Д.Ю., Голоденко Н.В., Левитская М.В., Домарёв А.О., Арестова С.В. Первый опыт артроскопии у детей первых месяцев жизни с гнойно-воспалительным поражением тазобедренного сустава // Детская хирургия. 2003. — № 6. — С. 53.
65. Крестьяшин В.М., Выборнов Д.Ю., Красовская Т.В., Голоденко Н.В. Первый опыт использования артроскопии коленного сустава у новорожденных детей // Материалы XXI научно-практической конференции детских травматологов-ортопедов г.Москвы. 1998. — С. 2526.
66. Крестьяшин В.М. Заболевания и повреждения коленного сустава у детей (клиника, диагностика, лечение.) Авт. дисс.д-ра мед. наук. М. 1999.
67. Кривченя Д.Ю., Бурин М.Д, Данилов А.А., Корнеев Ю.Е. Современные проблемы гематогенного остеомиелита у детей // Клиническая хирургия. — 1997. №6. — С. 74 -75.
68. Крисюк А.П., Куценок Я.Б., Гук Ю.Н., Кличая-Полищук Т.А., Вовченко А .Я, Лучко Р.В. Консервативное и оперативное лечение детей спатологическим вывихом бедра // Сб. : «Первый Белорусский международный конгресс хирургов», Витебск. 1996. — С. 61-62.
: «Первый Белорусский международный конгресс хирургов», Витебск. 1996. — С. 61-62.
69. Крочек И.В. Ранняя диагностика, активная хирургическая тактика и иммунокоррекция у детей с острым гематогенным остеомиелитом Авт. дисс.канд. мед. наук. Челябинск. 1997.
70. Круминыи М.К., Калнынь Я.Я. Удлинение конечности после стабилизации тазобедренного сустава при патологическом вывихе бедра у подростков // V Всероссийский съезд травмотологов ортопедов. Ленинград. 1990. — С. 85-86.
71. Кузнечихин Е.П., Ульрих Э.В. Хирургическое лечение детей с заболеваниями и деформациями опорно-двигательной системы М.: Медицина, 2004. — С. 313-403.
72. Лапиров СБ., Каримов Ф.С. Компьютерная томография при гематогенном остеомиелите как способ контроля за регенерацией костной ткани // Новые технологии в педиатрии и детской хирургии: Материалы научно-практической конференции, Уфа. 1997. — С. 181-182.
73. Лысов А.В., Атрощенко В.П. Компьютерная томография в ранней диагностике острого гематогенного остеомиелита длинных трубчатых костей // Возможности современных методов диагностики. Омск. — 1993. -С. 93-95.
Омск. — 1993. -С. 93-95.
74. Мавыев Б.О. Ортопедическая профилактика и лечение последствий острого гематогенного остеомиелита проксимального отдела бедренной кости у детей и подростков Авт. дисс.д-ра. мед. наук. Москва. 1994.
75. Малахов О.А., Леванова В.И., Мавыев Б.О. Хирургическое лечение патологического вывиха бедра у детей // Актуальные вопросы лечения заболеваний и повреждений Опорно-двигательного аппарата у детей, СПб. 1994.-С. 156-158.
76. Малышев Е.С., Горохов A.M., Ласкина В.А. и др. Комплексные специальные исследования при гематогенном остеомиелите у детей // Хирургия. 1989. — № 11. — С. 94-97.
77. Масликов В.М. Клинические и патоморфологические данные и обоснование хирургического лечения острого остеомиелита у детей // Актуальные вопросы детской хирургии: Сборник работ, Барнаул 1995. -С. 119-121.
78. Миронов П.И., Гайнанов Ф.Х., Шарипов Н.И., Бирюкова А.В. Интенсивная терапия острого гематогенного остеомиелита у детей в современных условиях // Материалы научно-практический конференции, Уфа. 1997.-С. 181.
1997.-С. 181.
79. Миронов С.П. (под ред.). Артроскопическая хирургия тазобедренного сустава М.: 2004. — С. 98.
80. Морозова O.JL, Чеснокова Н.П., Морозов Д.А., Филиппов Ю.В. Характер системных метаболических сдвигов у детей с острым гематогенным остеомиелитом // Детская хирургия. 2006. — №5. — С. 2932.
81. Неизвестных Е.А. Отдаленные результаты лечения патологического вывиха бедра у малышей с острым гематогенным остеомиелитом // Сб: «Актуальные вопросы теоретической и практической медицины», Челябинск. 1993. — С. 121-122.
82. Нейков Г.И., Мингазов И.Т. Диагностика и лечение острого гематогенного остеомиелита у детей // Вестник хирургии им. Грекова. -1994.-№1-2.-С. 75-78.
83. Нейков Г.И., Мингазов И.Т. Сравнительная оценка методов ранней диагностики острого гематогенного остеомиелита у детей // Клиническая хирургия. 1993. — № 3. — С. 47-49.
84. Новокрещенов Л.Б., Неизвестных Е.А. Выбор способа иммобилизации в профилактике патологического вывиха бедра при метаэпифизарном остеомиелите у малышей // Новые технологии в педиатрии: Материалы конгресса педиатров России, М. — 1995. С. 165.
— 1995. С. 165.
85. Носарь А.Е. Прогнозирование распространенности остеомиелитического процесса в длинных трубчатых костях у детей и выборметода лечения. Авт. дисс.канд. мед. наук. Ленинград. 1981.
86. Нурмагамбетов Т.К. Комплексная оценка общей, местной и внутрикостной температуры в ранней топической диагностике и патогенетическом лечении острого гематогенного остеомиелита у детей Авт. дисс. канд. мед. наук. Новокузнецк. 1987.
87. Ормантаев К.С., Султанбаев Т.Ж. Внутрикостные промывания при остеомиелите у детей. Л.: Медицина, 1970. — С. 176.
88. Пак Гван Чор. Периостальная поверхность кости, ее изменение при старении и некоторых химических воздействиях Авт. дисс.канд. мед. наук. М. 2001.
89. Панов И.А, Гингольд А.З., Москалева К.А. Рентгенодиагностика в педиатрии. М.: 1972. — С. 378.
90. Переслыцких П.Ф. Экспериментально-теоретические аспекты патогенеза гематогенного остеомиелита Иркутск, 1993.-С. 146.
91. Перманов Х.П., Мухаммедкулиева А., Реджепов К. О. Способ диагностики острого гематогенного остеомиелита у новорожденных и детей грудного возраста, РФ, 93035507, А, 10.09.1996.
О. Способ диагностики острого гематогенного остеомиелита у новорожденных и детей грудного возраста, РФ, 93035507, А, 10.09.1996.
92. Привес М.Г. Кровоснабжение длинных трубчатых костей человека — Л.: Медицина, 1936. С. 260.
93. Прокопова Л.В., Николаева Н.Г., Бугаева Т.Д., Кисилевич И.М. Прогнозирование результатов лечения острого гематогенного остеомиелита у детей раннего возраста // Вестник хирургии им. Грекова. — 1990.-№1.-С. 79-81.
94. Пулатов А.Т., Сафаров А.С. Острый гематогенный эпифизарный остеомиелит у новорожденных // Сб.: «30 лет детской хирургии Таджикистана», Душанбе. 1994. — С. 130-132.
95. Пулатов А.Т., Сафаров А.С. Щадящее промывание костномозгового канала при остром гематогенном остеомиелите у детей // Сб.: «30 лет детской хирургии Таджикистана», Душанбе. 1994. — С. 135-141.
96. Райте В.К. Место компьютерной томографии в рентгенодиагностике заболеваний и повреждений костей // Компьютерная томография в клинике: Тез. I Всесоюзного симпозиума, М. 1987. — С. 164-165.
1987. — С. 164-165.
97. Рахимов С.Р. Косвенные рентгенологические симптомы острого гематогенного остеомиелита у детей // Сб.: «Первый Белорусский международный конгресс хирургов», Витебск. 1996. — С. 87.
98. Рахимова Г.Н., Ахтамов М.А., О роли условно-патогенной стафилококковой флоры в этиологии острого гематогенного остеомиелита у детей раннего возраста // Сб.: «30 лет детской хирургии Таджикистана», Душанбе. 1994. — С. 147-149.
99. Ревел П.А. Патология кости М.: Медицина, 1993. — С. 11-44.
100. Рейнберг С.А. Рентгенодиагностика заболеваний костей и суставов М.: Медицина, 1964. — С. 293-332.
101. Рубашева А.Е. Частная рентгенодиагностика заболеваний костей и суставов Киев, 1967. — С. 112-113.
102. Русак П.С. Липосомальные препараты в комплексном лечении острого гематогенного остеомиелита у детей // Детская хирургия. 1998. — №2.-С. 18-20.
103. Садофьева Г.В. Патологический вывих бедра у детей и его лечение Авт. дисс. . канд. мед. наук. М. 1965.
104. Самков А.С. Ортопедическое лечение последствий гематогенного остеомиелита у детей Авт. дисс.канд. мед. наук. М., 1984.
105. Сафаров А.С. Ультразвуковая остеометрия в диагностике острого гематогенного остеомиелита у детей // 30 лет детской хирургии Таджикистана, Душанбе. 1994. — С. 134-135.
106. Сафонова М.В, Красовская Т.В., Кармазановский Г.Г. Актуальные вопросы диагностики остеомиелита у новорожденных и грудных детей // Международный медицинский журнал. 1999. — №3-4. — С. 218-223.
107. Свешников А.А., Березовская Т.П. Использование радионуклидов для оценки репаративного костеобразования в условиях гнойной инфекции // Медицинская радиология. 1985. — №11. — С. 64-70.
108. Серов В.В., Пауков B.C. Воспаление: Руководство для врачей М.: Медицина, 1995. — С. 640.
109. Сидоренко С.В. Резистентность микроорганизмов к антибактериальной терапии // Русский медицинский журнал. 1998. — Т. 6.-№11.-С. 717-725.
110. Ситко JI.A., Лысов А.В., Конев В.П., Поспелов B. C. Щадящее лечение острого гематогенного остеомиелита у детей // Хирургия. 1992. -№11-12.-С. 80-86.
C. Щадящее лечение острого гематогенного остеомиелита у детей // Хирургия. 1992. -№11-12.-С. 80-86.
111. Смолянников А.В. Остеомиелит // Многотомное руководство по патологической анатомии. М., 1962. — Т.6. — С. 69-103.
112. Соколовский A.M., Дяшкевич В.М. Хирургическая тактика при лечении патологического вывиха и подвывиха бедра // Ортопедия, травматология. 1989. — № 10. — С. 44-49.
113. Соколовский А. М, Соколовский О.А. Патологический вывих бедра. Кн. Мн.: Выс.шк., 1997.
114. Соловьева Е.И., Иванова М.Н. Особенности клинического течения острого гематогенного остеомиелита периода новорожденности // Хирургия. 1985. — №7. — С. 89-98.
115. Сорокин В. А. Источники кровоснабжения и морфология внутриорганных кровеносных сосудов надкостницы длинных трубчатых костей свободной тазовой конечности в сравнительно-анатомическом аспекте Авт. дисс.канд. мед. наук. М., 1993.
116. Сорокин В.А. Критерии излеченности остеомиелита у детей // Сборник тезисов докладов областной научно-практической конференции детских ортопедов травматологов, Владимир. — 1994. — С. 323-326.
— 1994. — С. 323-326.
117. Степанов П.В., Сапожникова Н.И. Эхографическое исследование тазобедренного сустава у детей в возрастном аспекте // Профилактика и лечение травм и их последствий в агропромышленном комплексе: Сборник научных трудов, Смоленск. 1988. — С. 84-87.
118. Степанов Э.А., Федин А.В., Голоденко Н.В., Арестова С.В, Кузнецова З.Ю., Левитская М.В, Синицина Л.И., Фридлянд М.И. Лучевые методы в диагностике острого гематогенного остеомиелита у детей раннего возраста // Детская хирургия. 2005. — №3. — С. 4-7.
119. Стецула В.И. Патогенез острого гематогенного остеомиелита и патогенетические принципы его профилактики и лечения // Детский гематогенный остеомиелит: Тезисы Республиканской научной конференции, Киев. 1989. — С. 4-6.
120. Страчунский Л.С, Козлов С.Н. Современная антимикробная химиотерапия: Руководство для врачей М.: «Боргес», 2002. — С. 431.
121. Стрелков Н.С, Бушмелев В.А. Щадящие методы ранней диагностики и лечения острого гематогенного остеомиелита // Материалы юбилейной конференции: К 100-летию со дня рождения Терновского С. Д., М.- 1996.-С. 98-99.
Д., М.- 1996.-С. 98-99.
122. Стрелков Н.С, Кирьянов Н.А., Бушмелев В.А. Патоморфологические данные к обоснованию раннего оперативного лечения острого гематогенного остеомиелита у детей // Человек и его здоровье: Сб. научных работ. Выпуск 1.- Курск. — 1998. — С. 31-34.
123. Стрелков Н.С. Моделирование гнойного остеомиелита в эксперименте // Труды Ижевского медицинского института. Ижевск, 1995.-Т. 33. — Часть 3.-С. 114-115.
124. Стрелков Н.С. Патогенетические методы ранней диагностики и лечения острого гематогенного остеомиелита у детей Авт. дисс.д-ра. мед.наук. Ижевск. 1999.
125. Стрелков Н.С. Современные методы исследования региональной гемодинамики и их значение в ранней диагностике острого гематогенного остеомиелита // Актуальные вопросы кардиологии и ангиологии. -Ижевск. 1994.-Часть 1.-С. 81-86.
126. Струков А.И., Серов В.В. Патологическая анатомия. М.: Медицина, 1995. — С. 686.
127. Стручков В.И., Гостищев В.К., Стручков Ю.В. Хирургическая инфекция // Руководство для врачей. М.: Медицина, 1991. — С. 560.
М.: Медицина, 1991. — С. 560.
128. Суслова О.Я. Рентгенодиагностика гематогенного остеомиелита у детей // Детский гематогенный остеомиелит: Тезисы республиканской научной конференции, Киев. 1989. — С. 9-10.
129. Суслова О.Я., Шумада И.В., Меженица Е.П. Рентгенологический атлас заболеваний опорно-двигательного аппарата. Киев, 1984. — С. 158.
130. Сяурусайтис Б.Ю. Ранняя диагностика острого гематогенного остеомиелита у детей Авт. дисс. д-ра. мед. наук. Вильнюс. 1990.
131. Тимофеев СВ., Вереютин Ю.М, Лукьяненко Е.В. К вопросу о лечебной тактике при метаэпифизарном остеомиелите у детей // Сб.: «Актуальные вопросы хирургии детского возраста», Ставрополь. 1995. -С. 31-32.
132. Тихилова М.И., Джелиев И.Ш., Попович B.C., Есипов К.Т., Лолаева Б.М., Макоев В.О. Хирургические осложнения вакцинопрофилактики туберкулеза у новорожденных // Детская хирургия. 2002. — №3. — С. 3740.
133. Тодуа Ф.И., Федоров В.Н., Колесников В.А. Современная рентгенологическая и радиологическая диагностика остеомиелита // Медицинская радиология. 1988. — №4. — С. 69-73.
1988. — №4. — С. 69-73.
134. Усенко Л.В., Мальцева Л.А., Мосенцев Н.Ф, Бредун И.Н., Андриенко А.И., Сакович Е.Ф. Применение гипербарического кислорода в практике ведения больных с септической патологией // Вопросы гипербарической медицины. 2007. — №1-2. — С. 74-76.
135. Хонду А.А. Особенности внутрикостных артерий бедренной и болыпеберцовой костей у детей раннего возраста и их значение для клиники остеомиелита Авт. дисс. канд. мед. наук. Л. 1944.
136. Цуман В.Г., Машков А.Е., Щербина В.И., Савицкая К.И., Тайем X. Нарушение системы антиинфекционной резистентности и их коррекция у детей с осложненными формами гнойно-септических заболеваний // Детская хирургия. 2000. — № 1. — С. 16-20.
137. Цуман В.Г., Машков А.Е., Щербина В.И., Наливкин А.Е., Семилов Э.А., Синенкова Н.В., Суровкина М.В. Новые технологии в лечении осложненных форм гнойно-септических заболеваний у детей Детская хирургия.-2001. -№ 1.-С. 7-12.
138. Чочиев Г.М. Ортопедическая реабилитация детей и подростков с последствиями острого гематогенного остеомиелита бедренной кости Авт. дисс.канд. мед. наук. М. 1996.
дисс.канд. мед. наук. М. 1996.
139. Шамсиев A.M., Махмудов З.М., Бургутов М.Д., Мамуров Н.Р. Способ хирургического лечения острого гематогенного остеомиелита костей тазобедренного сустава у детей, Узбекистан, 2004 0048, UZC, 19.02.2004.
140. Шарипов М.И., Мавлютова М.Г., Гайнанов Ф.Х. и др. К вопросу ранней диагностики острого гематогенного остеомиелита у детей // Материалы юбилейной конференции, М. 1996. — С. 117.
141. Шастин Н.П. Возможность восстановления роста путем резекции костной спайки физиса // Детская хирургия. 2006. — № 6. — С. 29-32.
142. Шихабудинова П.А. Патологический вывих бедра у детей Авт. дисс.канд. мед. наук. М. 1999.
143. Шихабудинова П.А., Мохачев СМ., Яхьева Я.М., Асперов А.Н. Анализ консервативного и оперативного лечения патологического вывиха головки бедренной кости у детей раннего возраста // Детская хирургия. -2000.-№3.-С. 53.
144. Щитинин В.Е., Коровин С.А., Дворовенко Е.В., Щербачев В.В., Галкина Я.А., Стручкова О.Ю. Лечение острого гематогенного остеомиелита у детей // Детская хирургия. 2000. — №5. — С. 8-11.
2000. — №5. — С. 8-11.
145. Юдин Я.Б. Ошибки в диагностике и лечении острого гематогенного остеомиелита // Сов. Медицина. 1990. — №12. — С. 90-93.
146. Юлдашев М.Д., Суворова A.M., Крылова Т.Г. Особенности клиники острого гематогенного остеомиелита у детей на современном этапе // Новые технологии в педиатрии и детской хирургии: материалы научно-практической конференции, Уфа. 1997. — С. 178.
147. Aigner R.M., Fueger G.F., Rutters G et al. Results of threephase bone scintigraphy and radiography in 20 cases of neonatal osteomyelitis // Nucl. Med. Commun.- 1996. -Vol. 17, N l.-P. 20-28.
148. Aksoy MC, Ozkoc G, Alanay A, Yazici M, Ozdemir N, Surat A. Treatment of developmental dysplasia of the hip before walking: results of closed reduction and immobilization in hip spica cast. // Turk J Pediatr. 2002. Vol. 44(2)-P. 122-7.
149. Alberty A. Effects of physeal distraction on the vascular supply of the growth area: a microanglio graphical study in rebblit // J. Pediatr. Orthop. -1993.-Vol.3.-P. 373-377.
Orthop. -1993.-Vol.3.-P. 373-377.
150. Allwright S.J., Miller J.H., Gilsanz V. Subperiosteal abscess in children: scintigraphic appearance // J. Pediatr Rev. 1991.- Vol. 12, N10.- P. 292 — 297.
151. Backstein D, Hutchison C, Gross A. Septic arthritis of the hip after percutaneous femoral artery catheterization. // J Arthroplasty. 2002. — Vol. 17(8)-P. 1074-7.
152. Bauer T.M. et all. Vertebral osteomyelitis caused by group В streptococci (Streptococcus agalactiae) secondaru to urinaru tract infection // J. Clin. Microbiol, infect.-1997.-Vol.3.-P. 114-118.
153. Blom N.A., Vreede W.B. Infected cephalhematomas associated with osteomyelitis, sepsis and meningitis // J Pediatr Infect Dis. 1993. — Vol. 12. -P. 1015-1017.
154. Bonhoeffer J, Haeberle B, Schaad UB, Heininger U. Diagnosis of acute haematogenous osteomyelitis and septic arthritis: 20 years experience at the University Children’s Hospital Basel // Swiss Med WkLY 2001- 131, N. 3940. P. 575-81.
155. Borovik PI. Comprehensive treatment of acute hematogenic osteomyelitis in newborn and young infants by using dimexide and HBO therapy // Vestn Khir Im 11 Grek. 1980 — 124, N. 2. P. 135-8.
Borovik PI. Comprehensive treatment of acute hematogenic osteomyelitis in newborn and young infants by using dimexide and HBO therapy // Vestn Khir Im 11 Grek. 1980 — 124, N. 2. P. 135-8.
156. Bruns J., Lussenhop S., Behrens P. Sonographische darstelung von Weichteitumoren der Extremitaten und gelenkassoziierten Weichteilveranderungen // J Ultraschal in der Medicin. 1994. — Vol. 4. — P. 74 -80.
157. Burk D.L., Mitchell D.G., Rifcin M.D. Recent Advances in Magnetic Resonance Imaging of the Knee // J radiol clin North. 1990. — Vol. 28, N 2. -P.379-393.
158. Burk D.L., Mitchell D.G., Rifcin M.D. Recent advances in magnetic resonance imaging // Radiol. Clin. Norht. 1991. — Vol. 20, N 2. — P. 347 — 355.
159. Byrd JWT. Hip arthroscopy: basic principles and technique, SF, 2001.
160. Carek P.J., Dickerson L.M., Sack J.L. Diagnosis and management of osteomyelitis // J Am Acad Orthop Surg. 2001. — Vol. 9, N 3. — PI66 — 175.
161. Cartoni C, Capua A., Damico C, Potente G. Aspergillus osteomyelitis of the rib: sonographic diagnosis // J. Clinical Ultrasound. 1992. — Vol. 3. — P. 217-220.
Aspergillus osteomyelitis of the rib: sonographic diagnosis // J. Clinical Ultrasound. 1992. — Vol. 3. — P. 217-220.
162. Chambers J.B., Forsythe D.A., Bertrand S.L., Iwinski H.J., Steflik D.E. Retrospective review of osteoarticular infections in a pediatric sickle cell age group // J Unfallchirurg. 1998. — Vol. 101,N 9. — P. 662 — 673.
163. Chao H.C., Lin S.J., Huang Y.C., Lin T.Y. Color Doppler ultrasonographic evaluation of osteomyelitis in children // J Pediatr Orthop. -1999. Vol. 19, N 2.- P.143-150.
164. Chen C.H., Lee Z.L., Yang W.E., Lin T.Y., Shih C.H. Acute septic arthritis of the hip in children—clinical analyses of 31 cases // J Orthop Rev. -1993.- Vol. 22,N8.-P. 925-928.
165. Civardi G., Livragni Т., Colombo P. Ultrasonically Guided Fine-Needle Aspiration Biopsy // J Clin. Ujtrasound. 1994. — Vol. 22. — P. 307 — 314.
166. Conwey J.J. Radionuclide bone scintigraphy in pediatric ortopedics // J Pediatr Clin North. 1986. — Vol. 33, N6. — P. 1313 — 1334.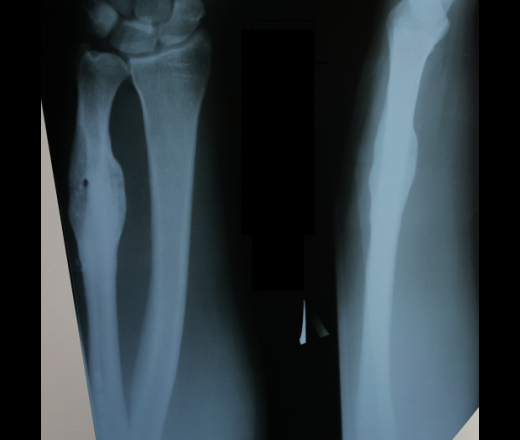
167. Crha В., Janovec M., Poul J. Neonatal osteomyelitis is still a reality // J Pediatr Orthop. 1990. — Vol. 10, N 5.- P.649 — 652.
168. Datz F.L. Radionuclide Imaging of Joint Inflammation in the 90s // J Nucl. Med. 1990. — Vol. 31, N 5. — P. 684 — 687.
169. De Angelis NA, Busconi BD, Hip arthroscopy in the pediatric population // Clin. Ortop.- 2003 Jan.(406) 60-3.
170. Demirhan M, Dikici F, Eralp L, Onen M, Goksan B. A treatment algorithm for developmental dysplasia of the hip for infants 0 to 18 months ofage and its prospective results // Acta Orthop Traumatol Turc. 2002. Vol. 36(1)-P. 42-51.
171. Dietz H.G., Bachmeyr A., Joppich I. Osteomyelitis in children // J Oral MaxillofaSurg.-2003.-Vol.32, N 5.-P.459 468.
172. Dobbs MB, Sheridan JJ, Gordon JE, Corley CL, Szymanski DA, Schoenecker PL. Septic arthritis of the hip in infancy: long-term follow-up. // J Pediatr Orthop. 2003. — Vol. 23(2) — P. 162-8.
173. Donowan-Post M.J., Bowen B.C., Sze G. Magnetic resonance imaging of spinal infection //Rheum Dis Clin Norht. 1991. — Vol. 17. — P. 773 — 794.
Magnetic resonance imaging of spinal infection //Rheum Dis Clin Norht. 1991. — Vol. 17. — P. 773 — 794.
174. Dormans J.P., Drummond D.S. Pediatric Hematogenous Osteomyelitis: New Trends in Presentation, Diagnosis, and Treatment // J Ultrasound Med. -1999. Vol. 18, N 11. — P. 729-734.
175. Dresing K., Sturmer K.M. Diagnosis and therapy of pediatric and juvenile hematogenous osteomyelitis // J.Pediatr.-1998.-Vol.l57, N 1.-P28-33.
176. Erasmie U., Hirsch G. Acute haematogenous osteomyelitis in children -the reliability of skeletal scintigraphy // J Radiology. 1980.- Vol. 135, N 3. — P. 731 — 736.
177. Farrell C, O’hara A.E. The use of thermography in the pediatric patient. A new diagnostic tool // Clin. Pediatr. 1972. — Vol. 11. — P. 673 — 683.
178. Finegold S. Host factors predisposing to anaerobic infections. FEMS Immunol //Med. Microbiol. 1993. — Vol. 6, N 2 — 3. — P. 159 — 163.
179. Forward DP, Hunter JB. Arthroscopic washout of the shoulder for septic arthritis in infants. A new technique. // J Bone Joint Surg Br. 2002. — Vol. 84(8)-P. 1173-5.
A new technique. // J Bone Joint Surg Br. 2002. — Vol. 84(8)-P. 1173-5.
180. Gandini D. Acute septic arthritis of the hip in children in northern Australia. // ANZ J Surg. 2003. — Vol. 73(3) — P. 136-9.
181. Garkavenko Iu.E., Bergaliev A.N., Pozdeev A.P., Sadofeva V.I. The effects of lengthening the femur in children with sequelae of hematogenic osteomyelitis on the state of the stabilized hip joint // J Infection. 2000. -Vol.28, N 5.-P.282- 286.
182. Gavilan M.G., Lopez J.B., Artola B.S. Peculiarities of osteo-articular infections in children // J Am Acad Orthop Surg. 1994. — Vol. 2, N 6. — P.333 -341.
183. Geissler W., Pumberger W., Wurnig P., Stuhr O. BCG osteomyelitis as a rare cause of mediastinal tumor in a one-year-old child // J. Radiology. 1991.-Vol. 79, N3.-P. 725-729.
184. Girschick H.J., Krauspe R., Tschammler A., Huppertz H.I. Diagnosis and therapy of pediatric and juvenile hematogenous osteomyelitis // J Orthopade. -1997.- Vol. 26, N 10. P.894 — 901.
185. Gold R. Diagnosis of osteomyelitis // J. Bone Joint Surg Am. -1991.-Vol. 73, Nl.-P. 37-51.
186. Gold R., Hawkins R.A., Katz R.D. Bacterial osteomyelitis: findings on plainradiography, CT, MR and scintigraphy // J. Roentgenol. 1991. — Vol. 157. — P.365-370.
187. Gordon JE, Huang M, Dobbs M, Luhmann SJ, Szymanski DA, Schoenecker PL. Causes of false-negative ultrasound scans in the diagnosis of septic arthritis of the hip in children. // Pediatr Orthop. 2002. — Vol. 22(3) — P. 312-6.
188. Graf R., Tschaunder C. Sonography of the infant hip: sources of error: progress and current clinical relevance. Radiologe 1994; 34: 30-38.
189. Guo Z, Dong F, Chen J, Xu X. 311 cases of chronic osteomyelitis treated by soaking with ganlingsan liquid // J Tradit Chin Med. 1999 — 19, N. 2. P. 100-4.
190. Gupta N.C. Presio LA. Radionuclide imaging in osteomyelitis // Semin Nucl Med. 1988. — Vol. 18. — P. 287 — 299.
191. Handmaker H., Giammona S.T. Improved early diagnosis of acute inflammatory skeletal-articular diseases in children: a two-radiopharmaceutical approach // Pediatrics. 1984. — Vol. 73, N 5. — P. 661- 669.
1984. — Vol. 73, N 5. — P. 661- 669.
192. Haskney D.B. Inflamation, infection, cavitary disorders and ischemia // Top Magn Reson Imaging. 1992. — Vol. 4. — P 62 — 77.
193. Hempfing A., Placzek R., Gottsche Т., Meiss A.L. Primary subacute epiphyseal and metaepiphyseal osteomyelitis in children, diagnosis and treatment guidedbyMRI//JPediatrOrthopB.-2003.-Vol. 12,N2.-P. 151 -154.
194. Holder L.E. Clinical Radionuclide Bone Imaging. Radiology. — 1990. -Vol. 176.-P. 607-614.
195. Ho wand C.B. Diagnosis of osteomyelitis // J. Bone Joint Surg Am. -1994.- Vol. 76, N2.-P. 311-314.
196. Hsu Y.P., Su C.C., Chih C.J., Wei K.Y. Septic arthritis of adult hip treated by total hip replacement~a case report // J Pediatr Orthop. 1996. — Vol. 16, N 2. — P.224 — 230.
197. Jager H.J. Schmitz-Stolbrink A., Gotz G.F. et all. Invasion of the growth plate by bone tumors and osteomyelitis in childhood // Radiologe. 1995. -Vol.35,N6.-P. 409-413.
198. Jung ST, Rowe SM, Moon ES, Song EK, Yoon TR, Seo HY. Significance of laboratory and radiologic findings for differentiating between septic arthritis and transient synovitis of the hip. // J Pediatr Orthop. — 2003. Vol. 23(3)-P. 368-72.
Significance of laboratory and radiologic findings for differentiating between septic arthritis and transient synovitis of the hip. // J Pediatr Orthop. — 2003. Vol. 23(3)-P. 368-72.
199. Jaramillo D., Treves S.T., Kasser J.R., Harper M., Sundel R., Laor T. Osteomyelitis and septic arthritis in children: appropriate use of imaging to guide threatment // J. Roentgenol. 1995. — Vol. 165, N2. — P. 399 — 403.
200. Jellis J. Heamatogenous osteomyelitis // Surgery. 1992. — Vol. 18. — P. 145 — 148.
201. Joosten K.F., Hazelzet J.A., Tiddens H.A., Hazebroek F.W., Dzoljic-Danilovic G., Neijens H.J., de Groot R. Ultrasonic signs of pelvic osteomyelitis in children // J Pediatr Radiol. 1994. — Vol. 24, N 7. — P. 484 — 487.
202. Kabak S, Halici M, Akcakus M, Cetin N, Narin N. Septic arthritis in patients followed-up in neonatal intensive care unit. // Pediatr Int. 2002. -Vol. 44(6) — P. 652-7.
203. Kalouche I, Ghanem I, Kharrat K, Dagher F. Osteomyelitis of the rib due to Streptococcus pneumoniae: a very rare condition in children // J Pediatr Orthop В. — 2005.- Vol. 14,N1.-P. 55-60.
— 2005.- Vol. 14,N1.-P. 55-60.
204. Khachatourians AG, Patzakis MJ, Roidis N, Holtom PD. Laboratory monitoring in pediatric acute osteomyelitis and septic arthritis. // Clin Orthop. -2003.-Vol. 409-P. 186-94.
205. Kiepurska A. Kiepurska A. Kiepurska A. Ultrasonic signs of pelvic osteomyelitis in children // J Changgeng Yi Xue Za Zhi. 1993. — Vol. 16, N 4. — P. 239 — 245.
206. Kim SJ, Choi NH, Ко SH, Linton JA, Park HW. Arthroscopic treatment of septic arthritis of the hip. // Clin Orthop. 2003. — Vol. 407 — P. 211-4.
207. Klein JD, Leach KA. Pediatric pelvic osteomyelitis. // Clin Pediatr (Phila) 2007. — Vol. 46, N. 9. — P. 787-90.
208. Krebs VE. The role of hip arthroscopy in the treatment of synovial disorders and loose bodies. // Clin Orthop. 2003. — Vol. 406 — P. 48-59.
209. Kuliev RA, Kuliev AM. Ultrasonic cavitation in the treatment of acute hematogenous osteomyelitis in children // Vestn Khir Im 11 Grek 1986 — 137, N. 12. P. 71-4.
210. Kursunoglu-BrahmeS. , Gundry C.R., Resnic D. Advansed Immaging of the Wrist // Radiol Clin North. 1990. — Vol. 28, N 2. — P. 307 — 320.
, Gundry C.R., Resnic D. Advansed Immaging of the Wrist // Radiol Clin North. 1990. — Vol. 28, N 2. — P. 307 — 320.
211. Langenskjold A., Videman Т., Nevalainen T. The Fate of FA Transplants in Operations for Partial Closure of the Growth Plate. Clinical Examples and an Experimental Study // J. Bone Jt Surg. 1986. — Vol. 68B. — P. 234-238.
212. Langer R., Kaufmann H.J. Complex special examination of children with hematogenic osteomyelitis // J Bone Joint Surg Br. 1988. — Vol. 70(5). — P 818 — 820.
213. Laughlin R.T., Wright D.S., Mader J.T., Caihoun J.H. Osteomyelitis // Curr. Opin. Rheumatol.- 1995.-Vol. 7,N4.-P. 315-321.
214. Lazzarini L, Mader JT, Calhoun JH. Osteomyelitis in long bones // J Bone Joint Surg Am. 2004. -Vol. 86, N.10. -P. 2305 — 2318.
215. Lee E.H., Gao G.X., Bose K. Management of partial growth arrest: physis, tet, or silastic ? //J Pediatr Orthop. 1993. — Vol. 3. — P. 368 — 372.
216. Lejman T, Strong M, Michno P. Septic arthritis in newborns and infants. Treatment of hip arthritis // Chir Narzadow Ruchu Ortop Pol. 1996 — 61, N. 6.- P. 567-77.
Treatment of hip arthritis // Chir Narzadow Ruchu Ortop Pol. 1996 — 61, N. 6.- P. 567-77.
217. Letts R.M., Afibi A., Sutherland J.B. Technetium bone scanning as an aid in the diagnosis of atypical acute osteomyelitis in arthritis // J. Bone Joint Surg.- 1975.-Vol. 39.-P. 1183 1186.
218. Liderman K. Klinische Probleme der Osteomyelitis // Dtsch. Orth. Ges., Verh., 51 Kongress. Stuttgart, 1975. — S. 77.
219. Lipczyk Z, Niedzielski J, Midel A, Krol R. Management of early symptoms of acute septic hip in neonates and infants—conservative or surgical? // Chir Narzadow Ruchu Ortop Pol. 2001 — Vol. 66, N. 5. — P. 429-34.
220. Longjohn D.B., Zionts L.E., Stott N.S. Acute hematogenous osteomyelitis of the epiphysis // Clin. Orthop. 1995. — Vol. 316. — P. 227 — 234.
221. Mah E.T., LeQuesne G.W., Gent R.J., Paterson D.C. Ultrasonic features of acute osteomyelitis in children. J Bone Joint Surg (Br) 1994; 76-B; 969-974.
222. Mah E.T., LeQuesne G.W., Gent R.J., Paterson D.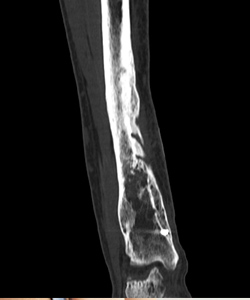 C. Ultrasonic signs of pelvic osteomyelitis in children // J. Orthop Rev.- 1993.- Vol. 22(8).- P. 925 -928.
C. Ultrasonic signs of pelvic osteomyelitis in children // J. Orthop Rev.- 1993.- Vol. 22(8).- P. 925 -928.
223. Mahan S., Jolles P.R., MAI osteomyelitis. 18-year scintigraphic follow-up // Clin. Nucl. Med. 1995. — Vol. 20, N 7. — P. 594 — 596.
224. Merino Arribas J, Carpintero Martin I, Marrero Calvo M, Anso Olivan S, Elvira Pardilla A, Iglesias Escalera G. Acute osteomyelitis. Clinical, radiological and bacteriological features and outcome // An Esp Pediatr. 2001 — 55, N. l.P. 20-4.
225. Mine J.H., Reicher M.A., Crues J.V. Magnetic Resonance Imaging of the Knee // J. Orthop Rev.-1993.- Vol. 23, N 9.- P. 925 -928.
226. Nade S. Septic arthritis. // Best Pract Res Clin Rheumatol. 2003. — Vol. 17(2)-P. 183-200.
227. Offiah AC. Acute osteomyelitis, septic arthritis and discitis: differences between neonates and older children // Eur J Radiol 2006- 60, N. 2. P. 221-32.
228. Parsch K., Wiedmann H. Diagnose und Therapie der septischen arthritis (coxitis) // Z. Orthop. 1990.-Bd.l28.-s.396-403.
Orthop. 1990.-Bd.l28.-s.396-403.
229. Pineda C, Vargas A, Rodriguez AV. Imaging of osteomyelitis: current concepts // Infect Dis Clin North Am 2006 — 20, N. 4. P. 789-825.
230. Poilane I., Fawaz F., Nathanson M., Cruaud P., et all. Corynebacterium diphtheriae osteomyelitis in an immunocompetent child: a case report // Eur J Pediatr. 1995. -Vol. 154, N 4. -P. 381-383.
231. Radio W., Michno P., Kotulski D. Subacute osteomyelitis in children // J Eur Radiol.- 2003.- Vol. 79, N 10.- P. 932 937.
232. Rankine J J., Barron D.A., Robinson P., Millner P.A., Dickson R.A. Osteomyelitis in children // Postgrad Med J. 2004. — Vol. 80, N 10, — P. 607609.
233. Riebel T.W., Nasir R., Nasarenko O. The value of sonography in the detection of osteomyelitis // Pediatr Radiol. 1996. — Vol. 26, N 4. — P. 291 -297.
234. Rubin L.P., Wallach M.T., Wood B.P. Radiological case of the month. Neonatal osteomyelitis diagnosed by ultrasound. Arch Pediatr Adolesc Med, 1996.-P. 53-55.
235. Sanchez A.A., Hennrikus W.L. Arthroscopicaly assisted treatment of acute septic knees in infant using The microjoint arthroscope // Arthroscopy N13(3) 1997 P.350(4)
236. Sattler H. Artrosonography. New York, 1990. — 314 p.
237. Schauwecker D.S. The Scintigraphic of Osteomyelitis // Roentgenol. -1992.-Vol. 159.-P. 9-18.
238. Schauwecker D.S., Braunstein E.M., Wheat L.J. Diagnostic imaging of osteomyelitis // Infect Dia Clin Norht. 1990. — Vol. 4. — P. 441 — 463.
239. Schmidt H.G.K., Neikes M., Wittec F. Zur Klassifizierung der Osteomyelitis // Acta Traumat. 1990. — Bd 20, N 6. — S. 303 — 309.
240. Schmit P., Glorion C. Osteomyelitis in infants and children // J Bone Joint Surg Br. 2003. — Vol. 85(4). — P. 559 — 564.
241. Sichardt G., Hofmann-von Kap-herr S. Acute multilocular osteomyelitis ininfancy and childhood // Acta Chir Orthop Traumatol Cech. 1991.- Vol. 58, N 1-2.-P. 28-36.
242. Smith SP, Thyoka M, Lavy CB, Pitani A. Septic arthritis of the shoulder in children in Malawi. A randomised, prospective study of aspiration versus arthrotomy and washout. // J Bone Joint Surg Br. 2002. — Vol. 84(8) — P. 1167-72.
A randomised, prospective study of aspiration versus arthrotomy and washout. // J Bone Joint Surg Br. 2002. — Vol. 84(8) — P. 1167-72.
243. Song K.M., Sloboda J.F. Acute hematogenous osteomyelitis in children // JBone Joint Surg Br. 2003. — Vol. 85, N.4. — P. 559 — 564.
244. Sorensen T.S., Hedeboe J., Christensen E.R. Primary epiphyseal osteomyelitis in children. Report of three cases and review of the literature // JPediatr Surg. 1988.- Vol. 23, N 8.- P. 779 — 781.
245. Spiegel D.A, Meyer J.S, Dormans J.P., Flynn J.M., Drummond D.S. Pyomyositis in children and adolescents: report of 12 cases and review of the literature // J.Pediatrics.-1998.-Vol.l02, N 6.-P.1376-1382.
246. Sponseller P.D., Malech H.L., McCarthy E.F. Jr, Horowitz S.F., Jaffe G., Gallin J.I. Osteomyelitis in children // J Chir Narzadow Ruchu Ortop Pol. -2003,- Vol. 68, N4.-P. 231-235.
247. Stephenson C.A., Seibert J.J., McAndrew H.P. et all. Sonographic diagnosis of tenosynovitis of the posterior tibial tendon // J Clinic. Ultrasound. -1990. -№ 2. -P. 114-117.
Ultrasound. -1990. -№ 2. -P. 114-117.
248. Stuart J.E., McHale K.A., Elias S., Mason J. Piriformis abscess mimicking a hip pyarthrosis // J. Am Acad Orthop Surg. 1992.-Vol.1 1-12.-P.80-86.
249. Sullivan D.C., Rosenfield N.S., Ogden J., Gottschalk A. Problems in the scintigraphic detection of osteomyelitis in children // J Acta Chir Orthop Traumatol Cech.- 2004.- Vol. 71,N 4.- P. 220 227.
250. Tang J.S.H., Gold R.H., Basett L.W., Seeger L. Musculoskeletal infection of extremites: evaluations with MR imaging // J. Radiology. 1988. -Vol. 166. — P. 205-209.
251. Thomas S, Tytherleigh-Strong G, Dodds R. Adductor myositis as a cause of childhood hip pain. // J Pediatr Orthop B. 2002. — Vol. 11(2) — P. 117-20.
252. Tsai J.C., Zlatkin M.B. Magnetic Resonance Imaging // J. Am Acad Orthop/ Surg. 1990.-Vol.28, N 2. — P.279 — 291.
253. Vestad E. Coxitis in children // J Pediatr Surg. 1992. — Vol. 2(2). — P. 118-121.
254. Wathne КО, Babovic A, Nordshus T. Acute osteomyelitis in young children—a diagnostic challenge // Tidsskr Nor Laegeforen 2001 — 121, N..jpg) 14. P. 1693-6.
14. P. 1693-6.
255. Xu XZ. Clinical study of soaked treatment of chronic osteomyelitis with herbal medicine // Zhong Xi Yi Jie He Za Zhi 1990 — 10, N. 11. P. 648-51.
256. Yamamoto Y, Ide T, Hachisuka N, Maekawa S, Akamatsu N. Arthroscopic surgery for septic arthritis of the hip joint in 4 adults. // Arthroscopy. 2001 Mar;17(3):290-297.
257. Yeh TC, Chiu NC, Li WC, Chi H, Lee YJ, Huang FY. Characteristics of primary osteomyelitis among children in a medical center in Taipei, 1984-2002 // J Formos Med Assoc. 2005. — Vol.104, N. 1. — P. 29 — 33.36.41.
Остеомиелит у детей: этиология, патогенез, клиника, диагностика и лечение
На правах рукописи
Цыбин Анатолий Александрович
ОСТЕОМИЕЛИТ У ДЕТЕЙ: ЭТИОЛОГИЯ, ПАТОГЕНЕЗ, КЛИНИКА, ДИАГНОСТИКА И ЛЕЧЕНИЕ
14.01.19 — детская хирургия
Автореферат
Диссертации на соискание ученой степени доктора медицинских наук
1 я ДПР ¿013
005051915
Работа выполнена в Государственном бюджетном учреждении здравоохранения Московской области «Московский областной научно-исследовательский институт им.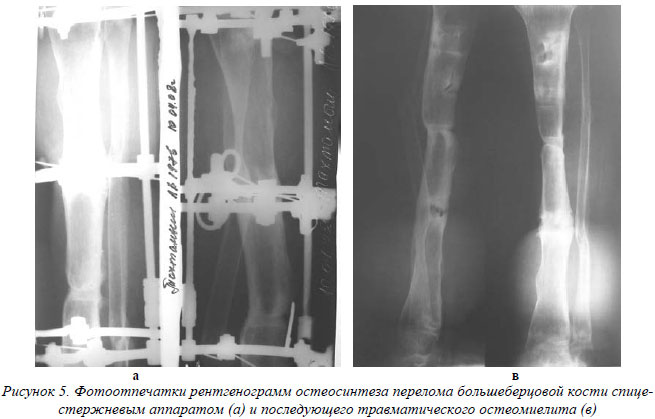 М.Ф Владимирского»
М.Ф Владимирского»
Научный консультатнт:
доктор медицинских наук профессор Машков Александр Евгеньевич
Официальные оппоненты:
Заслуженный деятель науки РФ, доктор медицинских наук, профессор кафедры детской хирургии, педиатрического факультета Российского национального исследовательского медицинского университета им. Н.И. Пирогова
Министерства Здравоохранения РФ Дронов Анатолий Федорович
доктор медицинских наук, профессор, заведующий кафедрой детской хирургии Российской медицинской академии последипломного образования
Министерства Здравоохранения РФ Соколов Юрий Юрьевич
доктор медицинских наук, профессор, заведующий кафедрой детской хирургии Воронежской Государственной медицинской академии им. H.H. Бурденко Министерства
Здравоохранения РФ Веч ркин Владимир Александрович
Ведущее учреждение «Московский Государственный медико -стоматологический Университет им. А.И. Евдокимова» Министерства Здравоохранения РФ
Защита состоится «_» «_» 20_года в_часов на
заседании диссертационного совета Д 208. 072.02 на базе ГБОУ ВПО РНИМУ им. Н.И.Пирогова Минздрава России по адресу: 117997, г. Москва, ул. Островитянова, д. 1.
072.02 на базе ГБОУ ВПО РНИМУ им. Н.И.Пирогова Минздрава России по адресу: 117997, г. Москва, ул. Островитянова, д. 1.
С диссертацией можно ознакомиться в Научной библиотеке ГБОУ ВПО РНИМУ им. Н.И.Пирогова Минздрава России по адресу: 117997, г. Москва, ул. Островитянова, д. 1
Автореферат разослан «……….»……………………….2013 года
Ученый секретарь диссертационного совета
доктор медицинских наук, профессор H.H. Котлукова
ОБЩАЯ ХАРАКТЕРИСТИКА РАБОТЫ Актуальность проблемы
Остеомиелит представляет собой один из наиболее сложных вариантов воспалительного процесса, о чем свидетельствуют трудности диагностики, лечения, относительно большое число осложнений и сложности реабилитации.
Отсутствие специфических методов выявления гематогенной природы остеомиелита в ранние сроки, является причиной диагностических и лечебно-тактических ошибок превышающих 50%. Посттрвматический остеомиелит легко распознается, но также трудно поддается лечению.
Частота возникновения острого гематогенного остеомиелита, который является преимущественно патологией детского организма, по данным многих авторов составляет 6-10% от числа больных с гнойными заболеваниями. В последние годы этот процент значительно уменьшился до 2-3 %. Однако изменилась возрастная структура заболеваемости и сдвинулась в новорожденный возраст и внутриутробный период. Переход заболевания в хроническую стадию до сих пор остается высоким и колеблется от 10 до 40%.
Вопросы профилактики осложнений и лечения последствий гематогенного остеомиелита вызывают дискуссию среди ученых и клиницистов. Неудачи и осложнения при лечении последствий ГО имеет место у 12-31%, а по отдельным видам — у 54,5% лечившихся детей. Большинство таких случаев требуют повторных хирургических вмешательств со значительным риском для жизни, и зачастую с неблагоприятным функциональным прогнозом пораженного сегмента.
Не до конца раскрыты и изучены механизмы таких осложнений как, хронизация, генерализация инфекции и процессов обширного остеонекроза.
Одним из основных патогенетических факторов при ГО является эндотоксикоз. Вероятно, решение проблемы инфекционно-воспалительного токсикоза связано с дальнейшим развитием концепции эндотоксикоза, изучением его более глубоких и тонких механизмов. Современный комплекс интенсивной терапии при остеомиелите (ДПА, иммунотерапия Т-активином, ГБО, антиоксидантное лечение, местное воздействие ЛТ при помощи ГНЛ) эффективен, оказывает положительное воздействие и стабилизирует общее состояние больного.
Однако основным в лечении остается хирургическая санация очага. При хирургическом лечении остеомиелита возникает проблема контроля и управления над процессом воспаления, протекающим в зоне оперативного вмешательства, это усложняет лечение и отягощает течение и прогноз заболевания.
Операция остеоперфорации в острой стадии тяжелого течения заболевания гематогенной природы и фистулсеквестрнекрэктомия в хронической фазе, недостаточно эффективна. Требует повторных травматичных операций. Это способствует увеличению частоты перехода остеомиелита в хроническую стадию или генерализации остеомиелитическо-го процесса с развитием сепсиса. Формирование хронического, длительно существующего гнойного очага, трудно поддается лечению. Важным моментом в комплексе лечебных мероприятий, является их патогенетическое обоснование. Радикальное удаление очага у детей не приемлемо. Это свидетельствуют об актуальности проблемы остеомиелита у детей и побуждают исследователей к изучению вопросов, имеющих наибольшее практическое значение.
Это способствует увеличению частоты перехода остеомиелита в хроническую стадию или генерализации остеомиелитическо-го процесса с развитием сепсиса. Формирование хронического, длительно существующего гнойного очага, трудно поддается лечению. Важным моментом в комплексе лечебных мероприятий, является их патогенетическое обоснование. Радикальное удаление очага у детей не приемлемо. Это свидетельствуют об актуальности проблемы остеомиелита у детей и побуждают исследователей к изучению вопросов, имеющих наибольшее практическое значение.
Таким образом, в изучении этиологии и патогенеза, а также лечении остеомиелита, его рецидивов и осложнений существует много нерешенных проблем, углубленная разработка которых может способствовать улучшению результатов комплексного лечения исследуемого заболевания и решению
проблемы в целом.
Вышеизложенные обстоятельства, подтверждают необходимость дальнейшего изучения патогенеза ГО, без учета которых лечение становится менее результативным.
ЦЕЛЬ РАБОТЫ: Улучшить результаты лечения остеомиелита и его осложнений у детей, путем разработки нового хирургического способа лечения заболевания, на основе нового концептуального подхода и патогенетического воздействия на воспалительный процесс.
ЗАДАЧИ ИССЛЕДОВАНИЯ.
1. На основе обзора литературы провести изучение и анализ существующих основных аспектов этиологии, патогенеза, клиники, диагностики, и лечения остеомиелита у детей. Представить общую характеристику исследования.
2. Изучить этиологическую структуру гнойного очага, ее динамику и роль иммунобиологических аспектов патогенеза гематогенного остеомиелита у детей.
3. Определить причины и закономерности перехода острого гематогенного остеомиелита в хроническую стадию.
4. Изучить влияние комплекса лечебных мероприятий на особенности и закономерности патогенеза острой стадии остеомиелита у детей, перехода ее в хроническую фазу и морфологическое состояние хронического очага остеомиелита.
5. Разработать новый подход и патогенетически обоснованный способ лечения гнойного очага при остеомиелите у детей (длительное непрерывное аспирационное дренирование костного гнойного очага). Изучить, цитологическую, и рентгенологическую, структуру гнойного очага при остеомиелите у детей в динамике в целях контроля воспаления и определения сроков аспирационного дренирования.
6. Обосновать новую концепцию и схему лечебного патогенетического воздействия на воспалительный процесс (общий и локальный) при остеомиелите у детей на основании системного анализа литературы и результатов собственных исследований.
7. Провести анализ эффективности оригинального комплекса лечебных мероприятий, сформулированных в настоящей работе.
НАУЧНАЯ НОВИЗНА
В работе, впервые, изучено клиническое применение нового оригинального способа — длительного непрерывного аспирационного дренирования костного гнойного очага (ДНАДКГО) при остеомиелите и ран мягких тканей у детей (авторское свидетельство № 1769867 1990 г. ).
).
Уточнена возможность и определены показания его применения как альтернативы радикальному удалению пораженной кости. Раскрыты и уточнены механизмы гидродинамики в остеомиелитическом очаге при использовании аспирационного дренирования.
Впервые регламентирована и патогенетически обоснована длительность сроков аспирационного дренирования гнойного воспалительного очага при остеомиелите и гнойном воспалении мягких тканей при данном заболевании (Патент РФ № 2412724,РФ,2009г.).
Предложены новый способ, и устройства для обработки кости — набор гибких свёрел и фрез (Патент РФ № 1780504, 1992).
Изучены и выявлены закономерности течения регенераторного процесса в пораженной остеомиелитом кости и ране мягких тканей при применяемой методике аспирационного дренирования. Разработана, апробирована и внедрена методика цитологического контроля над воспалительным процессом в очаге, позволяющая в динамике наблюдать и объективизировать регенераторные механизмы костной ткани (патент РФ № 2412724,РФ,2009г).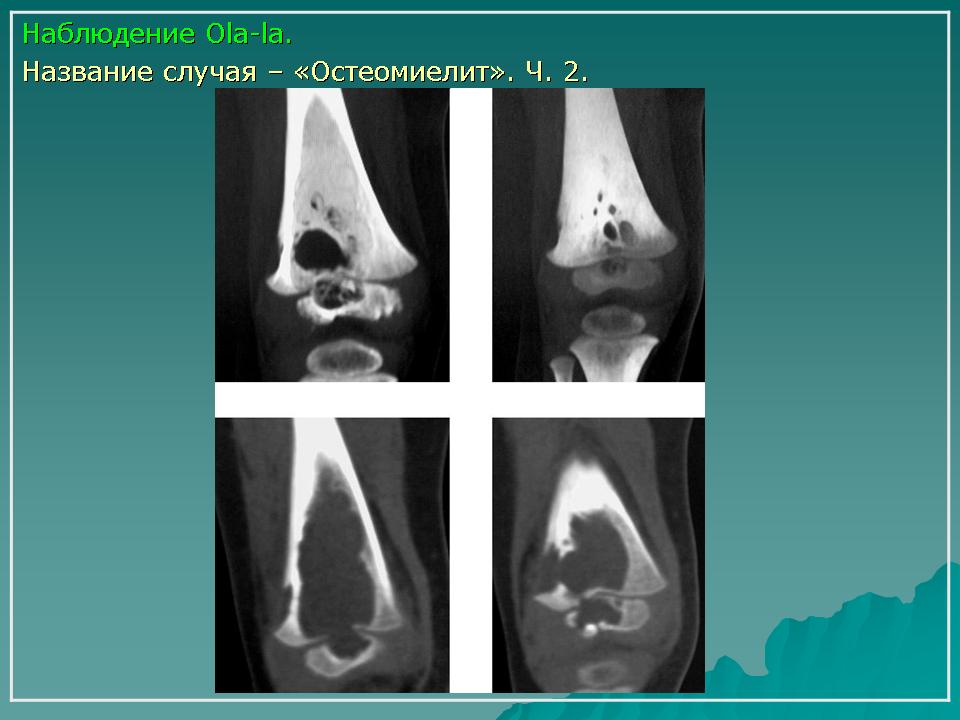 В известной степени, через местный очаг контролировать
В известной степени, через местный очаг контролировать
в целом процесс остеомиелитического воспаления в организме ребенка.
Доказаны преимущества нового хирургического способа лечения остеомиелита. Его способность предупредить деструкцию кости, распространение гнойно-воспалительного процесса за ее пределы. Остановить продолжающееся разрушение костной ткани и связанные с ними осложнения, за счет балансирующего, оптимизирующего и стимулирующего влияния на острую и хроническую стадии воспаления и в период восстановительных, регенераторных процессов. Это позволяет создать целое направление регенеративной хирургии костной ткани.
Разработана оригинальная концепция и практическая схема патогенеза остеомиелита, представляющая доказательство, что острый и хронический остеомиелит являются стадиями единого гнойно-воспалительного процесса в кости. Открыт порочный цикл патогенеза. Схема патогенеза подтверждает патогенетическую обоснованность и высокую эффективность нового способа хирургического лечения.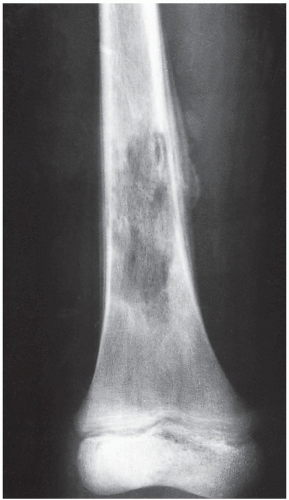
Доказана возможность и необходимость длительной аспирации патологического содержимого из остеомиелитического очага до момента регенерации основных костных структур. Впервые показано, что длительное дренирование при соблюдении методики гарантирует излечение от остеомиелита в любой стадии заболевания за счет устранения основных звеньев патогенеза.
ПРАКТИЧЕСКАЯ ЗНАЧИМОСТЬ
Проведенное исследование позволило разработать, оценить и применить новый хирургический способ длительного непрерывного аспирационного дренирования костного гнойного очага в лечении остеомиелита, и профилактике его осложнений у детей. Способ стимулирует регенераторный процесс в кости и мягких тканях. Позволяет добиться излечения от остеомиелита. Методика проста и доступна, не требует дополнительных
материальных и финансовых затрат, может использоваться в специализированном отделении. При раннем применении новый способ наружного дренирования очага остеомиелита предупреждает деструкцию кости. В случае запаздывания с оперативным лечением по причине диагностических или тактических ошибок способ позволяет остановить нарастающую деструкцию кости, и способствует в дальнейшем полной регенерации разрушенной костной ткани с функциональным восстановлением больного сегмента.
В случае запаздывания с оперативным лечением по причине диагностических или тактических ошибок способ позволяет остановить нарастающую деструкцию кости, и способствует в дальнейшем полной регенерации разрушенной костной ткани с функциональным восстановлением больного сегмента.
Длительное непрерывное аспирационное дренирование остеомиелитического очага и раны обладает многофакторным действием на организм ребенка и дает возможность осуществлять контроль и управление воспалительным процессом в очаге. Это благоприятно отражается на течении воспалительного процесса в целом. Длительный цитологический контроль над очагом остеомиелита позволяет прогнозировать восстановительные процессы в кости. Это способствует быстрой элиминации продуктов воспаления из очага и микробной деконтаминации. Своевременное применение методики в целях комплексной профилактики предупреждает осложнения в послеоперационной ране, костную деструкцию в остеомиелитическом очаге, и развитие общих осложнений с неудовлетворительными и неблагоприятными исходами заболевания.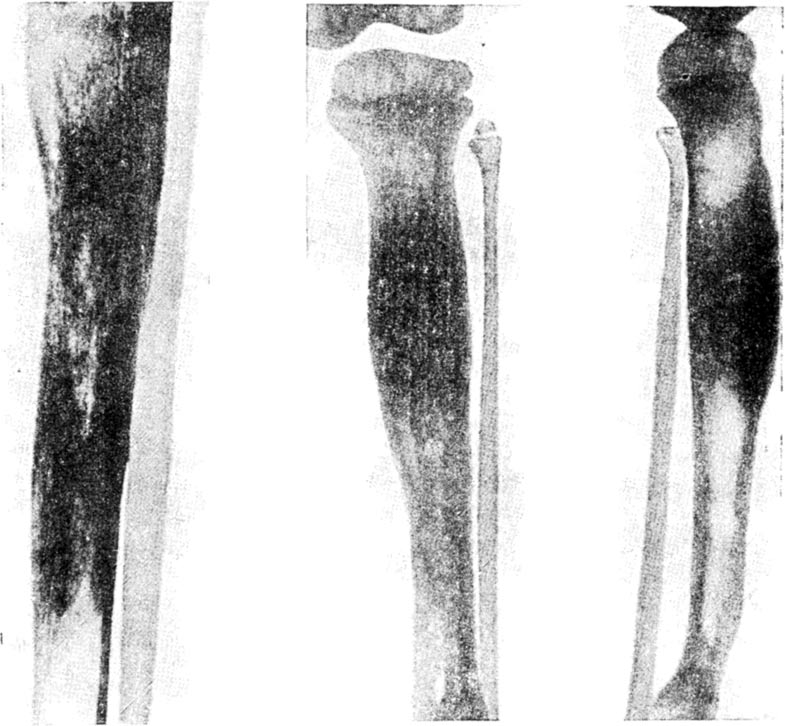 Сокращает сроки лечения, и при широком освоении методики на практике, может быть способом решения проблемы остеомиелита.
Сокращает сроки лечения, и при широком освоении методики на практике, может быть способом решения проблемы остеомиелита.
ПОЛОЖЕНИЯ, ВЫНОСИМЫЕ НА ЗАЩИТУ
Результаты основных положений сформулированных в настоящее работе состоят в том, что весь комплекс терапии и традиционных методов хирургического лечения при изучении ретроспективных групп больных приходилось применять на фоне возникших осложнений. Распространения гнойного воспаления по мягким тканям. Деструкции кости, тяжелого токсикоза и развития сепсиса. Патологических переломов, дефектов кости и
перехода процесса в хроническую стадию.
Эти изменения в организме являются результатом трудностей диагностики и лечения в первую очередь острой и затем хронической стадии. Не решенной до конца проблемы, санации деструктивного костного очага в острой и хронической фазе болезни, раскрытия механизмов патогенеза остеомиелита, как локализованного неспецифического воспалительного процесса. Поэтому улучшение результатов лечения остеомиелита зависит от эффективности хирургического воздействия на очаг, и остается его важнейшей задачей.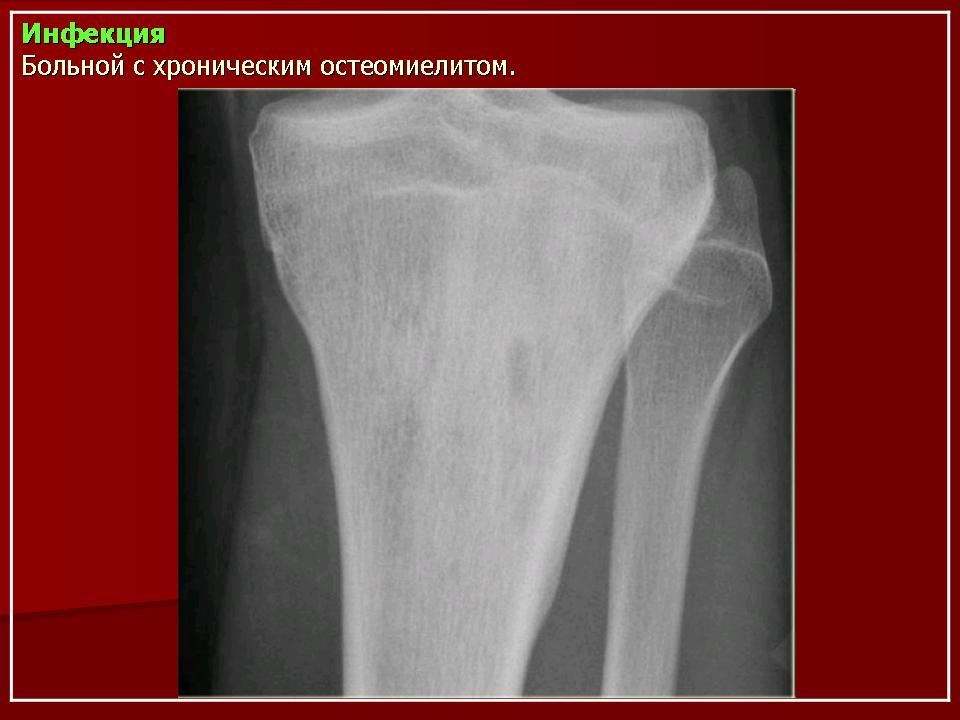
Наличие обширного и длительно существующего гнойного очага в хронической стадии, трудно поддающегося лечению, часто делает такую ситуацию тупиковой. Ликвидировать хронический очаг можно радикальным удалением, что не приемлемо у детей. Выйти из ситуации помогает новый подход и хирургический способ лечения, который позволяет одновременно воздействовать на все основные звенья патогенеза заболевания и в определенной степени контролировать и управлять остеомиелитическим очагом.
Новый патогенетически обоснованный подход в комплексном лечении ГО у детей состоял в повышении роли и эффективности наружной элиминации продуктов воспаления в острой и хронической стадии. В разработке хирургического способа лечения — длительное непрерывное аспирационное дренирование костного гнойного очага (ДНАДКГО), который применялся в III группе детей с остеомиелитом.
ВНЕДРЕНИЕ РЕЗУЛЬТАТОВ ИССЛЕДОВАНИЯ
Способ длительного аспирационного дренирования применяется в хирургическом стационаре Центральной районной больницы г. Серпухова Московской области с января 1985г., клиники детской хирургии МОНИКИ В этот период способ внедрялся и применялся в практической работе
Серпухова Московской области с января 1985г., клиники детской хирургии МОНИКИ В этот период способ внедрялся и применялся в практической работе
хирургических отделений г. Пущино и г. Люберцы Московской области. Методика внедрена в смежных специальностях в зарубежных странах (ближнее зарубежье). Используется в санатории костно-суставного туберкулеза им. А.А.Боброва г. Алупка, Крым, Украина. Методика внедрена в Симферопольском медицинском университете на кафедре хирургической стоматологии и челюстно-лицевой хирургии, на базе железнодорожной больницы Приднепровской УЖД. Методика внедрена в Донецком национальном институте травматологии и ортопедии (Украина) для лечения больных с гематогенным остеомиелитом у взрослых и детей.
По диссертационным исследованиям сделаны сообщения и доклады на 5-и конференциях Москвы и Московской области, 2-х международных конференциях и 5-и Российских конференциях с международным участием. На одном международном симпозиуме, а также на хирургическом обществе Московской области. АПРОБАЦИЯ ДИССЕРТАЦИИ
АПРОБАЦИЯ ДИССЕРТАЦИИ
Апробация материалов диссертации «остеомиелит у детей: этиология, патогенез, клиника, диагностика и лечение» проведена на совместной научной конференции, Кафедры хирургии ФУВ, Кафедры клинико-лабораторной диагностики ФУВ и отделения детской хирургии ГБУЗ МО МОНИКИ им. М.Ф. Владимирского. ПУБЛИКАЦИИ
По материалам диссертации опубликовано 36 научных печатных работ. Из них 5 статей в центральных журналах и 9 в журналах реферируемых ВАК. В том числе получены 2 авторских свидетельства и 5 патентов. На момент апробации диссертации состоялись 4 положительных решения на выдачу патента РФ.
ОБЪЕМ И СТРУКТУРА ДИССЕРТАЦИИ
Диссертация изложена на 302 страницах машинописного текста и состоит из 6 глав. Последняя глава представлена заключением, выводами,
практическими рекомендациями. Список литературы состоит из 701 наименований, в том числе 538-и отечественных и 163-х зарубежных источников. Работа содержит 274 иллюстрации, из них 236 рисунков, 38 таблиц, 13 выписок из историй болезни. МАТЕРИАЛЫ И МЕТОДЫ ИССЛЕДОВАНИЯ
МАТЕРИАЛЫ И МЕТОДЫ ИССЛЕДОВАНИЯ
В настоящую работу вошли клинические наблюдения и исследования 627 детей с острым и хроническим остеомиелитом различной этиологии и локализаций, в возрасте от 6 мес. до 18 лет. Больные лечились и наблюдались в период с 1981 по 2008 гг. Данные клинико-лабораторных тестов подвергались статической обработке в соответствии с общепринятыми рекомендациями (Ойвин А.И., 1960; Бирюкова Л.Р., 1962; Вальвачев Н.И. с соавт, 1989; Рокицкий П.Ф., 1973; Стентон Г., 1999). Расчеты проводились на компьютере Pentium — IV с использованием программ Excel и пакета прикладных программ «Биостатистика». Табличные данные были взяты для оценки стандартного отклонения по выборке с использованием следующей формулы:
Больные остеомиелитом подразделялись на три основные группы (1,11,III.). В I и II группы (565 б-х) вощли дети с острым и хроническим гематогенным остеомиелитом, у которых исследования были направлены на изучение общих закономерностей и особенностей этиологии патогенеза клиники, диагностики остеомиелита, его осложнений, и некоторых местных патоморфологических характеристик остеомиелитического очага.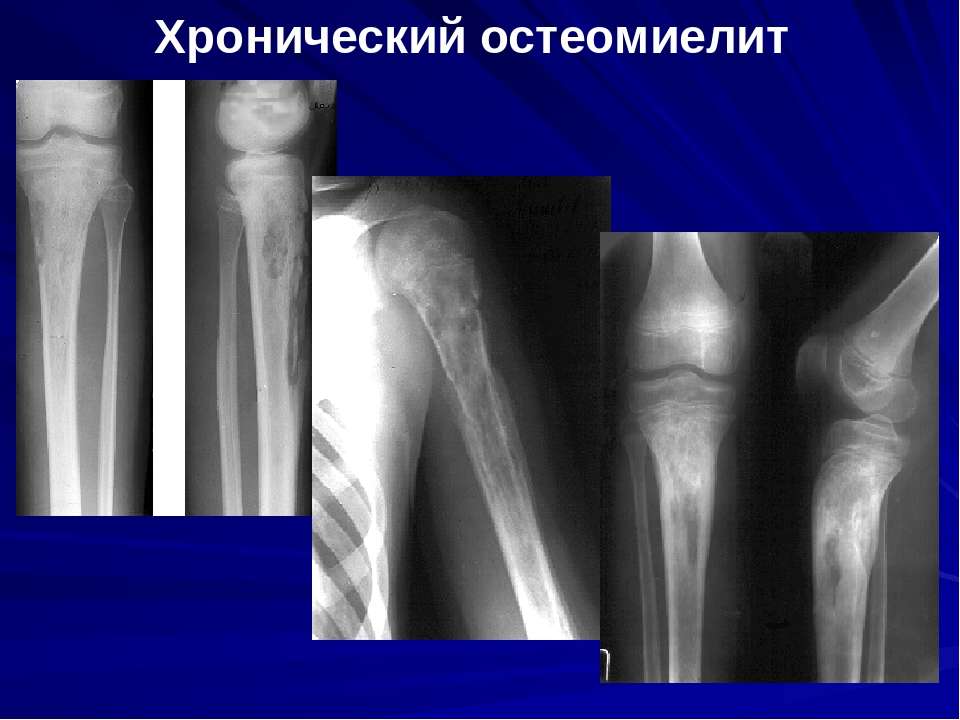 Комплексное лечение патологии у них проводилось с использованием традиционных методов (остеоперфорация — в острой стадии, фистулсеквестрнекрэктомия — в хронической фазе) хирургического лечения костного гнойного очага. В III гр. (62 б-х) вошли дети с острым и хроническим остеомиелитом разной
Комплексное лечение патологии у них проводилось с использованием традиционных методов (остеоперфорация — в острой стадии, фистулсеквестрнекрэктомия — в хронической фазе) хирургического лечения костного гнойного очага. В III гр. (62 б-х) вошли дети с острым и хроническим остеомиелитом разной
этиологии и локализации. У них исследования, в основном, были направлены на изучение местных закономерностей и особенностей этиологии патогенеза, клиники, диагностики остеомиелита, его осложнений, а так же некоторых общих характеристик остеомиелитического процесса. Комплексное лечение патологии у них проводилось с использованием нового способа лечения -длительного непрерывного аспирационного дренирования костного гнойного очага (ДНАДКГО).
Анализ этих данных исследования позволил впоследствии уточнить тактику и взгляд на этиологию, и патогенез остеомиелита у детей, его хирургическое лечение и профилактику осложнений.
Из детей I гр. 100 больных были с острым гематогенным остеомиелитом (ОГО) длинных трубчатых костей.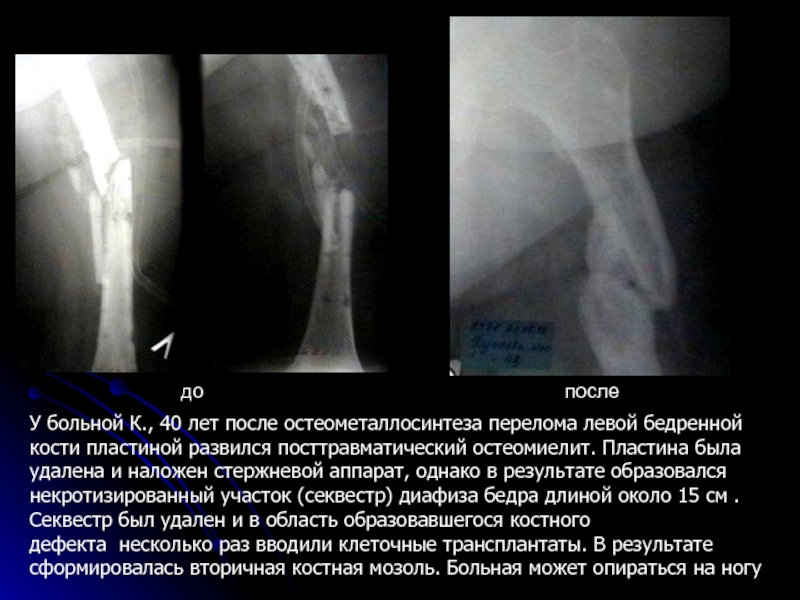 В 72 случаях имела место токсикосептическая форма остеомиелита, а в 28 — септикопиемическая. У 12 больных развилась картина сепсиса.
В 72 случаях имела место токсикосептическая форма остеомиелита, а в 28 — септикопиемическая. У 12 больных развилась картина сепсиса.
II группа детей была с хроническим гематогенным остеомиелитом (465 больных) с различной локализацией остеомиелитического процесса. Мальчиков было 316 (67,96%), девочек 149 (32,04%). Средний возраст детей составил 10,54±2,85 года, в возрасте от 2 до 5лет было 48 (10,2%) детей, 6-10 лет — 143 (30,75%) и 11-15 лет 274 (58,93%). Кости нижней конечности вовлекались в патологический процесс чаще, чем верхней конечности (392 -84,3% против 73 — 15,7%). У данных больных наблюдались 101 случай местных осложнений ХГО: патологический перелом у 45 (44,5%), вывих — у 11 (10,9%), ложный сустав — у 11 (10,9%), анкилозы — у 15 (14,9%), дефекты кости — у 9 (8,9%), укорочение конечности — у 10 (9,9%).
В III группу больных, вошли 62 ребенка с различной стадией и локализацией остеомиелита. Из общего числа больных детей с остеомиелитом (62) девочек было 13 человек (22,0 %), мальчиков 49 (78,0 %) от 1,5 до 18 лет.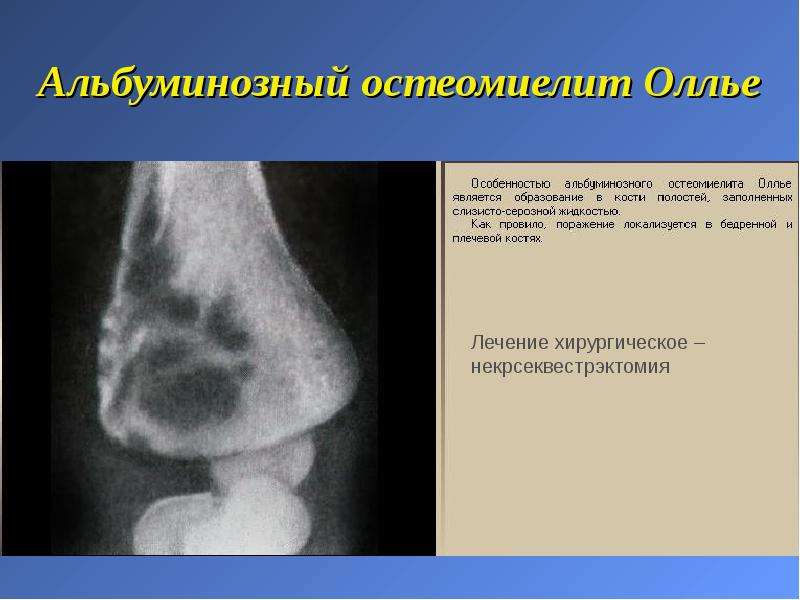 Из них 30 детей (48,3%) пациентов с острой стадией остеомиелита, и 32 (51,7%) человека в хроническом периоде болезни. Таким
Из них 30 детей (48,3%) пациентов с острой стадией остеомиелита, и 32 (51,7%) человека в хроническом периоде болезни. Таким
образом, в основную группу вошли пациенты за период с 1981 года по 2008 год. Мальчиков было (56, 19%), а девочек — (43,81%).
У всех детей использовался комплексный диагностический подход: клинический, рентгенологический, компьютерно-томографический (КТ), ультразвуковой, доплерографический, бактериологический, биохимический, иммунологический, морфологический, цитологический и общелабораторные анализы.
Биохимические исследования включали в себя: уровень активности ферментного-антиоксиданта супероксиддисмутазы (СОД), Содержание водорастворимого антиоксиданта аскорбиновой кислоты (АС), исследование одного из компонентов клеточной мембраны сиаловой кислоты (СК), малонового диальдегида (МДА).
Исследованы некоторые факторы системы антиинфекционной резистентности (АИР) организма: уровень белков острой фазы (БОФ), уровень сывороточных иммуноглобулинов А,М,С, фагоцитарная активность нейтрофилов (ФА) и фагоцитарный индекс (ФИ), комплементарная активность сыворотки крови, количество субпопуляции лимфоцитов СОЗ, СБ56, СЭ20, уровень циркулирующих иммунных комплексов, лейкоцитарного индекса интоксикации (ЛИИ), определение количества МСМ скрининговым методом..jpg)
Морфологические исследования проводились при помощи изучения гистологических срезов костной ткани взятых во время операций.
Бактериологические исследования осуществлялись выделением чистой культуры анаэробов по Цейсслеру. Кроме того проводились специальные бактериологические исследования количественной контаминации тканей при хроническом и остром остеомиелитическом процессе и бактериологический спектр в острой и хронической стадии болезни. Для определения характеристики микробной контаминации тканей раны, исследовались микробиологические посевы нативного материала
гнойных ран и отделяемого экссудата из дренажей. В обязательном порядке, в целях экспресс — диагностики готовились не менее 2 нативных мазков-отпечатков (раневых отпечатков) на предметных стерильных стёклах. Данные, полученные при микроскопии первичного материала, сопоставлялись с результатами изучения морфологии микроорганизмов, выросших в аэробных и в анаэробных условиях. Микроскопию нативного материала проводили в целях оперативного получения информации об интенсивности микробного обсеменения, исследуемых образцов методикой полуколичественного определения микроорганизмов методом калибровочной петли по Gould. Изучали соотношение грамположительных и грамотрицательных микроорганизмов, их форм, выраженности фагоцитоза.
Изучали соотношение грамположительных и грамотрицательных микроорганизмов, их форм, выраженности фагоцитоза.
Из 100 обследованых детей I гр. с ОГО у которых в комплексной терапии остеомиелита применялась остеоперфорация, проведены бактериологические исследования (рис.1). Все дети были с тяжелыми формами заболевания (токсическая форма — 58 больных, септикопиемическая -42).
Этиологическая струтура очага при ОГО у детей (начало болезни)
Отрицательные посевы в аэробных
Psaudomonas aureginosae
° /условиях
6,4% I ¿15%
Streptokoccus
Staph, aureus
Рис.1
В результате микробиологических исследований установлено, что в этиологии ОГО преобладает стафилококк. Так, в начале заболевания из гнойного очага наблюдаемых больных стафилококк был идентифицирован в 81,5% случаев. У 6,4% больных был обнаружен стрептококк, а у 5,2% -синегнойная палочка. В 14% посевов микроорганизмы в аэробных условиях не обнаружены.
В разгар болезни микрофлора, выделенная из гнойных очагов, имела отличие. Удельный вес стафилококка снизился до 56%, в то время как, число посевов с синегнойной палочкой увеличилось до 19,4%. Доля негемолизирующих грамотрицательных бактерий (НГОБ) составила 2,8%. В этот период болезни в гнойном очаге появились грибы рода Candida (2,8%), более, чем в 2 раза увеличилось число отрицательных посевов (33%).
Этиологическая структура очага при ОГО у детей (выздоровление)
Отрицательные посевы в аэробных условиях
Рис.2
К концу заболевания отмечается дальнейшее снижение количества посевов, в которых обнаружен стафилококк (29%) и рост в посевах синегнойной палочки (35%). Увеличился удельный вес других грамотрицательных микробов (НГОБ-6%, протей-6%). Число отрицательных посевов составило 35%. Следует отметить, что в процессе заболевания наблюдается рост количества микробных ассоциаций. Так, если в начале болезни их удельный вес составлял 6,9%, в разгар — 24,7%.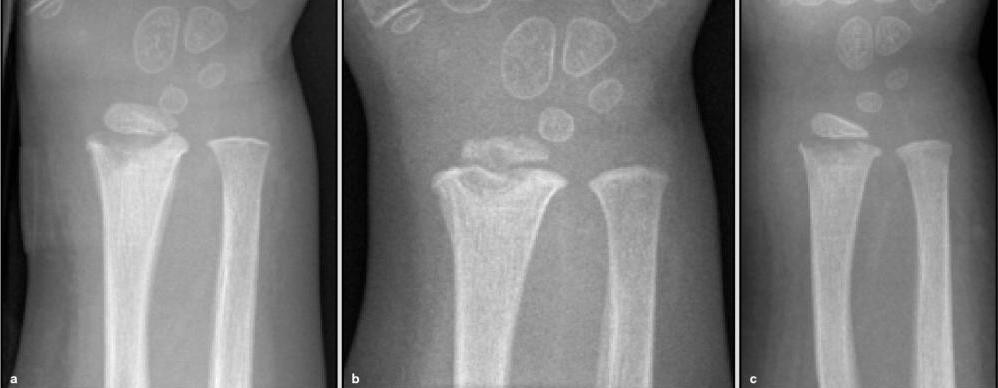 то к концу заболевания был — 52,1% (рис. 3).
то к концу заболевания был — 52,1% (рис. 3).
Таким образом, лидирующим этиологическим фактором у детей с острым остеомиелитом (ОО) является стафилококк. В дальнейшем отмечается рост количества грамотрицательных бактерий, отрицательных посевов и в редких случаях грибов рода Candida, и ассоциаций, достигающего максимальных значений к концу болезни до 5%.
Для изучения особенностей воспалительного процесса у детей с остеомиелитом при переходе его хроническую стадию подвергнута анализу I
группа больных. Из них дети с ОГО, перешедших в хроническую форму 30 больных, (основная группа, 1гр.). Дети с ОГО, у которых отмечалось благоприятное течение, без перехода воспалительного процесса в хроническую стадию (36 детей, группа контроля 2гр.).
У детей 1гр. частота высеваемости стафилококка из гнойного очага в разгар болезни и к периоду клинической ремиссии значительно превосходит таковую у больных 2 гр. Идентификация синегнойной палочки в разгар болезни у детей основной группы, больше по сравнению с группой сравнения (соответственно: 59,7% и 9,5%). К концу болезни это различие становится еще существенней (соответственно: 38,9% и 3,3%). Число отрицательных посевов у детей 2 гр. намного выше (соответственно: 82,3% и 13,2%).
К концу болезни это различие становится еще существенней (соответственно: 38,9% и 3,3%). Число отрицательных посевов у детей 2 гр. намного выше (соответственно: 82,3% и 13,2%).
Следовательно, у детей с переходом остеомиелитического процесса в хроническую стадию (1 гр.) отмечается замедленная элиминация стафилококка и синегнойной палочки из гнойного очага.
В II группе больных с ХГО в стадии обострения, у которых в комплексе лечения применялась, фистулсеквестрнекрэктомия проведены исследования посевов из очага на анаэробную флору. Положительные результаты наблюдались в 67,5% случаев. Среди них bacteroides был идентифицирован в 44,4%, prevotella 25,9%, fusobacterium 22,2% и porghyromonas в 7,4% случаев (рис. 3).
Рис.3. Идентификация анаэробной флоры у детей с ХГО при обострении
Следовательно, длительно существующий воспалительный процесс понижает резистентность костной ткани, и наряду с патогенной и условно-патогенной микрофлорой сопровождается значительной контаминацией кости неклостридиальными анаэробными микроорганизмами.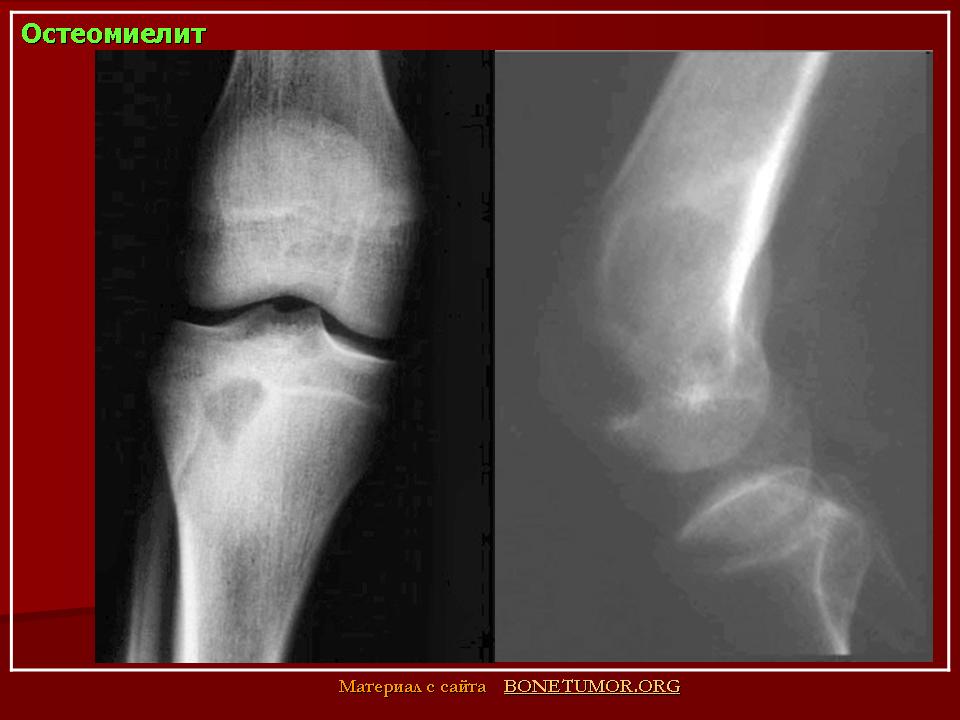 Это свидетельствуют о недостаточной их элиминации и в целом санации и деконтаминации гнойного очага.
Это свидетельствуют о недостаточной их элиминации и в целом санации и деконтаминации гнойного очага.
Одной из задач настоящей работы было изучение особенностей воспалительного процесса у детей I группы с остеомиелитом при переходе его хроническую стадию в сравнении.
При анализе полученных данных выявлено, что переход остеомиелитического процесса в хроническую стадию отмечается относительный рост количества лейкоцитов (соответственно: 6,4±0,3 и 8,4±0,2х109/л, 1=4,0), количества палочкоядерных нейтрофилов, снижение процентного содержания базофилов, эозинофилов. Прирост эозинофилов в процессе хронизации остеомиелита. Содержание лимфоцитов в периферической крови у детей 1 гр. достоверно ниже в разгар болезни и при ремиссии, значительное повышение процентного содержания моноцитов, СОЭ. Показатели ЩФ превышают таковые у больных 2 гр., повышение уровней 1§0,1§М, 1§А и ЦИК к периоду ремиссии (рис. 4,5,6). с
2,5
|д А
Хронизация [ Ремиссия [
Ремиссия [
1 2 3 периоды болезни
1 2 3 Периоды болезней
1 2 3 периоды болезни
Рис.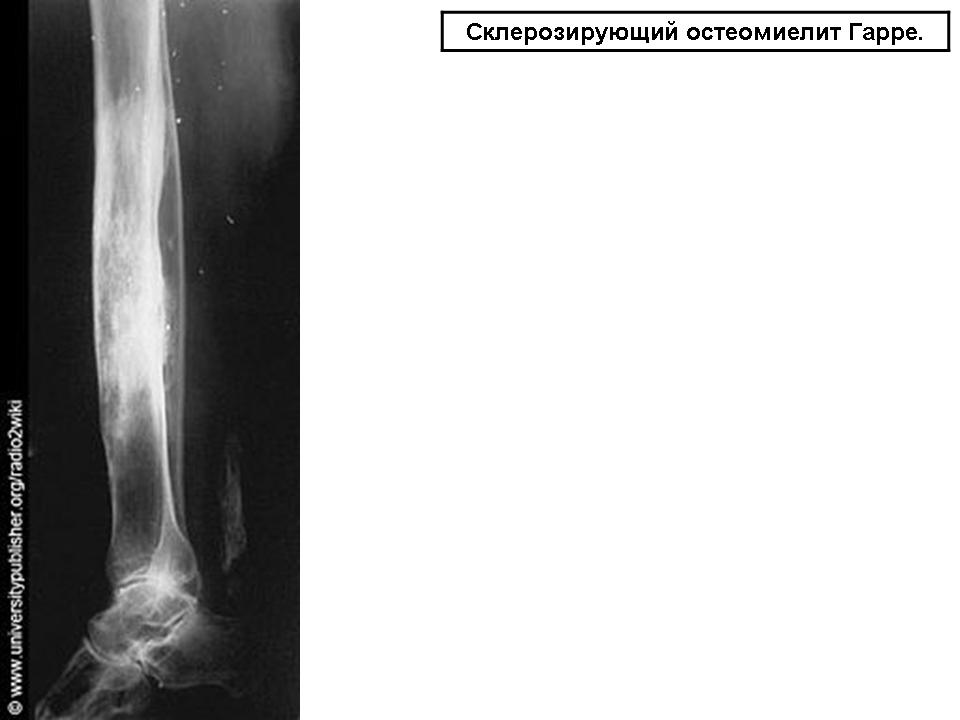 М и характерного для иммунного ответа при выздоровлении, практически не происходит при переходе процесса в хроническую стадию. В динамике клеточного иммунитета отмечено снижение числа СЭЗ в середине болезни в 1 гр. больных, сохраняющееся и при ремиссии, и С056. Количество СЭ20, наоборот, достоверно выше у детей 1 гр. во второй половине заболевания. У больных с переходом остеомиелита в хроническую форму (1 гр.) обнаружено значительное угнетение фагоцитарной активности нейтрофилов (ФА) и относительно низкий фагоцитарный индекс (ФИ) на протяжении всего заболевания, без тенденции к нормализации (рис. 7,8,9,10).
М и характерного для иммунного ответа при выздоровлении, практически не происходит при переходе процесса в хроническую стадию. В динамике клеточного иммунитета отмечено снижение числа СЭЗ в середине болезни в 1 гр. больных, сохраняющееся и при ремиссии, и С056. Количество СЭ20, наоборот, достоверно выше у детей 1 гр. во второй половине заболевания. У больных с переходом остеомиелита в хроническую форму (1 гр.) обнаружено значительное угнетение фагоцитарной активности нейтрофилов (ФА) и относительно низкий фагоцитарный индекс (ФИ) на протяжении всего заболевания, без тенденции к нормализации (рис. 7,8,9,10).
соз
СЭ56
50 40 30 20 -10
45 40 35 30 25 20 15 10 5 0
% 20
14 12 10
Периоды болезни
Рис. 9
%
50 40 30 20 10 0
Периоды болезни
Рис. 8
Фагоцитарная активность(ФА)
Периоды болезни
Рис. 10
Рис. 8,9,10,11. Динамика лимфоцитов СБ, лимфоцитов СЭ20, и СБ56 ( активных) и ФА у детей с ОГО при переходе в хроническую форму.
Уровень гемолитического комплемента (СН50) у детей 1 гр. также достоверно ниже, чем в группе сравнения, наблюдаются низкие уровни АТ к стафилококковому а-токсину. Обратная тенденция прослеживается при исследовании уровня лизоцима в крови детей с ОГО.
Полученные результаты указывают на дисбаланс в иммунной системе детей с остеомиелитом. В разгар болезни, в хронической стадии и в состоянии ремиссии относительно активизируется В-система иммунитета. Увеличивается количество С020 и иммуноглобулины всех классов. Происходит угнетения клеточного звена иммунитета. Снижается количество СЭЗ и СЭ56 клеток.
Важнейшим патогенетическим фактором в начальном периоде перехода остеомиелита в хроническую фазу является снижение активности нейтрофильного фагоцитоза. Это может свидетельствовать, что фагоцитоз в первую очередь угнетен в очаге воспаления, что не позволяет добиться его полноценной санации и регенерации поврежденных костных структур.
Довольно постоянными закономерностями перехода воспалительного процесса в хроническую фазу, является падение концентрации лизоцима в сыворотке крови.
Все эти факторы указывают на дисбаланс в иммунной системе ребенка с гематогенным остеомиелитом, являющегося следствием недостаточной внутренней и наружной элиминации микробного фактора и продуктов воспаления из очага и их резорбции в кровь. Это сопровождается расстройством регенераторных процессов в кости нарушением экссудативных процессов и пролиферативной фазы воспаления.
У больных детей II гр. с хроническим гематогенным остеомиелитом отмечается достоверное изменение процессов ПОЛ и антиоксидантной системы защиты. МДА увеличивается в 2,6 раза по сравнению с контролем
(0,89±0,09 и 0,38±0,03 мкмоль/л, соответственно), активность ферментного антиоксиданта — супероксиддисмутазы (СОД) в сыворотке крови снижается в 1,7 раза (8,04±1,2 и 14,25±0,013 ед./мл, соответственно), активность компонента клеточной мембраны сиаловой кислоты (СК) в сыворотке крови увеличивается в 1,8 раза по сравнению с контролем. Содержание водорастворимого антиоксиданта аскорбиновой кислоты (АК) снижается также в 1,7 раза (0,72±0,15 и 1,3±0,06 мг%, соответственно). затяжных (хронических) форм не наблюдалось.
затяжных (хронических) форм не наблюдалось.
Это указывает, что, чем ниже уровень и длительность гуморального ответа, тем слабее экссудативная фаза воспаления и воспалительного ответа на инфекцию и возможности санации тканей от патогенных микробов.
Гуморальное звено иммунитета является общим фактором первой фазы экссудативной воспалительной реакции организма, следующей за альтерацией, является компенсаторным и защитным механизмом, сопровождающимся плазморреей в очаге содержащей в себе гуморальные факторы защиты, за которым следует пролиферация и фагоцитоз. Они направлены на санацию и элиминацию продуктов воспаления из очага. Угнетение этого механизма, а так же недостаточный наружный санирующий эффект традиционных хирургических методов лечения, является одним из факторов перехода воспаления в хроническую стадию. Это впоследствии поддерживает угнетение регенерации тканей в пролиферативной фазе воспаления. Задача хирургического лечения состоит в максимальном восстановлении механизмов наружной санации и деконтаминации очага остеомиелита и адаптации его к общей терапии.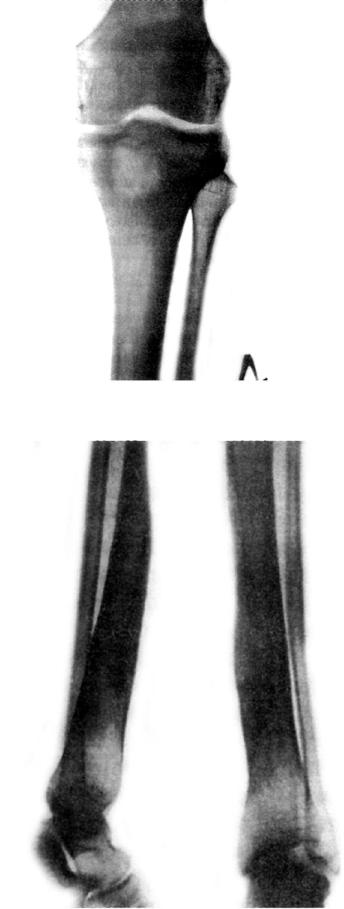
При исследовании общих белковых фракций крови детей установлено, что ОГО у детей протекает с диспротеинемией, сопровождающейся выраженным снижением количества альбумина, повышением глобулиновых фракций, снижением альбумино-глобулинового коэффициента, которые сохраняются до периода клинического благополучия.
У детей в хронической стадии процесса содержание данных фракций оставалось достоверно высоким на протяжении всего периода заболевания, при этом содержание у — глобулинов увеличивалось к периоду клинического выздоровления (табл. 1).
Следовательно, длительно протекающий остеомиелитический процесс сопровождается дисбалансом белковых фракций крови, что может быть вызвано токсикозом в обеих фазах заболевания.
Уровень общего белка, альбумина и А/Г коэффициента в динамике заболевания у больных с ОГО ( М ± m ).
Таблица 1
Группы Период Общ. белок г/л Альбумин А/Г Коэф.
% г/л
(п = 62) I 70,20±1,87# 42,28±1,55*# 29,92±1,02*# 0,64±0,02* #
11 74,08±1,74 43,84±1,10*# 31,27±0,89*# 0,71±0,04»#
III 76,00±1,85 45,25±1,17*# 35,09±0,88*# 0,84±0,04* #
IV 76,29±1,32 54,76±1,64# 41,64±0,88# 1,13±0,05#
2 (п-7) I 63,85±2,08»# 38,76±0,94*# 25,31±0,89*# 0,61±0,04*
II 70,00±2,66 36,64±1,37*# 24,91±1,21’# 0,54±0,03* #
III 72,42±3,42 37,55±1,41*# 26,24±1,26*# 0,59±0,03* #
IV 74,14±2,62 41,54±1,32*# 31,82±0,99*# 0,64±0,03* #
Контроль (п = 10) 74Д0±1,64 57,12±1Д6 43,26±0,65 1,15±0,04
I- острый период; П-подострый период; Ш-период клинического выздоровления; IV-через 1 месяц после выписки из стационара.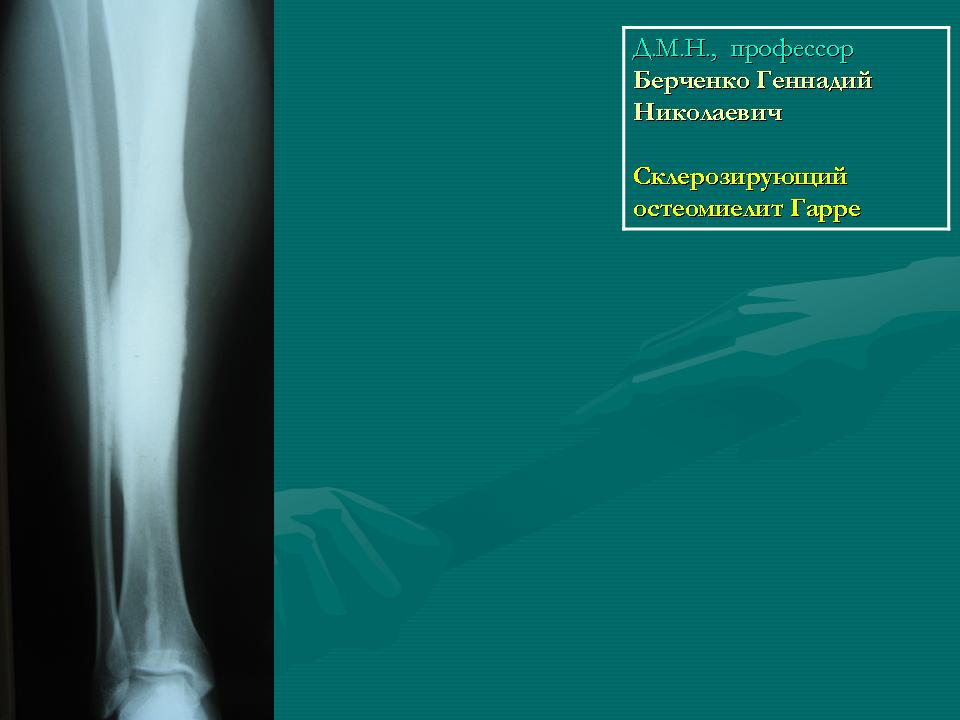 *- достоверность различий с контролем — р <0,001; и — достоверность различий между группами — р < 0,001.
*- достоверность различий с контролем — р <0,001; и — достоверность различий между группами — р < 0,001.
Патогенез ГО у детей сопровождается выраженными изменениями и закономерной динамикой содержания белков острой фазы (БОФ) (СРБ, а-1-ИП, а-1-КГП) в сыворотке крови. Для благоприятного исхода ОГО (1 гр.) характерна тенденция к постепенному снижению содержания данных белков к периоду клинического благополучия.
У детей в хронической стадии процесса (2 гр.), несмотря на тенденцию к снижению, содержание БОФ в сыворотке крови во все периоды заболевания относительно превышает таковое в группе сравнения. Контрольное обследование через 1 месяц, после выписки больных из стационара, указывало на продолжающуюся активность воспалительного процесса, несмотря на клиническое благополучие, рис. 12,13.
Динамика содержания БОФ в 2-х группах больных с ОГО
Динамика БОФ у детей с ОГО при благоприятном течении
з
2,5 2
■5 1.5
0,5
о
Динамика С-РБ у больных ОГО при благоприятном течении и при обострении и суперинфекции
острый период подострый суперинфекция( обострение)
Рис. 12
12
Таким образом, одной из особенностей и закономерностей патогенеза ГО у детей является реакция организма ребенка с увеличением уровня БОФ. Наиболее информативными показателями продолжающейся активности воспалительного процесса в костной ткани являются БОФ (С-РБ, а-1-ИП, а-1-КГП). Из них самый показательный и специфичный параметр С-РБ, который при наличии клинической картины можно расценивать как маркер ГО у детей.
Неудовлетворительные результаты лечения проявляются в продолжающейся деструкции костной ткани и генерализации гнойно-деструктивного процесса на модели ОГО у детей и переход его в сепсис в 12%. Генерализация воспалительного процесса у детей с ОГО сопровождается еще более глубокими нарушениями системы иммунобиологической защиты (угнетение гуморального и клеточного иммунитета).
Особенностями и закономерностями нарушений являются: 1. Резкое
острый перид подострый,выздоровление
Рис. 1 1
г
снижение абсолютного и процентного числа лимфоцитов в разгар болезни ( <15-17% и <1,5-1,7×10%!).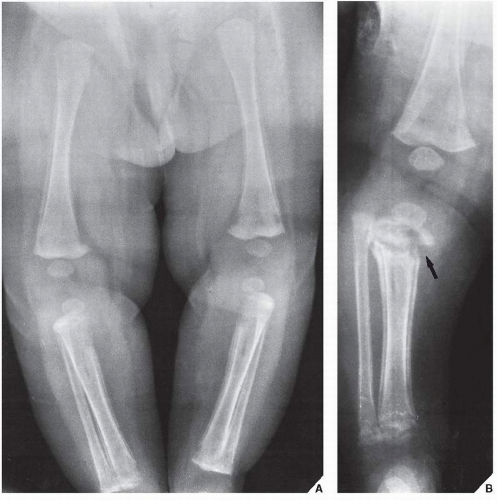 2. Тенденция к снижению лейкоцитоза в остром периоде заболевания вместе с уменьшением количества палочкоядерных нейтрофилов. 3. Постоянная, трудно поддающаяся коррекции анемия. 4. Повышение СОЭ в середине болезни или отсутствие тенденции к ее нормализации и моноцитоз. 5. Дефицит практически всех факторов системы АИР организма. 6. Резкое снижение количества СОЗ в процессе заболевания. 7. Чрезвычайно низкие показатели фагоцитарной активности нейтрофилов (<10%) и фагоцитарного индекса (<2,4) в острый период заболевания. 8. Продолжающаяся деструкция и формирование хронического гнойного очага.
2. Тенденция к снижению лейкоцитоза в остром периоде заболевания вместе с уменьшением количества палочкоядерных нейтрофилов. 3. Постоянная, трудно поддающаяся коррекции анемия. 4. Повышение СОЭ в середине болезни или отсутствие тенденции к ее нормализации и моноцитоз. 5. Дефицит практически всех факторов системы АИР организма. 6. Резкое снижение количества СОЗ в процессе заболевания. 7. Чрезвычайно низкие показатели фагоцитарной активности нейтрофилов (<10%) и фагоцитарного индекса (<2,4) в острый период заболевания. 8. Продолжающаяся деструкция и формирование хронического гнойного очага.
Например, в показателях гуморального иммунитета отмечаются низкие уровни у детей 1 гр. в начале заболевания и в его разгар. Их значения более, чем в 2 раза ниже по сравнению с больными 2 гр.. Но к концу болезни, наоборот, уровни у детей 1 гр. достоверно превосходили этот показатель в группе сравнения (рис. 13,14).
Динамика уровней 1дв при ОГО удетей при переходе в сепсис
20 18
ОГО
16 14 12
10 8 Сепсис
6 4 2 0
1 2 Периоды болезни 3
Динамика уровней |дМ при ОГО у детей при переходе в сепсис
1,4 1,2 1 0,8 0,6 0,4 0,2
Рис. А одновременно с угнетением антителогенеза к стафилококковому а-токсину (рис.15,16).
А одновременно с угнетением антителогенеза к стафилококковому а-токсину (рис.15,16).
Динамика уровней 1дА у детей при переходе ОГО в сепсис
Разгар болезни Выздоровление
< Динамика синтеза антител к ь стафилококковому альфа-токсину
Рис. 15 Рис. 16
В наибольшей степени выражено угнетение в Т-системе иммунитета. С самого начала заболевания до периода клинического выздоровления имеет место значительный дефицит С1)3. Количество СОЗ у этих больных, также, относительно ниже, чем у детей 2 гр. Снижение числа СОЗ отмечается в обеих группах в течение всей болезни. Но у детей с сепсисом дефицит СОЗ выражен в большей степени, особенно в острый период заболевания.
На неблагоприятное течение остеомиелита у детей и его исходы оказывали и диагностические и лечебно-тактические ошибки. В стадии хронических воспалительных изменений в кости ранний диагноз, как правило не вызывает сомнений. Другая ситуация складывается в остром периоде патологии, когда необходимо проводить дифференциальный диагноз с рядом состояний и заболеваний ребенка, при которых присутствуют боли в сегменте разной интенсивности. .Л£55881 Позднее поступление спустя 72ч
.Л£55881 Позднее поступление спустя 72ч
О 10 20 30 40 50 60 70
Всего больных подвергнутых анализу
Рис.17
Это отразилось в дальнейшем лечебно-тактических ошибках. У 48,4% больного оперативное лечение (остеоперфорация и вскрытие флегмоны) в хирургическом стационаре больницы было произведено более чем через 12 часов после постановки правильного диагноза. У 52,77% детей проведены повторные операции.
Исследования показали, что ранняя аппаратная диагностика острой стадии гематогенного остеомиелита не имеет специфичности и поэтому затруднена. Но при внимательном отношении к клинике и привлечению всех доступных современных методов диагностики поставить своевременный диагноз и провести раннюю операцию в течение суток возможно. Недоучет этих моментов в 50% случаях обуславливает ошибки, способствующие осложнениям.
В последующем многие дефекты лечения были устранены, но дальнейшая терапия проходила на фоне наступивших осложнений, которые потребовали значительных усилий, и применения дополнительных интенсивных мероприятий, в т.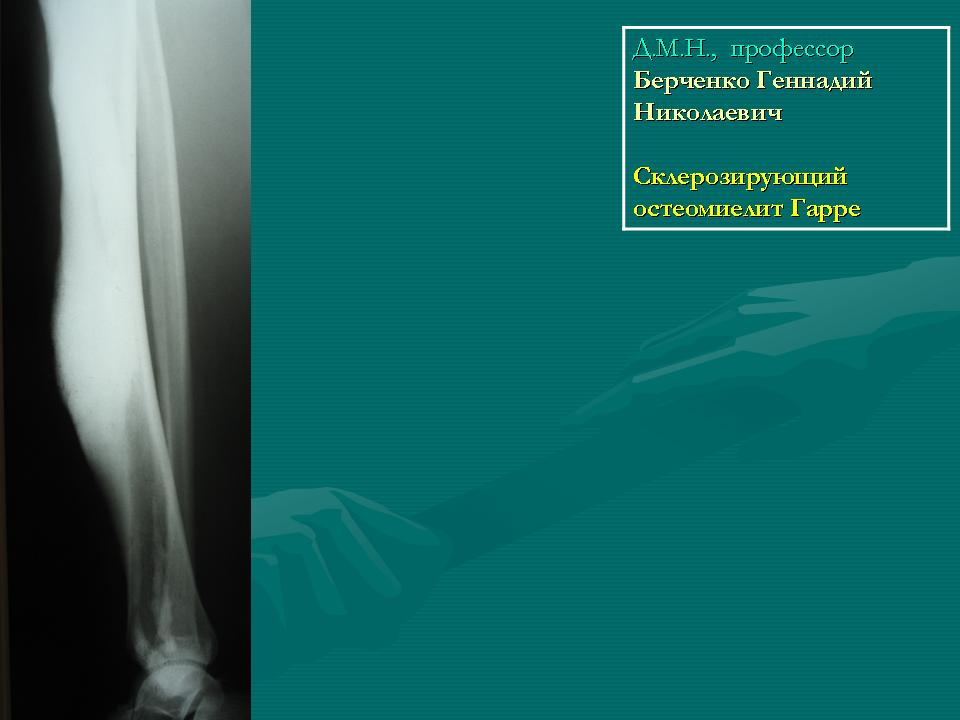 ч. длительных курсов антибактериальной
ч. длительных курсов антибактериальной
терапии. Иммунотерапии Т-активином, применения ГБО, дискретного плазмафереза, антиоксидангной терапии, местного применения гелий-неонового лазера. Действие их на организм ребенка, в условиях слабо-санированного очага, было иногда противоречивым и патогенетически не всегда обоснованным, которое прослеживалось в группах сравнения.
Например, не отмечено достоверного различия в процентном и абсолютном количествах сегментоядерных нейтрофилов при иммунотерапии Т-активином. ГБО практически не влияет на общее количество лейкоцитов в периферической крови и на число сегментоядерных нейтрофилов. После курса ГБО количество С03 оставалось достоверно выше, чем в группе сравнения (соответственно: 46,6±3,2 и 35,6±2,6%, 1=2,7). Вместе с тем, не отмечено стимулирующее влияние ГБО на количество С[320. Динамика I тела показывает, что на 3-5 сутки на фоне ДПА имеет место умеренный подъем I тела. Активность процессов образования промежуточных продуктов ПОЛ приближается к норме только чрез 1 месяц интенсивной терапии. Не обнаружено какого-либо действия ЛТ на динамику эозинофилов в периферической крови, отмечен резкий подъем базофилов крови после первого сеанса (соответственно: 0,7±0,1% и 0,3±0,05%, 1=4,0) и др. Отсутствует существенное влияние ГНЛ на синтез 1§0.
Не обнаружено какого-либо действия ЛТ на динамику эозинофилов в периферической крови, отмечен резкий подъем базофилов крови после первого сеанса (соответственно: 0,7±0,1% и 0,3±0,05%, 1=4,0) и др. Отсутствует существенное влияние ГНЛ на синтез 1§0.
Формирование хронического очага остеомиелита на фоне ошибок диагностики и невсегда успешного комплексного лечения поставило задачу исследования и изучение морфофункциональной струпуры костной ткани при ХГО в стадии ремиссии и обострения. Установлено, что при ХГО у детей наблюдаются различные по своей выраженности морфофункциональные изменения костной ткани, требующих длительного многолетнего лечения.
Установлено, что при ХГО у детей наблюдаются различные по своей выраженности морфофункциональные изменения костной ткани (рис. 18,19).
Рис.19. Костный мозг с воспалительными элементами. Г-Э. Ув. хЮО. Рис. 20. Воспалительный инфильтрат. Г-Э. Ув. хЮО.
После ликвидации обострения хронического гематогенного остеомиелита, в стадии ремиссии болезни у больных 2. -группы наблюдалась, выраженная продуктивная реакция с образованием полей грануляционной ткани (рис. 20,21).
-группы наблюдалась, выраженная продуктивная реакция с образованием полей грануляционной ткани (рис. 20,21).
Рис. 20. Исчезновение воспалительных элементов и замещение
фиброцитами. Г-Э. Ув. х400. Рис. 21. Появление остеокластов среди фиброзной ткани. Г-Э. У в. х400
Эти изменения в организме являются результатом трудностей диагностики и лечения. Не решенной до конца проблемы, санации деструктивного костного очага в острой и хронической стадии, раскрытия механизмов патогенеза остеомиелита. Отсутствие завершенности восстановительных процессов в гнойной кости. Наличие обширного и длительно существующего гнойного очага в хронической стадии, часто делает такую ситуацию неразрешимой. Ликвидировать хронический очаг
можно радикальным удалением, что не приемлемо особенно у детей. Поэтому улучшение результатов лечения остеомиелита зависит от эффективности хирургического воздействия на очаг, и остается его важнейшей задачей. Решить ее позволяет новый подход.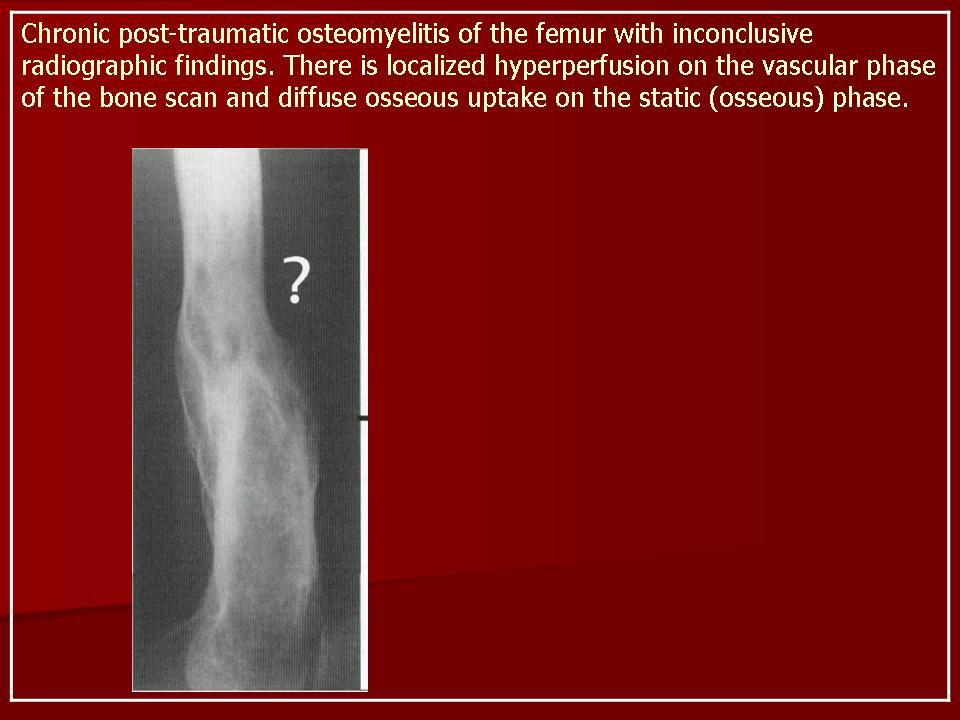
Патогенетически обоснованный новый подход в комплексном лечении ГО у детей состоял в повышении роли и эффективности наружной элиминации продуктов воспаления в острой и хронической стадии, за счет разработки нового хирургического способа лечения — длительное аспирационное дренирование костного гнойного очага (ДНАДКГО), который применялся в III группе детей с остеомиелитом.
У детей с остеомиелитом (62 человека), выделенных в III группу, проводилась комплексная клиническая оценки состояния и контроль над ходом лечения. Большинство детей поступало с осложненным, или затяжным течением заболевания и отклонениями в показателях характеризующих активность вопалительного процесса и токсикоза.
На фоне использования нового способа отмечен постепенный рост гемоглобина к 30 дню заболевания (рис. 22). Гематокрит, так же существенно менялся в положительную сторону. Температурная реакция нормализовалась практически после 7-го дня от начала лечения, а также лейкоцитарная формула периферической крови (лейкоциты 8,6±1,35; 7,15±1,25; S откл. -1,05) СОЭ имела особенности при лечении ДНАДКГО (47,3±6,4; 13,2±1,7). После операции она повышалась и держалась на повышенном уровне достаточно длительный срок. Это связано, с тем, что методика повышает экссудацию в очаге, что обеспечивает усиленную миграцию нейгрофилов в очаг воспаления.
-1,05) СОЭ имела особенности при лечении ДНАДКГО (47,3±6,4; 13,2±1,7). После операции она повышалась и держалась на повышенном уровне достаточно длительный срок. Это связано, с тем, что методика повышает экссудацию в очаге, что обеспечивает усиленную миграцию нейгрофилов в очаг воспаления.
Динамика количества гемоглобина у детей Шгр. с остеомиелитам при лечении ДНАДКГО
1 140
120 100
Периоды лечения 1=1-2дн. 2=5-7ДН. 3=10-15дн. 4=20-30дн 5=30дн.>
Рис.22
По мере санации гнойной кости СОЭ нормализуется. Лейкоцитоз и повышенное количество палочкоядерных нейтрофилов уменьшалось по мере стихания или ликвидации острого воспалительного процесса (12,3±2,6; 2,5±0,5). Реакция нейтрофилов имела прямую зависимость от степени тяжести больного и активности воспаления. Исчезал процентный и абсолютный дефицит лимфоцитов крови (21,2±5,2; 1,6±0,3 и 43,1±5,1; 4,0±0,3). Постепенно нормализовалось количество моноцитов (5,3±1,2; 0,7±0,21 и 8,5±1,8; 1,9±0,5).
Эозинофилы в процессе лечения имели тенденцию сначала к росту, и затем к снижению. Эозинофилия связана с процессом стимуляции фагоцитоза в очаге воспаления через антигенстимуриванные лимфоциты, а следовательно подтверждало стимулирующее влияние ДНАДКГО на репаративный остеогенез.
Динамика показателей крови у больных III гр.
3« детей с ОО в процессе лечения ДНАДКГО
25
20
1,2-начало 3,4- процесс 5.6-вызд.
Рис.23
В хронической стадии преобладают реорганизационные процессы в кости, но как уже показано они не имеют завершенности. Следует отметить,
что показатель СОЭ был в прямой коррелятивной зависимости с динамикой уровня эозинофильных гранулоцитов в обеих стадиях. Их рост, в процессе лечения, не являлся отрицательным фактором и оказывал позитивное воздействие на общее состояние и процессы регенерации в очаге.
В хронической стадии остеомиелита у детей повышенный уровень палочкоядерных нейтрофилов при обострении в начале болезни постепенно снижался.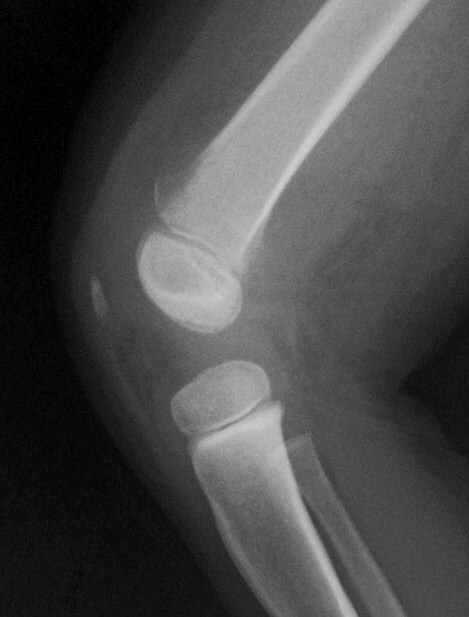 Отмечалось медленное повышение уровня лимфоцитов и моноцитов в пределах референтных значений, что в целом соответствует тенденции в хронической стадии. Быстрая тенденция к росту уровня с\я нейтрофилов.
Отмечалось медленное повышение уровня лимфоцитов и моноцитов в пределах референтных значений, что в целом соответствует тенденции в хронической стадии. Быстрая тенденция к росту уровня с\я нейтрофилов.
Это свидетельствует о стимулирующем, балансирующем и модулирующем санационном эффекте методики, что позволяет сравнить ее с ГБО. Однако ГБО не обладает свойством наружной санации и не уменьшает, а в начальном периоде увеличивает резорбцию из очага.
Доказательством могут служить и некоторые другие общие показатели неспецифического воспаления в органах и тканях: тимоловая проба, АЧВТ %, протромбин %, щелочная фосфатаза, биллирубин, АЛТ, ACT. Динамика уровня щелочной фосфатазы не отличались в начале и в конце лечения и были в пределах референтных значений, что связано с отсутствием основного осложнения — деструкции кости. В хронической стадии в начале лечения они были высокими за счет выраженных деструктивных изменений. Не было случаев угнетения факторов АИР. Динамика количества тромбоцитов у больных III группы имела выраженную позитивную направленность.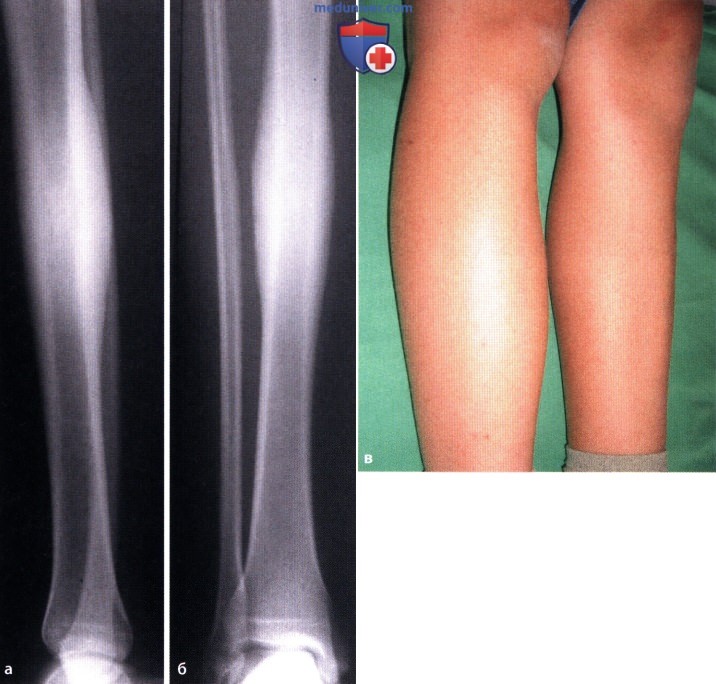 при ОГО в периоды обострения при ХГО. Их динамика в сторону увеличения, видимо не следует расценивать, как отрицательную тенденция в течении остеомиелита, а лишь о напряженности фагоцитарной реакции и опсонизирующим эффектом. Раньше всех нормализовались в остром периоде остеомиелита показатели иммуноглобулинов, а наиболее стойким маркером воспалительного процесса являлся С-РБ. С-РБ нормализовался примерно в течение 1,5-2-х месяцев после прекращения дренирования.
при ОГО в периоды обострения при ХГО. Их динамика в сторону увеличения, видимо не следует расценивать, как отрицательную тенденция в течении остеомиелита, а лишь о напряженности фагоцитарной реакции и опсонизирующим эффектом. Раньше всех нормализовались в остром периоде остеомиелита показатели иммуноглобулинов, а наиболее стойким маркером воспалительного процесса являлся С-РБ. С-РБ нормализовался примерно в течение 1,5-2-х месяцев после прекращения дренирования.
Были отмечены предшествующие общие заболевания, которые могли быть источником лимфогематогенного заноса инфекции в кость. Почти в 71% случаев у больных детей имел место предполагаемый источник инфицирования кости, в 39% он не был установлен. На первом месте по частоте встречаемости (30,6%), была механическая закрытая травма сегмента.
Проведен анализ характера хирургических методов лечения различных форм остеомиелита, которые предшествовали лечению новым способом. Ими были: простая инцизионно-дренажная операция (ИДО).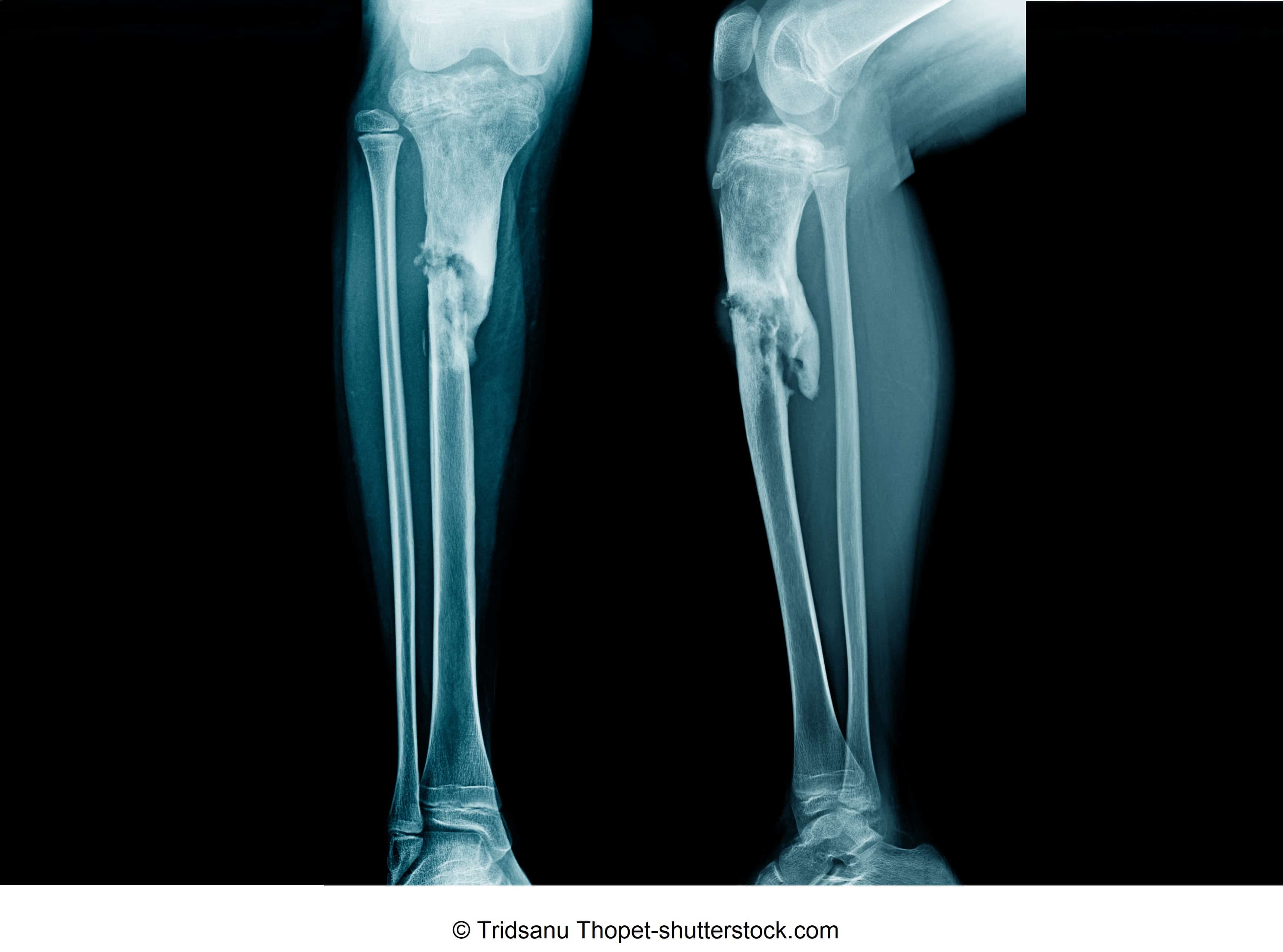 Остеоперфорация (ОП) в острой стадии остеомиелита. Приточно-аспирационное дренирование (ПАД) и неоднократная операция фистулсеквестрнекрэктомия (ФСНЭ) в хронической стадии с указанными вариантами наружного дренажа в среднем 2-3 у каждого больного.
Остеоперфорация (ОП) в острой стадии остеомиелита. Приточно-аспирационное дренирование (ПАД) и неоднократная операция фистулсеквестрнекрэктомия (ФСНЭ) в хронической стадии с указанными вариантами наружного дренажа в среднем 2-3 у каждого больного.
Для определения характеристики микробной контаминации тканей очага, исследовались микробиологические посевы нативного материала из ран мягких тканей и отделяемого экссудата из костного очага. Отмечено, что микробиологическая структура первичного и особенно вторичного (45 больных) гнойного очага при хроническом остеомиелите значительно отличается. В посевах первичного материала из костномозгового канала во время операции у больных детей (17) с острым остеомиелитом в 64,62±2,1 %
случаях, высевался стафилококк. Наличие Золотистого стафилококка в хроническом очаге остеомиелита при оперативных вмешательствах присутствует только в 13 (28,8%) случаях. В 52,45% случаев микрофлора гнойного очага была устойчива к исследуемым антибиотикам. Устойчивая микрофлора в очаге остеомиелита практически в 70% случаев (32 из 45) принадлежала больным с хроническим остеомиелитом.
Устойчивая микрофлора в очаге остеомиелита практически в 70% случаев (32 из 45) принадлежала больным с хроническим остеомиелитом.
В некоторых ситуациях тяжелое состояние ребенка не позволяло провести повторную, радикальную операцию. Но при наличии функционирующего свища, он использовался для миниинвазивного и малотравматичного наружного дренирования костного гнойного очага, заведением дренажа в очаг остеомиелита через наружное свищевое отверстие. Это позволяло разделить лечение на этапы. На I этапе наладить аспирационное дренирование через функционирующий свищ. Добиться снятия воспалительного отека сегмента, общей воспалительной реакции, устранить постоянный болевой синдром. Уменьшить токсикоз, что в последующем, давало возможность подготовить больного ко II этапу оперативного вмешательства.
ДНАДКГО позволила пересмотреть и выработать новый подход в сроках дренирования очага. Показания к удалению дренажей из кости на основании: «скудное отделяемое», «незначительное», применяемое для мягких тканей, даже в повседневной практике не может быть критерием.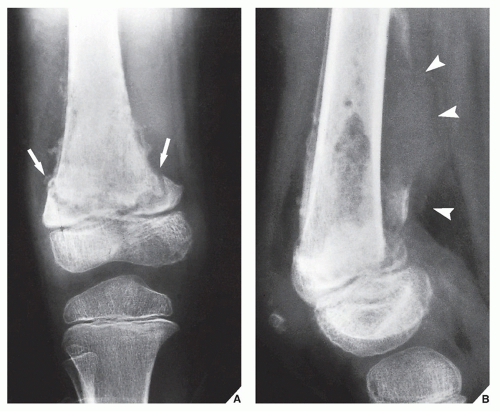 Что считать «скудным» для кости и для мягких тканей? В главе посвященной ВКГ в патогенезе остеомиелита было показано, что задержка более 5мл подобного экссудата в кости в течение суток у детей может расцениваться как состояние катастрофическое для организма ребенка.
Что считать «скудным» для кости и для мягких тканей? В главе посвященной ВКГ в патогенезе остеомиелита было показано, что задержка более 5мл подобного экссудата в кости в течение суток у детей может расцениваться как состояние катастрофическое для организма ребенка.
Экссудативные реакции в кости, отек тканей и следующая за ней внутрикостная гипертензия, являются кардинальными звеньями патогенеза, которые должны быть устранены в кратчайший и на длительный срок с момента установки диагноза. При использовании аспирационного
дренирования это происходит, за счет непрерывного оттока и позволяет достаточно точно посчитать количество экссудата отгекаемого из очага.
Длительное наружное удаление воспалительного экссудата из кости путем плазморреи, «мембранного просачивания», через нее, позволяет сравнить ДНАДКГО с ролью естественного ДПА. Костная ткань выполняет функцию «биологической мембраны», а прохождение, через нее плазмы, можно сравнить с интракорпоральным плазмаферезом.
Таким образом, сроки дренирования костного гнойного зависели от характера и степени отделяемого раневого экссудата, клинических, лабораторных, признаков стихания местного воспалительного процесса, рентгенологических данных и микроскопии дренажного экссудата и в среднем составили 9,5±6,2мес. Остаточной полости 1,2м.±10,3дн.
У больных с остеомиелитом, наличие гнойной раны, которая являлась своего рода «кожным окном», позволила в динамике проследить косвенную регенерацию в остеомиелитическом очаге при применении ДНАДКГО. Цитологическая и микробиологическая динамика мазков-отпечатков характеризовала воспалительный процесс и регенераторные изменения в тканях в раннем послеоперационном периоде. Процесс завершенности репаративных процессов в очаге также отражает динамика мазков отделяемого из дренажной трубки, установленной в послеоперационную рану и костный очаг. Такие исследования проведены у 25-ти больных.
По мере стихания воспалительного процесса в острой стадии, отсутствия осложнения, воспалительный тип мазка (рис. 25,26 ) сменялся на регенераторный тип отделяемого в мазках, без признаков дегенерации лейкоцитов, нейтрофилов, лимфоцитов. При этом снижалось количество лимфоцитов, и нарастали нейтрофилы в костном очаге.
25,26 ) сменялся на регенераторный тип отделяемого в мазках, без признаков дегенерации лейкоцитов, нейтрофилов, лимфоцитов. При этом снижалось количество лимфоцитов, и нарастали нейтрофилы в костном очаге.
Динамика цитологических элементов в мазках отделяемого экссудатау б-х с ОГО
100
Я 80 г
в 60 о
| 40
20 О
| флораоаущя
V
—V-X_у •«-фукмскиная'»*
Рис.24
-Пе(Жц™? 3 4 5 6 7 8 9 10 11 НМпхфты Недаш
Лимфоциты
Рис.25
В дальнейшем в мазках отмечались макрофаги, полибласты и остеобласты, указывающие на переход очага в стадию регенерации и реорганизации рубца. Обеспечение лучшего косметического результата достигается продолжением дренирования, до появления остеобластов и исчезновение остеокластов в морфологическом субстрате отделяемого экссудата из раны и кости.
Аналогичная закономерность с некоторыми особенностями прослеживается и при хронической стадии остеомиелита (рис. 27,28).
27,28).
В хронической стадии, в начале дренирования (рис.), также отмечается большое количество лейкоцитов (до 100в п/зр.), в цитологических мазках, но держится несколько длительней, 4-5 недель. В последующем их количество уменьшается (до 50-60 в п/зр.) и колеблется до максимальных величин. Вероятно, это зависело от неравномерности санации и фагоцитоза в костной ткани. То есть обильная флора сменялась скудной и оставалась такой в конце дренирования. После оперативного лечения в течение 2-х недель также имеется конвергенция в показателях нейтрофилов и лимфоцитов в очаге, то есть их становиться поровну 50:50. В последующем происходит дивергенция, но в меньшей амплитуде, этих форменных элементов. Ыейтрофилы увеличиваются в цитологических мазках до 90 в п/зр. С незначительными колебаниями, а лимфоциты соответственно снижаются. Эта динамика сохраняется до конца лечения.
Динамика цитологических элементов в мазках ‘отделяемого экссудата из дренежа у больных ХГО
Лимфоциты 120
Рис. 27
27
Регулирование в определенных параметрах экссудативных процессов в очаге остеомиелита за счет подаваемого разрежения, нормализует и модулирует миграцию фагоцитарных элементов в очаг воспаления, что способствует усилению местного фагоцитоза и удалению его продуктов через дренаж, скорейшей санации и деконтаминации гнойной костной ткани. Влияние на процессы в стадии экссудации в остром очаге, предупреждает распространение и генерализацию нагноения, деструкцию костной ткани, то есть повторные очаги альтерации и связанные с ними осложнения. В хронической стадии заболевания длительное регулирование процессом экссудации оптимизирует восстановительные механизмы в лролиферативной фазе, организации и реорганизации костной ткани, предупреждая преждевременное склерозирование и фиброз. Обеспечивает приток к пораженным тканям регенераторных элементов за счет стимулированной миграции. Модулирует образование костного матрикса и регенерацию очагов разрушения кости.
Данные исследований убедительно показали, что терапия острого остеомиелита особенно эффективна, в течение первых часов, от момента появления клинических симптомов заболевания, что и следует считать ранним лечением. Такая неукоснительная тактика повышает
Такая неукоснительная тактика повышает
резульгативнось нового способа лечения, позволяет предупредить осложнения, и на практике считать его способом решения проблемы остеомиелита в целом.
Сформулированная новая концепция патогенеза остеомиелита в
результате проведенных исследований и теоретического анализа, позволила глубже понять причины неблагоприятного течения заболевания, неудачи и осложнения, а главное их предупреждение и устранение в процессе лечения. На ее основе решить самую трудную задачу — предупреждение остеомиелитической деструкции кости и ее восстановления на месте разрушения костных структур.
Суть новой концепции состоит в том, что острое и хроническое ВОСПАЛЕНИЕ можно представить ввиде порочного круга и схемы основных клинических, патологических звеньев: нарушение микроциркуляции, плазморрея ВКГ, нагноение, деструкция, резорбция, токсикоз. Последнее обстоятельство поддерживает воспаление и нарушение микроциркуляции в костном очаге. /
плазморрея нагноение -
* \
/ деструкция
нарушение резорбция микроциркуляции
г к
В-воспаление
/К
токсикоз
гнойный свищ (рана)
секвестральная полость » (полость абсцесса)
резорбция
Рис. 28. Схема основных клинических, патологических звеньев.
На одном из этапов происходит самопроизвольное или оперативное дренирование гнойного костного очага с оттоком воспалительного экссудата, который не обеспечивает надежной санации очага остеомиелита. И порочный круг сохраняется. Происходит переход остеомиелита в хроническую стадию Вынужденная длительная противовоспалительная и деэскалационная антибактериальная терапия наряду с защитной функцией гомеостаза способствует подавлению эксудативной фазы воспаления и соответственно тормозит развитие пролиферативной стадии. В совокупности с
недостаточным дренажем очага данные процессы угнетают фагоцитоз, и восстановительные процессы в кости. (рана)
нарушение микроциркуляцип
VII.
деструкция резорбция
¡аспирационныП |
Рис. 2.9 Лечение остеомиелита ДНАДКГО в острой стадии. Лечение остеомиелита ДН АДКГО в хронической стадии.
В ней видно, что выпадают основные патогенетические звенья, поддерживающие воспалительный процесс в кости в острой и хронической стадии остеомиелита. Он создает условия для восстановительных механизмов и на практике решает трудную проблему гнойно-воспалительной деструкции кости подтвержденную Я- логическими исследованиями (рис. 30,31)
Больная М.,6 лет с острым гематогенным остеомиелитом правой бедренной кости. Заболела остро с высокой I и болей в бедре. Травма в анамнезе не отмечена. В течение суток проводилась консервативная терапия. На вторые сутки произведена операция -остеоперфорации в н/з бедренной кости. Последующая терапия была недостаточно эффективна. Нарастал токсикоз отек бедра, гноетечение. Наступил патологический перелом в н/з сегмента, который предпринято остеосинтезировать спицей Киршнера. На рис.30,31 видна развернутая картина заболевания, приведшая к патологическому перелому.
Рис.30 Рис.31
Рис.30,31. Больная М.,6 лет с острым гематогенным остеомиелитом правой бедренной кости. Развернутая картина заболевания, приведшая к патологическому перелому. Срок заболевания 2 мес. Больная в этом сроке была оперирована под общим обезболиванием. Применено ДНАДКГО с заведением дренажа через свищ.
Рис. 32 Рис. 33 Рис. 34 Рис. 35
Рис.32-35. Та же больная. Процесс лечения аспирационным дренированием. На Я-
граммах виден аспирационный дренаж и «груша» выполняющая роль аспирирующего устройства. Видна положительная динамика: купирование остеомиелита, наметившаяся консолидация перелома. Восстановление структуры костной ткани.
Рис.36. Та же больная. Результат Я-исследования через 7лет. Больной исполнилось 13 лет. Отсутствуют ортопедические нарушения, нет укорочения и нарушение походки. Иммобилизация сегмента 1,5мес,, срок дренирования 1г.8мес. Наступило выздоровление. Угловая деформация устранена в процессе роста сегмента. На контрольной Яо-графии бедра полностью восстановилась структура. Нет признаков перенесенного остеомиелита Функция конечности в полном объеме (рис. 36). Срок наблюдения 9лет. Отдаленный результат через 9 лет. (рис. 36). Рецидивов не было.
Таким образом, рентгенологические данные свидетельствуют об объективном контроле над регенерацией кости, в условиях гнойного воспаления и практическим восстановлением. Однако важен контроль, над ее полнотой, и отсутствием мелких секвестров, которые в отдаленный период, могли бы стать источником рецидива остеомиелита. С этой целью следует прибегать к КТ — исследованию (рис. 37, 38 )
Рис. 37
Рис. 38
Состояние после операции по поводу остемиелита бедренной кости в 2010 году ( до применения ДНАДКГО). При КТ-исследовании программой 1×1 с ретро-и реформантными реконструкциями: Бедренная кость сформирована правильно. В нижней трети визуализируется послеоперационный дефект (рис.213,216) кортикальной пластины по задней поверхности размером 4,6×1,6 см с наличием секвестров (рис.37) в костномозговом канале размером от 1,0×0,7 см до 0,9×4,5×0,3 см. Визуализируется частичное склерозирование (рис. 38) костномозгового канала. Общая протяженность изменений бедренной кости более 15 см
После дополнительного обследования и предоперационной подготовки девочке проведена операция по методике ДНАДКГО в плановом порядке, (рис. 39,40)
Вт рис.39
Рис. 40. Удалены секвестры во время операции.
■ I Рис. 40
Рис.41. Наружная поверхность бедра больной с установленными в п\о рану аспирационными дренажами с непринудительной аспирацией. Дренаж, выходящий из костного очага, указан стрелкой, фиксирован к коже полоской пластыря.
ДНАДКГО значительно уменьшает длительную химическую нагрузку на организм ребенка, сокращая системную терапию в послеоперационном
периоде. Выздоровление наступает у 98,6 — 100% больных в хронической и острой стадии остеомиелита соответственно по данным ближайших и отдаленных результатов наблюдения, которые составили от 8 до 30 лет.
ВЫВОДЫ.
1). Роль стафилококка в этиологии ОГО у детей уменьшается при переходе в хроническую стадию. Микробиологическая структура первичного очага в острой стадии в 70-80%, представлена стафилококком, а в хронической стадии его удельный вес не превышает 28-30% и имеет широкий спектр. Патогенез заболевания нуждаются в объединительной концепции. Клиническая картина остеомиелита разнообразна. Диагностика острой стадии не имеет строгой специфичности, поэтому распознание болезни чаще затруднено. Это ведет к лечебно-диагностическим и тактическим ошибкам в 21,8-54,7%, которые нередко приводят к глубоким разрушениями кости.
2). Иммуногенез острой стадии ГО у детей протекает с угнетением гуморального и клеточного звена иммунитета, фагоцитарной активности нейтрофилов крови и очага М, в, ФА< 10-13%, ФИ < 3,0). Наступают метаболические и биохимические нарушения в организме ребенка, местное распространение, генерализации, переход в сепсис, или хроническая стадия заболевания соответственно в 72%, 12 % и в 24-62 усл. % в группах сравнения.
3). Иммуногенез в хронической стадии ГО у детей протекает на фоне относительной активизации гуморального и угнетения клеточного звена иммунитета, нейтрофильного фагоцитоза крови и очага (увеличение в, А, ФИ<1,0). Нарушаются процессы ПОЛ, что формирует хронический очаг, с незавершенными зонами репаративной регенерации и микробную обсемененность. Это оказывает длительное патогенное влияние на организм ребенка, что часто становиться основным препятствием к выздоровлению.
4). Комплекс интенсивной терапии при остеомиелите оказывает
положительное воздействие и стабилизирует общее состояние больного ребенка. Распространенная первичная операция остеоперфорации (в острой стадии) и фистулсеквестрнекрэктомия (в хронической стадии) заболевания недостаточно эффективно санирует и деконтаминирует очаг воспаления. Это требует разработки нового подхода, универсального малотравматичного и высокоэффективного способа наружной санации и деконтаминации остеомиелитического очага.
5). Новый подход и способ длительного непрерывного аспирационного дренирования костного гнойного очага (ДНАДКГО) позволяет решить проблему наружной санации очага остеомиелита. Увеличение длительности наружного дренирования решает трудную проблему элиминации продуктов воспаления и микробов из очага и восстановления кости при гнойно-воспалительной деструкции. Осложнения, наступившие в остром периоде до применения метода, в т.ч. вследствие допущенных лечебно-диагностических и тактических ошибок, могут быть ликвидированы при применении ДНАДКГО, и не являются неразрешимыми задачами при его правильном применении.
6). Новая концепция патогенеза остеомиелита, заключается в обозначении и выделении порочного круга и практической схемы, которые доказывают, что острый и хронический остеомиелит принципиально не отличаются основными первичными клиническими звеньями, являясь локализованными стадиями единого процесса воспаления. Возникновение и течение остеомиелита при механической травме кости так же укладывается в новую концепцию и схему патогенеза.
7). Применение ДНАДКГО у детей с остеомиелитом, с учетом гидродинамики воспалительного процесса создает широкий, прямой и надежный дренажный канал для наружного оттока, с регулируемым разрежением внутри кости, принудительной аспирацией воспалительного экссудата и разобщает (разрывает) порочный, патологический круг на любой
стадии, и на длительный период заболевания.
ПРАКТИЧЕСКИЕ РЕКОМЕНДАЦИИ.
1. Технические характеристики методики позволяют применять ее в любом хирургическом стационаре, не требуют дополнительных финансовых затрат.
2. Новый способ хирургического лечения может служить методом выбора в лечении остеомиелита у детей в острой и хронической стадиях. Наиболее оптимальной и рациональной тактикой применения метода является дренирование КМК в течение первых 6 часов от начала заболевания.
3. ДНАДКГО может применяться для лечения остеомиелита различного происхождения.
4. Для достижения максимального результата, методика не должна применяться как конкурирующее лечение с общей терапией. Ее уникальность позволяет органично использовать ее в общем комплексе лечения.
5. Методика ДНАДКГО должна применяться с учетом гидродинамики воспалительного процесса.
6. Не рекомендуется применять разновариантные методы дренирования раны и кости, что может привести к нарущению дренажной функции тканей и затекам гнойного экссудата.
7. При осуществлении дренирования послеоперационной раны и костного очага необходимо соблюдать принцип раздельного дренирования в аспирационном режиме.
8. Рекомендуется применение методики одномоментного одновариантно-го раздельного дренирования кости и мягких тканей.
9. Тактической ошибкой следует считать сочетанное дренирование одновременно костного очага и мягких тканей.
10. Отказ от 1-х швов при высоком прогнозе нагноения послеоперационной раны.
11. Лечение ортопедических осложнений с использованием аппаратных конструкций должно применяться в сочетании с ДНАДКГО.
12. Длительное дренирование очага остеомиелита позволяет проводить все реабилитационные мероприятия, в том числе социальную адаптацию.
13. Для успешного широкого внедрения метода и получения максимального результата необходимо обучение хирургов теоретическим аспектам и практическим навыкам применения метода.
Список опубликованных работ по теме диссертации:
1. Цыбин A.A. Профилактика нагноения операционных ран.// Цыбин A.A., Бояринцев B.C., Ермилов А.Ю.// Издательство «Здоров’я». Клиническая хирургия №1,1989,с. 64-65.
2. Цыбин A.A. Аспирационное дренирование при анаэробной неклостри-диальной инфекции в хирургии.// Цыбин A.A., Бояринцев B.C., Ермилов А. Ю., и др.// Материалы Всесоюзного симпозиума « Анаэробная инфекция
в хирургии», г. Тернополь, 1989г.
3. Цыбин A.A.. Хирургический дренаж.// Бояринцев B.C., Цыбин A.A.// Авторское свидетельство № 1690785, 1991.
4. Цыбин A.A. Устройство для обработки кости.// Цыбин A.A., Бояринцев B.C., Войкин В.В.// Патент № 1780504, 1991.
5. Цыбин A.A., Аспирационное длительное дренирование в профилактике и лечении гнойных заболеваний мягких тканей. Материалы конференции молодых ученых, г. Москва, МОНИКИ, 1991.
6. Цыбин A.A. Способ лечения остеомиелита.// Бояринцев B.C., Цыбин A.A.// Авторское свидетельство №1769867, 1992.
7. Цыбин A.A., О патогенезе остеомиелита./’/ Цыбин A.A., Бояринцев B.C. // Сб.материалов научно-практической конференции посвященной 120-
летию со дня рождения Святителя Луки, профессора Войно-
Ясенецкого г.Симферополь, 1997.
8. Цыбин A.A. Аспирационное дренирование при остеомиелите. // Цыбин A.A., Бояринцев B.C.// Сб. материалов научно-практической конференции посвященной 120-летию со дня рождения Святителя Луки профессора Войно-Ясенецкого г. Симферополь, 1997.
9. Цыбин A.A. Формализация диагностических заключений и понятий в области хирургии и их взаимодействие при разработке экспертной системы.// Ивченко В.Д., Нурматова Е.В.,. Цыбин A.A.// Москва, 2001.,с.
77-78. Вест. нов. мед. техн. 2001-т.VIII, №3 с. 77-78.
10. Цыбин A.A. Свидетельство об официальной регистрации программы для ЭВМ № 2001611787.// Нурматова Е.В., Цыбин A.A.// Экспертная система диагностики заболеваний хирургического профиля и выработка
лечебной тактики (ARCHE1), 2001.
11. Цыбин A.A. Роль дренирования в профилактике раневых осложнений.// Цыбин A.A., Коноваленко С.И., Бояринцев B.C.// Сб. Материалов Всеармейской конференции с международным участием. Москва, 2002, с. 139-140.
12. Цыбин A.A., Активное лечение и дренирование ран. Инфекция в хирургии проблемы современной медицины. // Цыбин A.A., Генералов А.И., Бояринцев B.C.// Сб. Материалов Всеармейской конференции с международным участием. Москва, 2002, с. 139-140.
13. Цыбин A.A. Патогенез остеомиелита.// Бояринцев B.C., Коноваленко С.И.,. Цыбин A.A. // Вестник новых медицинских технологий — 2003 — т. х, № 1-2- с. 60-63.
14. Цыбин A.A. Новый подход в лечении остеомиелита. ДОКЛАДЫ АКАДЕМИИ НАУК, 2008, том 419, № 3, с. 425-429.
15. Цыбин A.A., Машков А.Е., Захарова Н.М., Хирургическое лечение острого остеомиелита. Детская хирургия, № 5, 2009, с. 38-41.
!б. Цыбин A.A. Способ лечения Воспалительного очага.// Цыбин A.A. Машков А.Е., Захарова Н.М.// Патент на изобретение № 2412724, РФ, 2009г.
17. Цыбин A.A. Длительный аспирационный дренаж при остеомиелите как продолжение хирургических разработок профессора В.Ф. Войно-Ясенецкого (святителя Луки). «Духовное и врачебное наследие святителя Луки ( Войно-Ясенецкого).// Бояринцев B.C., Цыбин A.A. // Сб. материалов научно-практической конференции с международным участием». Москва, 2010, с. 88-93.
18. Цыбин A.A. Хирургическое лечение хронического остеомиелита.// Цыбин A.A., Машков А.Е., Захарова Н.М.// Детская хирургия, № 2, 2010, с. 43-47.
19. Цыбин A.A. Некоторые аспекты патогенеза гематогенного остеомиелита у детей. // Цыбин A.A., Машков А.Е., Захарова Н.М., и др.// Биофизика, том 55,вып 3, 2010 с. 526-531.
20. Цыбин A.A. К вопросу об этиологии и патогенезе гематогенного остеомиелита у детей.// Цыбин A.A., Машков А.Е., Захарова Н.М., и др.// Детская хирургия, № 3, 2010, с. 15-19.
21. Цыбин A.A. Аспирационное дренирование в лечение ран. Духовное и врачебное наследие святителя Луки (Войно-Ясенецкого).// Цыбин A.A., Бояринцев B.C..// Сб. материалов научно-практической конференции с международным участием. Москва, 2010, с. 93-100.
22. Цыбин A.A. Цитологическая картина слизистой оболочки полости носа и околоносовых синусов у пациентов с полипозным риносинуситом при проведении NO-терапии.// Н.М.Захарова, С.Н. Шатохина, В.М. Свистушкин, и др.// Альманах клинической медицины № 25’2011 с 25-29
23. Цыбин A.A. Остеомиелит различного происхождения. Современное
состояние проблемы. Духовное и врачебное наследие святителя Луки (Войно-Ясенецкого).// Цыбин A.A., протоиерей Валерий Бояринцев.//Сб. материалов научно-практической конференции с международным участием. Москва, 2011, с 175-176
24. Цыбин A.A. Общие и местные закономерности течения остеомиелита, факторы, влияющие на этиопатогенез классификация. Духовное и врачебное наследие святителя Луки (Войно-Ясенецкого).// Цыбин A.A., протоиерей Валерий Бояринцев.// Сб. материалов научно-практической конференции с международным участием, Москва. 2011, с 177-183
25. Цыбин А. А. Некоторые аспекты патогенеза остеомиелита. Краткая история изучения. Духовное и врачебное наследие святителя Луки (Войно-Ясенецкого)./’/ Цыбин А. А., протоиерей Валерий Бояринцев.// Сб.
материалов научно-практической конференции с международным участием, Москва, 2011, с 184-190
26. Цыбин A.A. Хирургическое лечение ран мягких тканей. Духовное и врачебное наследие святителя Луки (Войно-Ясенецкого).// Цыбин A.A., протоиерей Валерий Бояринцев.// Сб. материалов научно-практической конференции с международным участием. Москва, 2011.
27. Цыбин A.A., протоиерей Валерий Бояринцев, Машков А.Е., Захарова
Н.М., Слесарев В.В. Некоторые особенности и преимущества длительного аспирационного дренирования. Сб. материалов четвертой международной научно-практической конференции. « Духовное и врачебное наследие святителя Луки (Войно-Ясенецкого). Москва 2012,с 205-212
28. Цыбин A.A. Способ лечения инфекционных осложнений переломов
трубчатых костей с использованием аппарата внешней фиксации.// Цыбин A.A., протоиерей Валерий Бояринцев, Машков А.Е., и др.// Сб. материалов четвертой международной научно-практической конференции « Духовное и врачебное наследие святителя Луки (Войно-Ясенецкого). Москва, 2012, с 212-217
29. Цыбин А.А.Цитологический контроль очага остеомиелита у детей. // Цыбин A.A., Машков А.Е., Слесарев В.В., и др.// Сб. Публикаций восьмой ежегодной Московской конференции с участием регионов России и стран СНГ «Гнойно-септические заболевания у детей», Москва, 7-8 июня 2012, с 156-157
30. Цыбин A.A. Этиологические аспекты остеомиелита у детей.// Машков А.Е., Цыбин A.A., Слесарев В.В., и др.// Сб. Публикаций восьмой ежегодной Московской конференции с участием регионов России и стран СНГ «Гнойно-септические заболевания у детей», Москва, 7-8 июня 2012, с 115-117
31. Цыбин А.А.Морфологические изменения очага хронического гематогенного остеомиелита у детей.// Султонов Ш.Р., Машков А.Е., Цыбин A.A., и др.// Сб. публикаций восьмой ежегодной Московской конференции с участием регионов России и стран СНГ «Гнойно-
септические заболевания у детей», Москва, 7-8 июня 2012, с 150-151
32. Цыбин A.A. Устройство для обработки кости.// Цыбин A.A., Машков А.Е., Сергеев C.B.// Патент на изобретение №2452414, РФ, 2012г
33. Цыбин A.A. Устройство для забора жидкости из организма.// Цыбин A.A., Машков А.Е., Захарова H.H. // Патент РФ на изобретение № 2422158, 201 !г
34. *Цыбин А.А.Устройство для аспирации патологического отделяемого из
организма.// Цыбин A.A., Машков А.Е.// Патент РФ на изобретение № 2422158,2012г.
35. Цыбин A.A. Способ хирургического лечения и профилактики инфекционных осложнений переломов трубчатых костей с использованием аппарата внешней фиксации. //. Цыбин A.A., Машков А.Е., Рушай А.К.//Патент РФ от 30.052012г.
36. Цыбин А.А.//Захарова Н.М., Шатохина С.Н., Волошин В.П. и др.// Особенности костной воспалительной реакции в области хирургического вмешательства при эндопротезировании тазобедренных суставов. «Альманах клинической медицины», т. XII, 2012
Цыбин Анатолий Александрович
Автореферат
Диссертации на соискание ученой степени доктора медицинских наук
Остеомиелит челюсти у детей: симптомы, причины, последствия
Главным признаком острого остеомиелита является боль, которая может проявляться по-разному. Она может концентрироваться в определенной точке или ощущаться распространенной по всей области челюсти. Иногда бывает так: ребенок испытывает спазмы при жевании, ему трудно глотать, а отек мешает открывать рот полностью. Обнаружение подобных симптомов требует срочного осмотра у специалиста.
Гораздо сложнее с маленькими детьми, которые не могут выразить словами, что их беспокоит. В этом случае тревогу следует бить уже при самых общих признаках: слабости, вялости, отказа от пищи, бледности, нарушении сна. Сразу нужно измерить температуру, проверить полость рта на наличие отеков или покраснений, присмотреться к контуру лица, чтобы обнаружить или, наоборот, исключить асимметрию. При наличии любого из перечисленных симптомов нужно показать малыша врачу.
Хронический остеомиелит у детей
Детям для развития хронической стадии достаточно нескольких дней, а то и меньше, поэтому так важно показать их врачу и начать лечение как можно скорее.
После диагностирования остеомиелита у ребенка нужно быть начеку, нельзя прекращать назначенный курс терапии только потому, что симптомы уменьшились или даже, на первый взгляд, исчезли. Хроническую стадию можно сравнить с бомбой замедленного действия: при отсутствии прежней боли и лихорадки может происходить разрушение костной ткани. Скорее всего, ребенок будет продолжать испытывать слабость и переутомление, кроме того, в области челюсти может прощупываться уплотнение, нажатие на которое все-таки будет сопровождаться болью. Также при пальпации области шеи и под челюстью можно обнаружить увеличение лимфоузлов.
Явный сигнал со стороны организма — появление свищей во рту. Свищ представляет собой либо закрытый «мешочек» с гнойным содержимым, похожий на прыщ, либо отверстие, через которое вытекает гной. В запущенных случаях отверстия каналов для выведения гноя могут находиться не только на слизистой, но и на коже.
Это наиболее распространенный вариант развития событий. Однако у ребенка может случиться первичный тип хронического остеомиелита, которому не предшествует острая стадия. Тогда на начальном этапе можно заметить лишь недомогание, слабость и увеличение лимфоузлов. Болезненные ощущения могут присутствовать, но не такие явные, как при остром или вторичном хроническом заболевании.
Если не обращать внимания на перечисленные симптомы и вовремя не обратиться к врачу, то есть риск обнаружить болезнь, когда уже начнется деформация кости и изменение формы челюсти.
Последствия заболевания и реабилитация
Запущенный гнойный процесс затрагивает не только челюсть, но и переходит в челюстные пазухи и орбиты. У маленьких детей воспаление нередко затрагивает даже черепную ямку. Это приводит к дополнительным серьезным заболеваниям, таким как гнойные синуситы и менингиты. При отсутствии лечения воспаление будет распространяться все дальше и дальше, захватывая области на шее и грудной клетке, образуя флегмоны. Одним из тяжелых исходов является заражение крови.
Характерным для детей осложнением хронического остеомиелита является гибель зачатков постоянных зубов. Наличие в челюсти фрагментов омертвевшей твердой ткани способно привести к некрозу.
Деформация челюсти или задержка ее роста и, как следствие, изменение формы лица — это не единственные заметные со стороны осложнения. Остеомиелит челюсти может не только препятствовать функционированию жевательного аппарата, но и довольно заметно влиять на внешность. Из-за дефектов костной ткани могут не формироваться постоянные зубы, а из-за ослабления структуры челюсть может подвергаться частым переломам. Последнее грозит еще и формированием ложных суставов. В дальнейшем могут быть такие «отголоски», как болезни височно-нижнечелюстного сустава (артриты и артрозы).
Реабилитация у детей после изменения формы кости и гибели зачатков зубов происходит постепенно. В период, когда еще формируются кости черепа, оперативное вмешательство сводят к минимуму — зубные протезы ставят временные, также избегают операций из серии пластической хирургии. Зато применяют физиотерапевтические процедуры, способствующие нормализации работы височно-нижнечелюстного сустава. После окончания формирования черепа при необходимости можно делать пластические операции и постоянное протезирование зубов.
Кроме того, дети, у которых был диагностирован остеомиелит челюсти, должны состоять на учете у стоматолога и два раза в год обязательно его посещать.
Диагностика
Диагностика проводится поэтапно. Сначала собираются данные при осмотре пациента. Врач отмечает покраснение, отеки, наличие уплотнений, проверяет устойчивость зубов в лунке. По синюшности слизистой выясняет, где находится очаг воспаления, а путем пальпации определяет наличие гнойных масс.
Выводы врача требуют рентгенографического подтверждения. На снимке будет видно местоположение очага остеомиелита, участков деструкции и уплотнения кости, некротических фрагментов и омертвевших зачатков зубов. Однако в сложных случаях остеомиелита кости обычного рентгена может быть недостаточно и пациента направят на томографию. Кроме того, при наличии свищей может потребоваться фистулография, в процессе которой в каналы с гнойным отделяемым вводят специальное вещество, а затем проводят их рентгеноскопию.
Пациента могут дополнительно направить на анализы крови и мочи, чтобы удостовериться в повышении уровня содержания белков и лейкоцитов, что подтвердит диагноз. С помощью анализа крови также следят за течением болезни, определяя начало ремиссии.
Лечение
После диагностирования остеомиелита лечение включает в себя устранение омертвевших участков и гноя, а также антибиотикотерапию для уничтожения гнилостной микрофлоры.
Если у пациента определен одонтогенный остеомиелит, то удаляют зуб, который стал очагом инфекции. В этом случае гной обычно выходит естественным образом из лунки, но врач может сделать дополнительное отверстие для оттока, если того требует ситуация.
После удаления вскрывают надкостницу для устранения образовавшихся абсцессов. Полости очищают от некротизированных масс, обрабатывают антибиотиками и антисептиками. Терапия предусматривает также применение иммуностимулирующих средств, способствующих восстановлению организма.
При остеомиелите детей госпитализируют, так как им необходим врачебный присмотр и лечение, которое может быть обеспечено именно в отделении хирургии. Чем раньше будет произведена операция, тем вероятнее скорое выздоровление, и наоборот, промедление в этих случаях может грозить серьезными осложнениями.
При хроническом остеомиелите тоже предусмотрено операционное вмешательство для удаления омертвевших частей, например зачатков постоянных зубов. Некротизированные фрагменты должны быть извлечены, иначе они будут поддерживать воспалительные процессы. Однако на первом месте будет медикаментозная терапия: устранение инфекции с помощью антибиотиков, нейтрализация аллергической реакции антигистаминными препаратами и стимуляция иммунитета укрепляющими средствами. Кроме того, применяются такие методики, как лазерная физиотерапия.
МОРФОЛОГИЧЕСКАЯ ОЦЕНКА ПОСЛЕДСТВИЙ ГЕМАТОГЕННОГО ОСТЕОМИЕЛИТА ДЛИННЫХ КОСТЕЙ У ДЕТЕЙ | Гаркавенко
1. Болабовко А.Э. Морфологическая характеристика врожденных и приобретенных ложных суставов у детей [автореф. дис. … канд. мед. наук]. СПб.: ГУ НИДОИ им. Г.И. Турнера; 2003.
2. Гаркавенко Ю.Е. Ортопедические последствия гематогенного остеомиелита длинных трубчатых костей у детей (клиника, диагностика, лечение) [автореф. дис. … д-ра мед. наук]. СПб.: ФГБУ НИДОИ им. Г.И. Турнера; 2011.
3. Гаркавенко Ю.Е., Поздеев А.П. Отдаленные функциональные результаты артропластики тазобедренного сустава у детей с последствиями острого гематогенного остеомиелита. Травматология и ортопедия России. 2008; 4: 46-53.
4. Гаркавенко Ю.Е., Поздеев А.П. Ортопедические последствия гематогенного остеомиелита длинных трубчатых костей у детей. В кн.: Педиатрия. Национальное руководство в двух томах. М., 2009. Т.2. с. 546-552.
5. Даниелян О.А. Деформации суставов нижних конечностей у детей и подростков при последствиях гематогенного остеомиелита (клиника, диагностика, лечение) [автореф. дис. … д-ра мед. наук]. СПб.: НИДОИ им. Г.И. Турнера; 1996.
6. Николаев А.И. Профилактика и раннее комплексное лечение детей с патологическим вывихом бедра [автореф. дис. … канд. мед. наук]. СПб.: ФГУ НИДОИ им. Г.И. Турнера; 2005.
7. Поздеев А.П. Ложные суставы и дефекты костей у детей [автореф. дис. … д-ра мед. наук]. СПб.: НИДОИ им. Г.И. Турнера; 1999.
8. Самков А.С. Деформации костей и суставов после гематогенного остеомиелита у детей. В кн.: Травматология и ортопедия: руководство для врачей под ред. Ю.Г. Шапошникова. М., 1997. Т. 3. с. 566-574.
9. Скворцов А.П. Хирургическое лечение последствий гематогенного остеомиелита области суставов нижних конечностей у детей [автореф. дис. . д-ра мед. наук]. Казань: Казанская ГМА, НИЦ «ВТО»; 2008.
10. Blockey N.J. Chronic osteomyelitis, an unusual variant. J. Bone Joint Surg.Br. 1983;65(2):120-123.
11. Calhoun J.H., Manring M.M., Shirtliff M. Osteomyelitis of the long bones. Seminars in plastic surgery. 2009; 23(2):59-72.
12. Carek P.J., Dickerson L.M., Sack J.L. Diagnosis and management of osteomyelitis. Am Fam. Physician. 2001;63(12):2413-2420.
13. Carr A.J., Cole W.G., Roberton D.M., Chow C.W. Chronic multifocal osteomyelitis. J. Bone Joint Surg. Br. 1993;75:582-591.
14. Deogaonkar K., Ghandour A., Jones A., Ahuja S., Lyons K. Chronic recurrent multifocal osteomyelitis presenting as acute scoliosis: a case report and review of literature. Eur Spine J. 2008;17 (Suppl. 2):S248-S252.
15. Khanna G., Sato T.S.P., Ferguson P. Imaging of Chronic Recurrent multifocal osteomyelitis. RadioGraphics 2009;29:1159-1177.
16. Rasool M.N. Primary subacute haematogenous osteomyelitis in children. J Bone Joint Surg. Br. 2001;83:93-98.
Отдаленные результаты лечения тотального поражения кости при остром гематогенном остеомиелите у детей
Ключевые слова: острый гематогенный остеомиелит, тотальное поражение длинных трубчатых костей, остеоперфорация, дренирование полости флегмоны.
Актуальность проблемы. Диагностика и лечение острого гематогенного остеомиелита до настоящего времени остается актуальной проблемой детской хирургии. Внедрение новых технологий в лечении острого гематогенного остеомиелита у детей играет ведущую роль в ближайших и отдаленных исходах заболевания.
Цель. Улучшение результатов лечения острого гематогенного остеомиелита у детей при тотальном поражении длинных трубчатых костей.
Материал и методы. Тотальное поражение кости наблюдали у 13 больных в возрасте от рождения до 16 лет, находившихся на лечении в Центре детской хирургии. Из них большеберцовой кости — в 4 случаях, малоберцовой — в 3, бедренной — в 3, плечевой — в 2, лучевой — в 1 случае. Оперативное лечение проведено у 12 больных, консервативное — у 1 пациента. У одного больного с тотальным поражением большеберцовой кости было выявлено множественное поражение костей — 9 локализаций (рис. 1). Все дети поступали в сроки свыше 4 суток от начала заболевания. Септико-пиемическая форма острого гематогенного остеомиелита была выявлена у всех пациентов.
Рис. 1. Множественное поражение костей при остром гематогенном остеомиелите (9 локализаций)
Результаты и обсуждение. Тотальное поражение большеберцовой кости отмечено у 4 больных, из них у 1 — консервативное лечение пункциями и у 3 — оперативное: двоим выполнено сквозное дренирование кости и полости флегмоны, одному — вскрытие флегмоны множественными разрезами на всем протяжении.
Тотальное поражение малоберцовой кости выявлено у 3 больных с наличием флегмоны мягких тканей: у 2 произведены остеоперфорации в проксимальном и дистальном метафизе с дренированием флегмоны, у 1 больного выполнены остеоперфорации малоберцовой кости с дренированием кости и флегмоны.
Тотальное поражение бедренной кости наблюдали в 3-х случаях. Из них без вовлечения в процесс шейки бедра — в 2: у одного больного произведено сквозное дренирование кости на всем протяжении и полости флегмоны, у второго — выполнено сквозное дренирование полости флегмоны без дренирования кости. У третьего пациента произведено вскрытие флегмоны множественными разрезами на протяжении.
Клинический случай 1:
Пациент Г. Поступил в ДХЦ через 3,5 недели от начала заболевания с диагнозом острый гематогенный остеомиелит правой бедренной кости. На рентгенограмме — тотальный секвестр, патологический перелом, патологический вывих бедра (рис. 2).
Рис. 2. Пациент Г., 3,5 недели от начала заболевания
Через 1,5 года от начала заболевания (рис. 3) после проведенного комплексного лечения пациент Г. был приглашен на контрольное обследование. Наблюдается укорочение конечности на 2 см, сколиоз, плоскостопие.
Рис. 3. Пациент Г., 1,5 года от начала заболевания
Тотальное поражение плечевой кости встречали в 2-х случаях: произведены остеоперфорации в проксимальном и дистальном метафизе со сквозным дренированием полости флегмоны.
Клинический случай 2:
Пациент Л., 3 года. Поступил через 2 недели от начала заболевания с диагнозом острый гематогенный остеомиелит плечевой кости. Проведено комплексное лечение. Комплексное лечение включает в себя декомпрессию остеомиелитического очага (рис.4), применение антибиотиков, низкоинтенсивное лазерное излучение.
Рис. 4. Схема операции (1-доступ, 2-распространение флегмоны, 3-первая дренажная трубка, 4-вторая дренажная трубка, 5-остеоперфорации)
На рентгенограмме через 2 месяца от начала заболевания намечается линия патологического перелома (рис. 5), через 3 месяца — патологический перелом с секвестром (рис. 6), через 3,5 месяца у пациента Л. сформировался ложный сустав (рис. 7), через 1 год от начала заболевания наблюдается ограничение движения в суставе (рис. 8).
Рис. 5. Пациент Л., 2 месяца от начала заболевания
Рис. 6. Пациент Л., 3 месяца от начала заболевания
Рис. 7. Пациент Л., 3,5 месяца от начала заболевания
Рис. 8. Пациент Л., 1 год от начала заболевания
Через 2 года от начала заболевания пациент Л. был приглашен на контрольное обследование. Функция в суставе полностью восстановлена.
У одного больного было тотальное поражение лучевой кости с гнойным артритом локтевого сустава, произведена артротомия локтевого сустава со сквозным промывным дренажем и пункционная декомпрессия кости.
Переход в хроническую форму выявлен у 8 (61,5 %) пациентов. В том числе плечевой — у 1 больного (патологический перелом с формированием ложного сустава), бедренной — у 1 (секвестральная форма), большеберцовой — у 3 (секвестральные формы), малоберцовой — у 3 (секвестральные формы).
Выводы:
1. Для первичной диагностики остеомиелита нужно применять лечебно-диагностическую пункцию воспалительного очага с взятием материала для цитологического и бактериологического исследования с одновременной декомпрессией костномозгового канала.
2. Лечение при тотальном поражении кости остеомиелитом должно быть направлено на проведение ранней декомпрессивной остеоперфорации, длительной антибиотикотерапии, восстановление кровообращения в пораженной конечности.
3. При тотальном поражении кости нижних конечностей при остром гематогенном остеомиелите в дальнейшем наблюдался сколиоз, разница между уровнем лопаток 1,5–2 см, плоскостопие.
Литература:
1. Катько В. А. Гематогенный остеомиелит у детей: монография / Минск: БГМУ, 2007. — 160 с. — ISBN 978–985–462–778–6. — С. 86–126
2. Акжигитов Г. Н. Гематогенный остеомиелит / Г. Н. Акжигитов, Я. Б. Юдин. М.: Медицина, 1998. 288 с.
3. Катько В. А. Детская хирургия: учеб. пособие / Минск: Выш. шк., 2009. — 507 с.: ил. ISBN 978–985–06–1636–4. — С. 300–316
4. Гринев М. В. Остеомиелит / М. В. Гринев. Л.: Медицина, 1977. 152 с.
Остеомиелит у детей | Детская больница Филадельфии
Остеомиелит — это инфекция кости. Инфекция чаще встречается в длинных костях тела, но может поражать любую кость в организме. Остеомиелит может возникнуть у детей любого возраста, но чаще встречается у недоношенных детей и детей, рожденных с осложнениями, поскольку их иммунная система может быть не полностью развита.
Остеомиелит может вызывать множество различных видов бактерий. Самый распространенный вид бактерий — Staphylococcus aureus .Грибки также могут вызывать остеомиелит. Бактерии и грибки могут попадать в организм различными путями, включая, помимо прочего, следующие:
Инфицированные раны
Открытые переломы, при которых сломанные кости проникают через кожу
Посторонний предмет, проникающий под кожу
Зараженные суставы
Инфекция, которая распространяется из другого источника внутри тела, например ушные инфекции
Травма
Ниже приведены наиболее частые симптомы остеомиелита.Однако каждый ребенок может испытывать симптомы по-разному. Симптомы могут включать:
Нежность или боль в инфицированной области
Ребенок может использовать ограниченную или не использовать инфицированную конечность
Ребенок обычно будет охранять или защищать эту область от прикосновений или видимых
Отек в инфицированной зоне
Покраснение в зоне поражения
Тепло вокруг зараженной территории
Лихорадка
Важно немедленно обратиться к врачу при подозрении на остеомиелит.Симптомы остеомиелита могут напоминать другие состояния или проблемы со здоровьем. Всегда консультируйтесь с врачом вашего ребенка для постановки диагноза.
Врач ставит диагноз остеомиелита на основании полной истории болезни ребенка, медицинского осмотра и диагностических тестов. Врач собирает полную историю беременности и родов ребенка и спрашивает, не болел ли ребенок в последнее время простудными заболеваниями или другими инфекциями.
Диагностические процедуры могут включать:
Рентгеновские снимки. Диагностический тест, использующий невидимые лучи электромагнитной энергии для создания изображений внутренних тканей, костей и органов на пленке.
Сканы костей. Метод ядерной визуализации для оценки любых дегенеративных и / или артритных изменений суставов; для выявления заболеваний и опухолей костей; для определения причины боли в костях или воспаления.
Анализы крови
Специфическое лечение остеомиелита определит врач вашего ребенка на основании:
Возраст вашего ребенка, общее состояние здоровья и история болезни
Степень состояния
Толерантность вашего ребенка к определенным лекарствам, процедурам или методам лечения
Ожидания по ходу состояния
Ваше мнение или предпочтение
Цель лечения — облегчить боль и полностью вылечить инфекцию.Лечение может включать одно или несколько из следующих действий:
В большинстве случаев инфекция лечится антибиотиками. В тяжелых случаях остеомиелита инфекция может быть очень разрушительной для костей, окружающих мышц, сухожилий и кровеносных сосудов, что приводит к длительной или хронической инфекции. Ампутация инфицированной конечности встречается редко.
Острый гематогенный остеомиелит | Американская академия педиатрии
Цели
После прочтения этой статьи читатели должны уметь:
Опишите патофизиологию острого гематогенного остеомиелита.
Сопоставьте наиболее частые инфекционные причины остеомиелита с возрастом пациента.
Распознать типичные клинические проявления острого гематогенного остеомиелита.
Объясните, как правильно использовать дополнительную информацию, полученную в результате лабораторных исследований и визуализационных исследований, для постановки диагноза острого гематогенного остеомиелита.
Обсудите медицинские и хирургические принципы ведения при лечении острого гематогенного остеомиелита.
Патофизиология
Наиболее распространенным типом остеомиелита, инфекции костей, который встречается у детей, является острый гематогенный остеомиелит. Первоначально инфекция возникает в метафизарной области трубчатых костей, начиная с метафизита после посева бактериями. Аппендикулярный скелет — наиболее частая локализация остеомиелита. Нижняя конечность, особенно бедренная кость, поражается чаще, чем верхняя конечность, где наиболее вероятно инфицирование плечевой кости.Кости таза или ключицы поражаются реже, чем длинные кости конечностей. Наиболее частая кость, поражающая детей при остром гематогенном остеомиелите, — это бедренная кость. Осевой скелет с меньшей вероятностью может быть очагом острого гематогенного остеомиелита. Проявлениями остеомиелита с поражением осевого скелета чаще всего являются дискит, остеомиелит позвоночника и инфекции ребер и костей черепа.
В большинстве случаев предшествующая бактериемия, приводящая к острому гематогенному остеомиелиту, протекает скрыто и бессимптомно, хотя остеомиелит может быть очаговым осложнением клинически симптоматической бактериемии и даже явной сепсии.Очаг инфекции начинается в бесклапанных синусоидальных петлях венул при их отражении от эпифиза и объясняется медленным и неламинарным кровотоком через этот сосуд. Манодж Рамачандран, консультант, детский хирург-ортопед
- 1 Центр ортопедии, Королевские больницы Лондона и Бартса и Лондонские детские больницы, Фонд здравоохранения Бартса, NHS Trust, Лондон E1 1BB
- Для корреспонденции: Мадж Рамачандран.ramachandran {at} bartshealth.nhs.uk
- Одобрено 23 декабря 2013 г.
Острый остеомиелит — редкое, но серьезное заболевание, поражающее ранее здоровых детей. Требуется высокий индекс подозрительности, поскольку раннее лечение имеет важное значение для хорошего результата. В последнее десятилетие быстрые изменения в эпидемиологии этого состояния, в частности инфекций, вызванных устойчивым к метициллину Staphylococcus aureus (MRSA), и достижения в области диагностики выявили необходимость изменения практики, основанной на имеющихся данных.Мы рассматриваем соответствующие аспекты острого остеомиелита, выделяя подводные камни в диагностике и обеспечивая основу для лечения.
Сводные пункты
Острый остеомиелит у детей — это инфекция кости продолжительностью менее двух недель, которая обычно распространяется гематогенно
Метициллин-резистентная Staphylococcus aureus , особенно остеомиелит
9000, увеличивается.Задержка в диагностике может вызвать нарушение роста, деформацию или даже смерть
Лечение включает своевременное внутривенное введение антибиотиков
Многопрофильный подход с участием бригад первичной, вторичной и третичной медицинской помощи необходим для обеспечения хорошего результата
Дети могут поступать незаметно, поэтому требуется тщательный сбор анамнеза и клиническое обследование с высоким показателем подозрительности
Что такое острый остеомиелит?
Остеомиелит — это воспаление костей, вызванное гноеродными организмами.В остром периоде симптомы продолжаются менее двух недель. Основными источниками инфекции являются гематогенное распространение, отслеживание от соседних очагов инфекции и прямая инокуляция после травмы или хирургического вмешательства1. Гематогенное распространение — наиболее частый источник инфекции у детей, обычно поражающий длинные кости. Семена инфекции в метафизе, где кровоток обильный, но вялый.2 Чаще всего поражаются бедренная и большеберцовая кость (27% и 26%, соответственно, рис. 1⇓) .3
Источники и критерии отбора
Мы провели поиск в Medline и Google Scholar, используя термины «p (a) ediatric», «острый остеомиелит», «инфекция костей», «септический артрит», «антибиотики» и «визуализация».По возможности мы использовали данные рандомизированных контролируемых испытаний, систематических обзоров (включая Кокрановские обзоры) и экспертных обзоров…
(PDF) Диафизарный остеомиелит бедренной кости с подозрением на саркому Юинга у детей 8 лет: отчет о болезни
Sananta P et al . Int J Res Med Sci. 2018 Dec; 6 (12): 4110-4115
Международный журнал исследований в области медицинских наук | Декабрь 2018 | Том 6 | Выпуск 12 Страница 4114
Успешное лечение остеомиелита зависит от правильного выбора и введения антибиотика
, терапии и хирургического вмешательства по мере необходимости.Эмпирические
антибиотиков у педиатрических пациентов с остеомиелитом следует лечить
антибиотиками, которые имеют превосходный охват инфекция,
клинический ответ и наличие основных факторов риска.
Обычно дается от 3 до 6 недель антибиотикотерапии
в зависимости от клинического ответа.Имеются убедительные
доказательств того, что лечение продолжительностью менее 3 недель приводит к
неприемлемо высокой частоте рецидивов. Хроническая инфекция
зарегистрирована у 19% детей, получавших лечение менее 3 недель
по сравнению с 2% у детей, пролеченных дольше
3 недели.25
Авторы полагались на клиническую оценку и низкий уровень подозрения Юинга (
). Остеомиелит
трудно отличить от злокачественных опухолей костей, так как у него отсутствуют
специфических признаков и симптомов.Различие между двумя потенциальными диагнозами
важно для того, чтобы начать правильное клиническое ведение
.
ЗАКЛЮЧЕНИЕ
Представление остеомиелита бедренной кости, имитирующего
опухоли костей, подчеркивает важность клинического
анамнеза, лабораторных исследований и рентгенографических интерпретаций
в диагностике этого состояния, которое обычно трудно обнаружить.
трудно отличить
остеомиелит бедренной кости от опухолей кости
с помощью простой пленочной рентгенографии, и это состояние
обычно имитирует саркому Юинга.Считается, что МРТ
является чувствительным и полезным методом лечения этого состояния. Когда
все визуализирующие и клинические признаки рассматривались как
вместе, только этническая принадлежность и наличие мягких тканей
были прогностическими для диагноза. Хотя открытая биопсия
обеспечивает более высокую диагностическую ценность, мы по-прежнему поддерживаем выполнение чрескожной биопсии в первую очередь, чтобы избежать риска заболеваемости
, связанного с хирургическими процедурами.Мы
рекомендуем получить консультацию хирурга
перед чрескожной биопсией, чтобы гарантировать, что пациент
быстро пройдет открытую процедуру, если результаты первоначальной биопсии
неубедительны.
Финансирование: Нет источников финансирования
Конфликт интересов: не заявлен
Этическое одобрение: не требуется
ССЫЛКИ
1. Tountas AA, Kwok JM. Острый гематогенный
диафизарный остеомиелит в детском возрасте.Канадская
Медицинская ассоциация J. 1985, 1 июня; 132 (11): 1287.
2. Пацакис М.Дж., Залаврас К.Г. Хронический посттравматический
остеомиелит и инфицированное несращение большеберцовой кости:
современные концепции лечения. JAAOS. 2005 Октябрь
1; 13 (6): 417-27.
3. McCarville MB. Ребенок с болью в костях:
злокачественных новообразований и имитаторов. Визуализация рака.
2009 (9): S115-21.
4. Фрэнк Г., Махони Х.М., Эппес, Южная Каролина.Скелетно-мышечные
инфекции у детей. Pediatr Clin North Am.
2005; 52 (4): 1083-106.
5. Гутьеррес К. Инфекции костей и суставов у детей.
Детская поликлиника. 1 июня 2005 г .; 52 (3): 779-94.
6. Йео А., Рамачандран М. Острый гематогенный
Остеомиелит у детей. BMJ. 2014 Янв
20; 348 (315): g66.
7. Абди Р., Тахери ММН. Отчет о случае саркомы Юинга
эпифиза большеберцовой кости с ретробульбарной массой.J
Хирургия и травма. 2015; 3 (1-2): 23-5.
8. Пелтола Х., Пяакконен М. Острый остеомиелит у
детей. N Engl J Med. 2014; 370 (4): 352-60.
9. Кремерс Х.М., Нводжо М.Э., Рэнсом Дж. Э., Вуд-
Вентц С.М., Мелтон III LJ, Хаддлстон III PM.
Тенденции эпидемиологии остеомиелита. популяционное исследование
, 1969–2009 гг. J Bone Joint
Surg Am. 2015; 97: 837-45.
10. Сферопулос Н.К.Лобковая саркома Юинга у ребенка
, ошибочно диагностированного как остеомиелит: описание случая.
Res Rev Ortho. 2017: 1 (2): 4-8.
11. Форсберг JA, Кайл Поттер MAJB, Cierny III G,
Webb L. Диагностика и лечение хронической инфекции
. J Am Acad Orthop Surg. 2009: 8-19.
12. Хеннингер Б., Глодный Б., Рудиш А., Триб Т.,
Лоизидес А., Путцер Д., Джудмайер В., Шок М.Ф.
Саркома Юинга против остеомиелита: дифференциальный диагноз
Диагностика с помощью магнитно-резонансной томографии.
Skeletal Radiol. 2013 (42): 1097-104.
13. Несбит М.Э. младший, Гехан Э.А., Бургерт Э.О. мл., Вьетти Т.Дж.,
Кангир А., Теффт М. и др. Мультимодальная терапия для лечения
первичной неметастатической саркомы кости
Юинга: долгосрочные результаты исследования First
Intergroup. J Clin Oncol. 1990; 8 (10): 1664-74.
14. Видхе Б., Видхе Т. Начальные симптомы и особенности
остеосаркомы и саркомы Юинга. J Bone Joint
Surg Am.2000; 82 (5): 667-74.
15. Heck Jr RK. Злокачественные опухоли костей. В: Терри
Canale S, Beaty JH. Оперативная служба Кэмпбелла
ортопедия. 11 изд. Филадельфия:
Мосби; 2008: 901-38.
16. Варунджикар, доктор медицинских наук, Джаян Б.Э. Остеомиелит бедренной кости
, имитирующий саркому овец — описание случая. Sch J Med
Case Rep.2014; 2 (2): 118-21.
17. Буксир BPB, Tan MH. Отсроченный диагноз саркомы Юинга
правой плечевой кости, первоначально рассматривавшейся как хронический остеомиелит
: отчет о клиническом случае.J Orthop Surg.
2005: 13 (1): 88-92.
18. Меткалфеа Дж. Э., Гример Р. Дж. Саркома Юинга стопы
, маскирующаяся под остеомиелит. Euro Foot
Ankle Soc. 2004 (10): 29-33.
19. McCarville MB, Chen JY, Coleman JL, Li Y, Li X,
Adderson EE, et al. Отличить остеомиелит
от саркомы Юинга с помощью рентгенографии и МРТ. AJR
Am J Roentgenol 2015; 205 (3): 640-51.
20. Funk SS, Copley LAB.Острый гематогенный
остеомиелит у детей Патогенез, диагностика,
Диафизарный остеомиелит бедра с подозрением на саркому Юинга у детей 8 лет: история болезни | Сананта
Tountas AA, Kwok JM. Острый гематогенный диафизарный остеомиелит в детском возрасте. Канадская медицинская ассоциация J. 1 июня 1985 г .; 132 (11): 1287.
Пацакис MJ, Залаврас CG. Хронический посттравматический остеомиелит и инфицированное несращение большеберцовой кости: современные концепции лечения.JAAOS. 2005 г., 1 октября; 13 (6): 417-27.
McCarville MB. Ребенок с болями в костях: злокачественные новообразования и имитаторы. Визуализация рака. 2009 (9): S115-21.
Фрэнк Г., Махони Х.М., Эппес, Южная Каролина. Скелетно-мышечные инфекции у детей. Pediatr Clin North Am. 2005; 52 (4): 1083-106.
Гутьеррес К. Инфекции костей и суставов у детей. Детские клиники. 1 июня 2005 г .; 52 (3): 779-94.
Йео А., Рамачандран М. Острый гематогенный остеомиелит у детей. BMJ. 2014 20 января; 348 (315): g66.
Abdi R, Taheri MMH. Отчет о случае саркомы Юинга эпифиза большеберцовой кости с ретробульбарной массой. J Surg и травма. 2015; 3 (1-2): 23-5.
Peltola H, Pääkkönen M. Острый остеомиелит у детей. N Engl J Med. 2014; 370 (4): 352-60.
Кремерс Х.М., Нводжо М.Э., Рэнсом Дж.Э., Вуд-Венц С.М., Мелтон III LJ, Хаддлстон III PM. Тенденции эпидемиологии остеомиелита. популяционное исследование, 1969–2009 гг. J Bone Joint Surg Am. 2015; 97: 837-45.
Сферопулос Н.К.Лобковая саркома Юинга у ребенка, ошибочно диагностированного как остеомиелит: клинический случай. Res Rev Ortho. 2017: 1 (2): 4-8.
Forsberg JA, Kyle Potter MAJB, Cierny III G, Webb L. Диагностика и лечение хронической инфекции. J Am Acad Orthop Surg. 2009: 8-19.
Henninger B, Glodny B, Rudisch A, Trieb T., Loizides A, Putzer D, Judmaier W, Schocke MF. Саркома Юинга против остеомиелита: дифференциальный диагноз с помощью магнитно-резонансной томографии. Skeletal Radiol. 2013 (42): 1097-104.
Несбит М.Э. младший, Гехан Е.А., Бургерт Е.О. младший, Вьетти Т.Дж., Кангир А., Теффт М. и др.Мультимодальная терапия для лечения первичной неметастатической саркомы кости Юинга: долгосрочное наблюдение за результатами исследования первой межгрупповой группы. J Clin Oncol. 1990; 8 (10): 1664-74.
Widhe B, Widhe T. Начальные симптомы и особенности остеосаркомы и саркомы Юинга. J Bone Joint Surg Am. 2000; 82 (5): 667-74.
Heck Jr RK. Злокачественные опухоли костей. В: Terry Canale S, Beaty JH. Оперативная ортопедия Кэмпбелла. 11 изд. Филадельфия: Мосби; 2008: 901-38.
Varunjikar MD, Jayan BE.Остеомиелит бедренной кости, имитирующий саркому овец, — описание случая. Sch J Med Case Rep.2014; 2 (2): 118-21.
Буксир BPB, Tan MH. Поздний диагноз саркомы Юинга правой плечевой кости, первоначально лечившейся как хронический остеомиелит: отчет о клиническом случае. J Orthop Surg. 2005: 13 (1): 88-92.
Metcalfea JE, Grimer RJ. Саркома Юинга стопы, маскирующаяся под остеомиелит. Euro Foot Ankle Soc. 2004 (10): 29-33.
Маккарвилл М.Б., Чен Дж.Й., Коулман Дж.Л., Ли И, Ли Х, Аддерсон Э.Е. и др. Отличить остеомиелит от саркомы Юинга с помощью рентгенографии и МРТ.AJR Am J Roentgenol 2015; 205 (3): 640-51.
Funk SS, Copley LAB. Острый гематогенный остеомиелит у детей: патогенез, диагностика и лечение. Orthop Clin N Am. 2017; 48: 199-208.
Шимосе С., Сугита Т., Кубо Т., Мацуо Т., Нобуто Х., Очи М.: Дифференциальный диагноз между остеомиелитом и опухолями костей. Acta Radiol. 2008 (49): 928-33.
Хуан П.Й., Ву П.К., Чен С.Ф., Ли Ф.Т., Ву Х.Т., Лю С.Л. и др. Остеомиелит бедренной кости, имитирующий опухоль кости: обзор 10 случаев. Мир J Surg Oncol.2013 (11): 283-91.
Lyall HA, Constant CR, Wraight EP. История болезни: саркома Юинга в дистальном метафизе большеберцовой кости, имитирующая остеомиелит. Clin Radiol. 1993 (48): 140-42.
Коттиас П., Томено Б., Анракт П., Винь Т.С., Форест М. Подострый остеомиелит, проявляющийся в виде опухоли кости. Обзор 21 случая. Int Ortho. 1997 (21): 243-8.
Dich VQ, Нельсон JD, Haltalin KC. Остеомиелит у младенцев и детей: обзор 163 случаев. Am J Dis Child. 1975; (129): 1273-8.
Детский остеомиелит: история вопроса, патофизиология, эпидемиология
Hollmig ST, Copley LA, Browne RH, Grande LM, Wilson PL.Тромбоз глубоких вен, связанный с остеомиелитом у детей. J Bone Joint Surg Am . 2007 июль 89 (7): 1517-23. [Медлайн].
Nourse C, Starr M, Munckhof W. Внебольничный устойчивый к метициллину Staphylococcus aureus вызывает тяжелую диссеминированную инфекцию и тромбоз глубоких вен у детей: обзор литературы и рекомендации по ведению. J Детский педиатр . 2007 Октябрь 43 (10): 656-61. [Медлайн].
Бельтур М.В., Бирчанский С.Б., Вердуго А.А., Мейсон Е.О. младший, Халтен К.Г., Каплан С.Л. и др.Патологические переломы у детей с острым остеомиелитом, вызванным Staphylococcus aureus. J Bone Joint Surg Am . 2012 г. 4 января. 94 (1): 34-42. [Медлайн].
Bouchoucha S, Benghachame F, Trifa M, Saied W., Douira W., Nessib MN, et al. Тромбоз глубоких вен, связанный с острым гематогенным остеомиелитом у детей. Orthop Traumatol Surg Res . 2010 декабрь 96 (8): 890-3. [Медлайн].
Окубо Т., Ябэ С., Оцука Т., Такидзава И., Такано Т., Дохма С. и др.Мультифокальные абсцессы таза и остеомиелит, вызванные внебольничным метициллин-резистентным золотистым стафилококком у 17-летнего баскетболиста. Диагностика Microbiol Infect Dis . 2008 Март 60 (3): 313-8. [Медлайн].
Sdougkos G, Chini V, Papanastasiou DA, Christodoulou G, Tagaris G, Dimitracopoulos G. Метициллин-резистентный золотистый стафилококк, продуцирующий лейкоцидин Пантона-Валентайна, как причина острого остеомиелита у детей. Clin Microbiol Infect .2007 июн.13 (6): 651-4. [Медлайн].
Hawkshead JJ 3rd, Patel NB, Steele RW, Heinrich SD. Сравнительная тяжесть детского остеомиелита, обусловленного устойчивостью к метициллину, по сравнению с чувствительным к метициллину Staphylococcus aureus. J Педиатр Ортоп . 2009 Янв-Фев. 29 (1): 85-90. [Медлайн].
Рэнсон М. Визуализация детской скелетно-мышечной инфекции. Семин Musculoskelet Radiol . 2009 Сентябрь 13 (3): 277-99. [Медлайн].
Schallert KE, Kan HJ, Monsalve J, et al. Метафизарный остеомиелит у детей: как часто подтвержденный МРТ выпот из суставов или эпифизарный отек указывают на сосуществующий септический артрит? Педиатр Радиол . 2015 июл. 45 (8): 1174-81. [Медлайн].
Шмит П., Глорион С. Остеомиелит у младенцев и детей. евро Радиол . 2004, 14 марта, приложение 4: L44-54. [Медлайн].
Blickman JG, van Die CE, de Rooy JW.Современные концепции визуализации при детском остеомиелите. евро Радиол . 2004 14 марта, приложение 4: L55-64. [Медлайн].
McNeil JC, Forbes AR, Vallejo JG и др. Роль посевов под контролем оперативной или интервенционной радиологии при остеомиелите. Педиатрия . Май 2016. 137 (5):
Mader JT, Shirtliff M, Calhoun JH. Стадия и применение при остеомиелите. Clin Infect Dis . 1997 25 декабря (6): 1303-9. [Медлайн].
Chiappini E, Conti C, Galli L, de Martino M. Клиническая эффективность и переносимость линезолида у педиатрических пациентов: систематический обзор. Clin Ther . 2010 января, 32 (1): 66-88. [Медлайн].
Заутис Т., Локалио А.Р., Лекерман К., Сэдлмайр С., Бертох Д., Керен Р. Длительная внутривенная терапия по сравнению с ранним переходом на пероральную антимикробную терапию острого остеомиелита у детей. Педиатрия . 2009 Февраль 123 (2): 636-42.[Медлайн].
Peltola H, Pääkkönen M, Kallio P, Kallio MJ. Краткосрочное и долгосрочное противомикробное лечение острого гематогенного остеомиелита в детском возрасте: проспективное рандомизированное исследование 131 случая с положительным посевом. Pediatr Infect Dis J . 2010 29 декабря (12): 1123-8. [Медлайн].
Лю С., Байер А., Косгроув С.Е., Даум Р.С., Фридкин С.К., Горвиц Р.Дж. и др. Руководство по клинической практике Американского общества инфекционистов по лечению метициллин-резистентных инфекций Staphylococcus aureus у взрослых и детей: резюме. Clin Infect Dis . 2011 г. 1. 52 (3): 285-92. [Медлайн].
Бачур Р., Пагон З. Успех короткого курса парентеральной антибактериальной терапии острого остеомиелита у детей. Clin Pediatr (Phila) . 2007 Январь 46 (1): 30-5. [Медлайн].
Jacobs RF, Adelman L, Sack CM, Wilson CB. Лечение остеохондрита Pseudomonas, осложняющего колотые ранения стопы. Педиатрия . 1982 Апрель, 69 (4): 432-5. [Медлайн].
Озбек З., Макай Б., Унсал Е., Дурак И., Гунес Д., Анальный О. Поражение конъюнктивы при хроническом рецидивирующем мультифокальном остеомиелите. Роговица . 2008 27 января (1): 117-9. [Медлайн].
Catalano-Pons C, Raymond J, Chalumeau M, Armengaud JB, Kalifa G, Gendrel D. Случай 2: детский хронический остеомиелит: отчет о двух случаях. Диагноз случай 1: туберкулез легких, осложненный пневмомедиастинумом. Случай 2, диагноз: остеомиелит, вызванный актиномицетами. Acta Paediatr . 2007 декабрь 96 (12): 1849-52. [Медлайн].
Асенси В., Альварес В., Валле Е. и др. Полиморфизм промотора IL-1альфа (-889) является фактором риска развития остеомиелита. Am J Med Genet . 1 июня 2003 г. 119A (2): 132-6. [Медлайн].
Auh JS, Binns HJ, Katz BZ. Ретроспективная оценка подострого или хронического остеомиелита у детей и молодых людей. Clin Pediatr (Phila) . 2004 июль-авг. 43 (6): 549-55.[Медлайн].
Брэдли Дж.С., Каплан С.Л., Тан Т.К. и др. Пневмококковые инфекции костей и суставов у детей. Группа по изучению педиатрического многоцентрового надзора за пневмококками (PMPSSG). Педиатрия . 1998 декабрь 102 (6): 1376-82. [Медлайн].
Бернетт М.В., Басс Дж. У., Кук Б.А. Этиология остеомиелита, осложняющего серповидно-клеточную анемию. Педиатрия . 1998 Февраль 101 (2): 296-7. [Медлайн].
Кушинг А.Х.Дискит у детей. Clin Infect Dis . 1993 июл.17 (1): 1-6. [Медлайн].
Дартнелл Дж, Рамачандран М., Катчбуриан М. Гематогенный острый и подострый детский остеомиелит: систематический обзор литературы. J Bone Joint Surg Br . 2012 май. 94 (5): 584-95. [Медлайн].
Faust SN, Clark J, Pallett A, Clarke NM. Лечение инфекций костей и суставов у детей. Arch Dis Детский . 2012 июн.97 (6): 545-53.[Медлайн].
Фишер РГ. Неонатальный остеомиелит. NeoReviews . Июль 2011. 12 (7): e374-e380.
Gallagher KT, Roberts RL, MacFarlane JA, Stiehm ER. Лечение хронического рецидивирующего мультифокального остеомиелита интерфероном гамма. J Педиатр . 1997 сентябрь 131 (3): 470-2. [Медлайн].
Гутьеррес К. Инфекции костей и суставов у детей. Педиатрическая клиника North Am . 2005 июн. 52 (3): 779-94, vi.[Медлайн].
Herigon JC, Hersh AL, Gerber JS, Zaoutis TE, Newland JG. Лечение антибиотиками инфекций Staphylococcus aureus в детских больницах США, 1999-2008 гг. Педиатрия . 2010 июн. 125 (6): e1294-300. [Медлайн].
Каплан SL. Остеомиелит у детей. Инфекция Dis Clin North Am . 2005 декабря 19 (4): 787-97, vii. [Медлайн].
Klein JD, Leach KA. Детский тазовый остеомиелит. Clin Pediatr (Phila) . 2007 ноябрь 46 (9): 787-90. [Медлайн].
Кохли Р., Хэдли С. Грибковый артрит и остеомиелит. Инфекция Dis Clin North Am . 2005 декабря 19 (4): 831-51. [Медлайн].
Лев Д.П., Вальдфогель Ф.А. Остеомиелит. N Engl J Med . 1997 г., 3. 336 (14): 999-1007. [Медлайн].
Пяакконен М., Каллио П.Е., Каллио М.Дж., Пелтола Х. Лечение костно-суставных инфекций, вызванных золотистым стафилококком, аналогично лечению других этиологий: анализ 199 стафилококковых инфекций костей и суставов. Pediatr Infect Dis J . 2012 май. 31 (5): 436-8. [Медлайн].
Раз Р., Мирон Д. Ципрофлоксацин для перорального применения для лечения инфекций после колотых ран ногтя. Clin Infect Dis . 1995 21 июля (1): 194-5. [Медлайн].
Schauwecker DS, Braunstein EM, Wheat LJ. Диагностическая визуализация остеомиелита. Инфекция Dis Clin North Am . 1990 Сентябрь 4 (3): 441-63. [Медлайн].
Scott RJ, Christofersen MR, Robertson WW Jr, et al.Острый остеомиелит у детей: обзор 116 случаев. J Педиатр Ортоп . 1990 сентябрь-октябрь. 10 (5): 649-52. [Медлайн].
Тейлор М.Н., Чаудхури Р., Дэвис Дж., Новелли В., Джасвон М.С. Детский остеомиелит в виде патологического перелома. Клин Радиол . Март 2008 г., 63 (3): 348-51. [Медлайн].
Thomsen I, Creech CB. Достижения в диагностике и лечении детского остеомиелита. Curr Infect Dis Rep .2011 Октябрь 13 (5): 451-60. [Медлайн].
Unkila-Kallio L, Kallio MJ, Eskola J. Сывороточный С-реактивный белок, скорость оседания эритроцитов и количество лейкоцитов при остром гематогенном остеомиелите у детей. Педиатрия . 1994, январь 93 (1): 59-62. [Медлайн].
Вайнштейн М.П., Страттон К.В., Хоули Н.Б. и др. Многоцентровая совместная оценка стандартизированного сывороточного бактерицидного теста в качестве предиктора терапевтической эффективности при остром и хроническом остеомиелите. Am J Med . 1987 августа 83 (2): 218-22. [Медлайн].
Wong M, Isaacs D, Howman-Giles R, Uren R. Клинические и диагностические особенности остеомиелита, возникающего в первые три месяца жизни. Pediatr Infect Dis J . 1995 г., 14 (12): 1047-53. [Медлайн].
Справочная информация: Хирургическое лечение хронического остеомиелита у детей все еще остается сложной задачей в развивающихся странах.Это исследование проанализировало степень заболевания и терапевтический режим. Объекты и методы: Это ретроспективное исследование, проведенное в двух больницах первичной медико-санитарной помощи с января 2009 г. по декабрь 2013 г., 27 детей (20 мужчин и 7 женщин, средний возраст 7 лет), поступивших из развивающихся стран и лечившихся от хронического остеомиелита. Сообщается локализация, продолжительность заболевания, степень поражения костей, спектр микробов, количество предыдущих и необходимых хирургических процедур и продолжительность пребывания в больнице. Результаты: Всего 16 случаев имели гематогенную и 11 случаев посттравматическую этиологию. Средняя продолжительность заболевания составила 18 месяцев. В среднем было выполнено три предыдущих хирургических вмешательства (от 1 до 12). Пораженными костями были: большеберцовая кость в 11, бедренная кость в 8, предплечье в 6 случаях, позвоночник и плечевая кость в 1 случае. Staphylococcus aureus был ответственным микробом в 75%. В среднем требовалось четыре (от 2 до 8) хирургических вмешательств. Костная стабилизация потребовалась 17, пластическая реконструкция мягких тканей — 8.В трех случаях с метафизарным / диафизарным дефектом необходимо было выполнить перенос костей (2 × малоберцовая кость-протибия, 1 × ребро для лучевой кости). Средняя продолжительность госпитализации составила 8 (от 4 до 20) недель. За 3 месяца произошло три местных рецидива, все излечимы хирургическим путем. Выводы: Хирургическое лечение хронического остеомиелита у детей требует радикального удаления раны. Знание различных пластических и хирургических процедур необходимо для восстановления дефектов костей и / или мягких тканей. Ключевые слова: Детство, хронический, развивающаяся страна, остеомиелит
В отличие от промышленно развитых стран, хронический остеомиелит гораздо чаще встречается в развивающихся странах. [1], [2], [3], [4], [5], [6], [7] Годовая распространенность остеомиелита среди населения Кении составляет около 1: 1000. [3] Сообщается, что хронический остеомиелит является серьезным бременем для здравоохранения во многих развивающихся странах. В Гамбии, например, на остеомиелит приходилось 7,8% случаев госпитализации детей в хирургические отделения и 15,4% дней пребывания в стационаре. [8] Из-за образа жизни, традиций и социального положения остеомиелит играет важную роль в развивающихся странах. [8], [9], [10] В промышленно развитых странах посттравматический остеомиелит играет незначительную роль у детей, в отличие от взрослых. Однако в развивающихся странах тяжелые проявления посттравматического остеомиелита должны отмечаться все чаще. Из-за зачастую недостаточной медицинской помощи, особенно в сельской местности, и отсутствия надлежащего питания, хронический остеомиелит с длительным анамнезом и отчетливыми симптомами может быть результатом даже после незначительных травм. [3], [8], [11], [12], [13], [14] Следовательно, хронический остеомиелит требует междисциплинарной концепции лечения системных и / или местных антибиотиков и хирургических ортопедических процедур. Необходимы радикальная хирургическая обработка раны и секвестрэктомия. Также могут быть показаны различные пластико-реконструктивные процедуры костей и мягких тканей. Из-за отсутствия адекватных ресурсов и специалистов эту междисциплинарную концепцию лечения очень трудно реализовать в развивающихся странах. Нам нравится сообщать о нашем опыте лечения хронического остеомиелита у детей из развивающихся стран, переведенных и госпитализированных в нашу больницу немецкой организацией помощи «Friedensdorf International» (Деревня международного мира).
С января 2009 года по декабрь 2013 года 27 детей (20 мужчин и 7 женщин), поступивших из развивающихся стран, прошли лечение в двух соседних больницах от хронического остеомиелита.Всего 17 детей приехали из Анголы, 10 — из Афганистана. Трансфер детей организовала немецкая благотворительная организация Friedensdorf International Oberhausen. Обе больницы являются больницами первичного звена здравоохранения, в одной из них есть травматологический центр II уровня. Организация по оказанию помощи «Friedensdorf International Oberhausen» продвигает в первую очередь проекты в развивающихся странах Анголы и Афганистана. Решение о транспортировке в Германию было принято местным персоналом гуманитарной организации в развивающейся стране — исключительно на основе социальных аспектов; отбирались только безденежные люди.Задержка между отбором и доставкой в Германию составляла в среднем 3 недели. Все дети страдали хроническим остеомиелитом (т. Е. Длительностью более 6 месяцев). Средний возраст детей на момент поступления составлял 7 лет (от 2 до 12 лет). Диагностические процедуры включают анализы крови и радиологические исследования с использованием рентгенограмм и магнитно-резонансной томографии (МРТ) в случаях, когда невозможно точно определить степень поражения костей или мягких тканей. Локализация и патогенез остеомиелита, продолжительность анамнеза, степень поражения костей, спектр патогенных микроорганизмов, если они изолированы, общее количество предыдущих хирургических вмешательств, а также тип и количество хирургических вмешательств в нашем центре. учреждение, были проанализированы. Хирургические процедуры включали санацию раны, необходимые методы стабилизации и фиксации, а также пластические реконструктивные процедуры костей и мягких тканей. Регистрировали также продолжительность пребывания в больнице, функциональное ограничение пораженных суставов и частоту рецидивов. Последующий уход длился не менее 6 месяцев, прежде чем дети смогли покинуть общежитие благотворительной организации и вернуться на родину. По истечении этого времени дальнейшее наблюдение стало возможным у 18 детей при регулярном контакте гуманитарной организации с ее местным офисом в родной стране по электронной почте или по переписке. Заявления о функциональном состоянии невозможны. Средний срок наблюдения составил 25 месяцев (от 11 до 39 месяцев). Статистические методы Никаких статистических методов для текущего исследования не требовалось.
Всего было зарегистрировано 16 случаев гематогенного остеомиелита, а посттравматический остеомиелит в результате открытого перелома диагностирован у 11 детей. Средняя продолжительность заболевания составляла 18 месяцев (диапазон, 11-60 месяцев), в среднем три (диапазон, 1-12) предшествующих хирургических вмешательств. Обычно использовались простые разрезы и дренирование абсцессов и санация костей.Чаще всего поражалась большеберцовая кость ( n = 12), затем бедро ( n = 7), лучевая и / или локтевая кости ( n = 6), позвоночник и плечевая кость (каждая в одном случае). . Выделения из пазух [Рис. 1] a наблюдались у всех детей. В 16 случаях — единственная пазуха; в 7 случаях необходимо было наблюдать две пазухи и в 4 случаях множественные пазухи.
На момент поступления ни у одного из детей не было температуры или лихорадки. Анализы крови первичной диагностики включали общий анализ крови, измерение С-реактивного белка (СРБ), электролитов и креатинина. Во всех случаях рентгенограммы на чистой пленке были взяты из пораженной кости [Рисунок 1] b, [Рисунок 2] a, [Рисунок 3] a, [Рисунок 4] a.МРТ была проведена в 15 случаях, когда костная протяженность остеомиелита не могла быть четко определена [Рисунок 2] b, и в тех случаях, когда предполагалось поражение суставов. Только у трех детей были выявлены повышенные воспалительные анализы крови (лейкозитоз> 12000 / мл, значение CRP> 5 IE / л).
Рентгенологические исследования выявили псевдоартроз [Рисунок 3] a у 13 детей. Отклонение оси в переднезадней или сагиттальной плоскости выявлено у восьми детей, у пяти из них перелом зажил при этом неправильном положении.Секвестры могли быть окончательно обнаружены с помощью рентгенограмм [Рис. 1] b в семи случаях и дополнительно с помощью МРТ в двух случаях. Поражение суставов выявлено с помощью МРТ в двух случаях (1 коленный сустав, 1 голеностопный сустав). Во всех случаях мазки брали из сукровицы пазухи при поступлении. Были проведены дополнительные обследования на гепатит, ВИЧ и туберкулез. Staphylococcus aureus как ответственный микроб может быть обнаружен в 20 случаях (74%), из которых два могут быть идентифицированы как устойчивые к метициллину S. золотистый (MRSA). Следующими выявленными патогенными микроорганизмами были: гемолитический стрептококк в 14 случаях (54%) и грамотрицательные микробы ( Enterobacter , Proteus , Pseudomonas , Escherichia coli ) в семи случаях (26%). Четырнадцать случаев (52%) были полимикробными; посевы были отрицательными у четырех пациентов (15%). Не было заметной корреляции между обнаруженными микробами и пораженными костями. Ампициллин в комбинации с сульбактамом был назначен для первичного внутривенного лечения антибиотиками.При необходимости препарат адаптировали с учетом устойчивости выделенного микроорганизма. Линезолид использовался в случаях обнаружения MRSA до тех пор, пока обмен не стал отрицательным после хирургического лечения. Средний период внутривенного лечения антибиотиками составлял 7 дней (диапазон от 3 до 12 дней). После этого антибиотик вводили перорально в течение 6 недель. Девятнадцать из 23 детей, у которых можно было идентифицировать микроорганизм, получали клиндамицин как чувствительный антибиотик. Было выполнено несколько хирургических процедур, в среднем 4 (диапазон, 2-8) процедур на пациента.Первичная процедура заключалась в очистке пазухи и пораженной кости у девяти пациентов с дополнительным удалением секвестров, в среднем на третий (диапазон, 1-6) день госпитализации. При псевдоартрозе края костей были освежены, и для стабилизации использовался внешний фиксатор [Рисунок 3] b и c. Пазухи и полости мягких тканей лечили с помощью системы закрытия с помощью вакуума (VAC). Повязки меняли каждые 3-4 дня в зависимости от результата микробиологического мазка.Каждый пациент прошел в среднем три (1-7) процедуры VAC, прежде чем реконструкция мягких тканей и / или кости стала возможной. Отрицательные результаты микробиологических мазков, нормальные анализы крови и наличие хорошо васкуляризованной грануляционной ткани были постулированы как требования, позволяющие окончательно закрыть рану. У 17 пациентов стабилизация кости должна была быть выполнена из-за псевдоартроза или из-за заживления перелома при неправильном положении [Рисунок 3] a. Двум детям потребовался артродез при поражении соседнего сустава (1 голеностопный, 1 коленный). Трансплантация кости была необходима трем детям в случае диафизарного или метафизарного дефекта полной толщины кости [Рисунок 4] a. Средняя длина костного дефекта составила 5 см (диапазон 4-6 см). Контралатеральная малоберцовая кость была использована у двух детей для реконструкции диафизарного дефекта большеберцовой кости [Рисунок 4] b и c. Дистальный диафизарный дефект лучевой кости у девочки 2 лет восстановлен с использованием ребра в качестве костного трансплантата. В каждом случае костные трансплантаты фиксировали винтами [рис. 4] b и c. У 12-летней девочки обнаружено укорочение левой бедренной кости на 10 см; Лечилась методом Илизарова дистракционного остеогенеза костной мозоли. В 17 случаях раны закрывались простыми вторичными швами. Девяти пациентам потребовались различные пластико-реконструктивные процедуры для закрытия дефекта мягких тканей. Местные мышечные лоскуты использовались у пяти пациентов (1 × бедро, 4 × голень), а местных кожных лоскутов было достаточно у четырех пациентов, трансплантация кожи разделенной толщины была выполнена в 10 случаях. Продолжительность пребывания в больнице варьировалась от 4 до 26 недель (в среднем 8 недель). Незапланированная хирургическая ревизия потребовалась восьми детям из-за гематомы или стойкого секрета раны. Одной ревизии, включая чистку, местную хирургическую обработку раны и дренирование, было достаточно у четырех детей. Остальным четырем детям еще раз была проведена ВАК-система, которую нужно было повторить в среднем 2 раза (от 1 до 4 раз), пока не стало возможным вторичное закрытие раны. Трое детей получили переливание крови, каждому из них по две единицы эритроцитов, когда уровень гемоглобина был <6 г / л. Дальнейших осложнений во время пребывания в больнице не наблюдалось. После этого все дети остались в Германии еще на 6 месяцев; Их поселили в общежитии «Friedensdorf International Oberhausen». В этот период трое детей поступили с локальным рецидивом остеомиелита (1 голень, 2 бедра). Во всех трех случаях потребовалось повторное хирургическое вмешательство. Во всех случаях можно было добиться окончательного заживления раны с помощью местной обработки раны и двукратного VAC. После окончательного закрытия раны пероральное лечение адаптированными к бактериям антибиотиками продолжалось в течение 6 недель. В общей сложности 15 детей, которым был установлен внешний фиксатор для стабилизации кости, были повторно госпитализированы для удаления имплантата в среднем через 13 недель (диапазон, 10–18 недель), прежде чем они могли уехать в свою страну. Статус других детей был проверен по телефону или электронной почте в гуманитарную организацию. В дальнейшем рецидивов не было. Функциональные ограничения наблюдались у 13 детей (48%). У шести детей (22%) разница в длине ног составила> 2 см, которую пришлось компенсировать балансировкой подошвы.Пришлось выполнить сращивание коленного и голеностопного суставов, каждое в одном случае. Кроме того, у четырех детей были замечены значительные ограничения функций. У двоих детей из-за рубцевания кожи и мышц сгибание коленного сустава составляло всего до 30 °. Диапазон движений в локтевом суставе был ограничен до 0 ° / 60 ° / 90 ° относительно разгибания и сгибания у одного ребенка с вовлечением дистального отдела плечевой кости и проксимального отдела локтевой кости. У 2-летней девочки с диафизарным дефектом лучевой кости и последующим замещением кости развилось радиальное отведение лучезапястного сустава.Диапазон движений лучезапястного сустава составлял 20 ° / 0 ° / 10 ° относительно разгибания и сгибания. Однако вращение предплечья не ограничивалось. Дальнейший рецидив остеомиелита можно было исключить у 18 детей, регулярно обращаясь по электронной почте в местный офис организации помощи в стране детского дома. Таким образом, средний срок наблюдения 24 месяца (диапазон 11–39 месяцев) был возможен. В двух случаях простые рентгеновские снимки пораженной кости были отправлены через 12 и 14 месяцев соответственно [Рисунок 3] d, но информация о функциональном статусе, возможных несоответствиях длины ног или отклонениях оси была невозможна.
Хронический остеомиелит является следствием либо гематогенного остеомиелита, либо осложненного течения открытой травмы, то есть посттравматического остеомиелита. Хронический остеомиелит у детей редко встречается в промышленно развитых странах. Однако в развивающихся странах это заболевание встречается гораздо чаще. [3], [4], [5], [6], [7] Сообщается, что бремя хронического остеомиелита в развивающихся странах является существенным. [8], [9], [10] Так, например, в Уганде 35% всех хирургических процедур были выполнены из-за диагноза остеомиелит в 2010 году. Треть этих пациентов составляли дети в возрасте от 10 до 14 лет. [9] Причинно-следственной связью считается зачастую недостаточная медицинская помощь, особенно в сельской местности. Таким образом, незначительные травмы или открытые переломы могут привести к хроническому остеомиелиту. В противном случае гематогенный остеомиелит может проявиться как хронический из-за отсутствия последующего лечения антибиотиками. [3], [4] В то время как у детей посттравматический остеомиелит считается крайней редкостью в промышленно развитых странах, его доля хронических проявлений в развивающихся странах составляет 40-60%. [3], [4], [5], [6] В нашей серии исследований мы наблюдали посттравматический хронический остеомиелит в 11 из 27 случаев (40%). В развивающихся странах необходимо наблюдать отчетливые стадии болезни из-за задержки начала последующего лечения.Таким образом, Onche и Obiamo [4] сообщили о среднем интервале в 13 месяцев между появлением симптомов остеомиелита и началом последующего лечения в больнице в Нигерии. Помимо рентгенограмм с простой пленкой для определения секвестра или новообразования надкостницы (обертка) [Рис. 1] b МРТ считается подходящей для определения точной степени остеомиелита в костномозговом канале и поражения мягких тканей. [1], [2], [3] Сонографические и сцинтиграфические исследования не имеют значения для диагностики хронического остеомиелита, [11] актуальны при остром гематогенном остеомиелите. Существуют разные системы классификации. Классификация Waldvogel [6] ориентирована на продолжительность и этиологию остеомиелита, но в клинической практике это не имеет большого значения. Две общепринятые системы классификации — это системы по Сиерни-Мадеру и Солагберу. Классификация Cierny-Mader делит на четыре стадии в зависимости от глубины и протяженности остеомиелита. [6], [13] Пять этапов классификации Solagberu специфичны для развивающихся стран и основаны на хронологическом течении болезни.Но обе классификации соответствуют взрослой кости. Недавно опубликованная классификация согласно Jones et al . [8] учитывает инфантильное состояние кости. Различают три типа остеомиелита: тип A — абсцесс, тип B — секвестр или обертка и тип C — склеротический. Мы считаем данную классификацию наиболее обоснованной для выбора адекватного хирургического лечения. Согласно обзору литературы, большеберцовая и бедренная кость считается пораженной костью примерно в 80% всех случаев, таким образом, это наиболее часто поражаемые локализации. [1], [2], [7], [8] В нашей серии эти локализации наблюдались в двух третях случаев. Часто наблюдаемое метафизное поражение остеомиелита у детей можно объяснить сниженной скоростью кровотока и отсутствием ретикулоэндотелиальных клеток в этой области детской кости. [2] Staphylococcus aureus считается наиболее частым возбудителем остеомиелита как в развивающихся, так и в промышленно развитых странах, с частотой 70-80% всех обнаруженных микроорганизмов. [1], [2], [6], [7], [11], [12], [13], [14] В нашей серии мы обнаружили этот росток в 75% случаев. Существуют разные данные о возникновении устойчивости к метициллину в развивающихся странах. Большинство авторов сообщают о значительно более низком уровне сопротивления в развивающихся странах по сравнению с промышленно развитыми странами. [5], [12], [13] Однако, Mantero et al. al . [3] сообщает о 48% устойчивости к метициллину в случаях обнаружения S. aureus в Кении. В нашей серии мы наблюдали устойчивость к метициллину в двух из 20 (10%) подтверждений S. aureus . В литературе существуют разные утверждения о сроках необходимого лечения антибиотиками. [1], [2], [11], [12] Однако в большинстве случаев рекомендуется внутривенное введение в течение 1 недели с последующим пероральным введением в течение 4-6 недель, в литературе нет доказательных утверждений относительно более длительное лечение антибиотиками. [14] В случаях доказанной чувствительности предпочтение отдается клиндамицину из-за его хорошей биодоступности и способности адекватно проникать в кости. [1], [14] В случае отрицательных посевов рекомендуются антибиотики, чувствительные к стафилококку, поскольку он часто встречается. В развивающихся странах необходимо принимать во внимание потенциальный риск туберкулеза костей, если необходимо длительное лечение туберкулеза. Однако основным краеугольным камнем лечения хронического остеомиелита в детстве является адекватная хирургическая обработка раны.Эксклюзивного лечения антибиотиками будет недостаточно, особенно в случае образования секвестров. [1], [2], [14] Уже Лаутенбах [15], [16] сообщил о своей хирургической технике орошения и отсасывания для лечения хронического остеомиелита. Папино и и . [17] представили свою двухэтапную процедуру, состоящую из местной хирургической обработки, орошения и вторичного губчатого костного трансплантата. Но доказано, что струйная жидкость течет по пути наименьшего сопротивления (так называемый «эффект шоссе»).Следовательно, это больше не кажется уместным. [1] Показан при острой стадии флегмоны костномозгового канала. Однако в случае хронического остеомиелита наиболее важной и эффективной процедурой остается адекватная хирургическая обработка раны. [1], [2] Образовавшийся костный дефект требует соответствующего замещения и достаточной стабилизации в зависимости от степени, локализации и периостального кровоснабжения. В некоторых случаях достаточно образования новой кости (обертки). Если костный дефект меньше 2 см и хорошее кровоснабжение надкостницы сохраняется, целесообразным считается применение губчатого костного трансплантата. В случаях более крупных дефектов и дефектов на всю толщину [Рис. 4] a, описанный Илизаровым остеогенез дистракции [18] или одностадийный перенос малоберцовой кости на большеберцовую кость [19] сообщается для возможного перекрытия дефекта. Метод Илизарова требует много времени; он требует от пациента высокой комплаентности и связан с высоким процентом осложнений.Однако костное кровоснабжение улучшится после процедуры отвлечения внимания. Таким образом, в большинстве случаев остеомиелит можно вылечить. [18] Считается, что оба метода, дистракционный остеогенез и перенос малоберцовой кости на большеберцовую кость, позволяют достичь сравнимых функциональных результатов. [1] В двух случаях диафизарного дефекта большеберцовой кости мы выбрали перенос малоберцовой кости из-за сокращенного периода лечения. При дефектах бедренной кости перенос малоберцовой кости считается недостаточно несущим. [1] В этой локализации предпочтение отдается методу Илизарова. Когда образовалось достаточное количество новой костной ткани и сохранилось хорошее кровоснабжение надкостницы, можно обойтись без замены кости [Рис. 1] b. Помимо реконструкции кости, особое значение имеет покрытие мягких тканей, особенно когда дефект находится на голени. У трети наших пациентов потребовались различные пластические реконструктивные процедуры для закрытия дефекта мягких тканей.Обычно используются местные кожно-фасциальные и мышечные лоскуты. В литературе существует лишь несколько сообщений об использовании системы VAC в концепции хирургического лечения остеомиелита. [20] Собственный опыт обнадеживает, особенно в отношении кондиционирования мягких тканей. Отрицательное давление на поверхности ран способствует удалению жидкости и увеличивает образование грануляционной ткани. Сообщается, что частота рецидивов после предполагаемого хирургического лечения остеомиелита составляет 10-30%. [1], [2] В нашем исследовании местный рецидив, требующий повторной хирургической обработки раны, должен был наблюдаться у трех из 27 пациентов (11%) в течение 3 месяцев после выписки. Утверждения о частоте функциональных ограничений пораженных суставов и соответствующих различиях в длине ног различаются и составляют от 2% до 30% после излечения остеомиелита. Мы наблюдали расхождение в длине ног более 2 см у 6 из 27 детей (22%). У четырех детей (14,8%) развились соответствующие, но хорошо компенсируемые ограничения объема движений в коленном или локтевом суставе.
Клиническая картина хронического остеомиелита у детей из развивающихся стран характеризуется затяжным течением и более запущенными стадиями заболевания. Радикальная обработка костной ткани — важнейший аспект лечения. В зависимости от размера и локализации дефекта, а также возможного сохраненного кровоснабжения в сочетании с образованием новой кости могут потребоваться различные реконструктивные процедуры и стабилизация кости.Знание различных пластических реконструктивных процедур для достижения адекватного покрытия мягких тканей является обязательным. Система VAC может сыграть решающую роль.
Все данные исследования были одобрены местным комитетом по этике; ответственная организация помощи дала свое информированное согласие на всех детей до их включения в исследование.
Источник поддержки: Нет, 081 8 907 907 907 907 907 908 Чек |
DOI: 10.4103 / 0189-6725.143133
[Рисунок 1], [Рисунок 2], [Рисунок 3], [Рисунок 4].

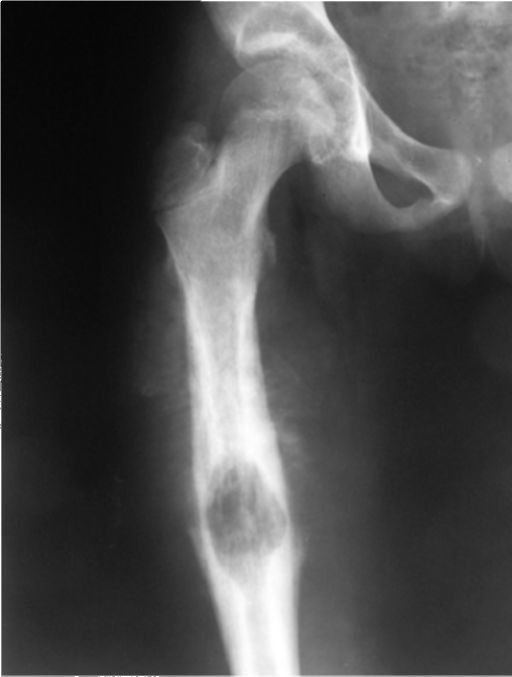 С помощью рентгена можно выявить болезнь на ранних стадиях. По мере роста воспаления изменяется характер изображения на снимках, поэтому время протекания болезни можно обозначить с высокой точностью.
С помощью рентгена можно выявить болезнь на ранних стадиях. По мере роста воспаления изменяется характер изображения на снимках, поэтому время протекания болезни можно обозначить с высокой точностью.