Памятка по профилактике внебольничной пневмонии
Внебольничная пневмония — — это острое заболевание, возникшее вне стационара илидиагностированное в первые 2 суток от момента госпитализации. Острой пневмонией(воспалением легких) называют инфекционное заболевание, при котором ввоспалительный процесс вовлекаются легкие. В тяжелых случаях пневмония можетпривести к летальному исходу. Внебольничная пневмония является достаточнораспространенным заболеванием в нашей стране. За последние 2 года наблюдается ростколичества заболеваний. Обычно внебольничные пневмонии развиваются в периодподъема заболеваемости ОРВИ и гриппом, но как видно заболеваемость можетрегистрироваться в любое время года, даже летом.
Основная группа микроорганизмов, способных вызвать внебольничные пневмонии:пневмококк, гемофильная палочка, клебсиелла, хламидия, микоплазма, легионелла,респираторные вирусы.
Некоторые возбудители имеют свои особенности в плане источников заражения илитечения заболевания.
Источником инфекции является больной человек с признаками инфекции дыхательныхпутей, а так же люди с бессимптомным течением инфекции, без клинических симптомовзаболевания.
Основной путь передачи – воздушно-капельный (при чихании, кашле, разговоре,дыхании). Источником заражения при хламидийной пневмонии может быть птица(попугаи, куры, утки). Легионелла может «проживать» в кондиционерах принеправильном уходе за ними. Микоплазмоз дыхательных путей – инфекционноезаболевание, вызывающееся микробом, распространяющимся в коллективах при тесномконтакте с больным человеком. Нередко микоплазма вызывает пневмонию, сходную потечению с гриппом. Беспокоит сухой кашель, повышение температуры, одышка.
В типичных случаях острая пневмония проявляется следующими симптомами: повышениетемпературы тела, озноб, кашель, который сначала может быть сухим, а потом статьвлажным с отделением мокроты, одышка – ощущение затруднения при дыхании, боли вгрудной клетке. Также больного могут беспокоить общие симптомы, особенно притяжелых случаях: резкая слабость, отсутствие аппетита.
Также больного могут беспокоить общие симптомы, особенно притяжелых случаях: резкая слабость, отсутствие аппетита.
К сожалению, из-за особенностей самих микроорганизмов, а также и по причинебезграмотного и неправильного бесконтрольного применения антибиотиков, например,при острых вирусных респираторных заболеваниях (ОРВИ или ОРЗ), многие бактерииприобретают устойчивость к ряду антибиотиков. Лечение назначает только врач.
При пневмонии, вызванной «атипичным возбудителем» может отсутствовать лихорадка,общее состояние может быть нетяжелым, но проявления легочной недостаточности –одышка, усиление сердцебиения, слабость, снижение аппетита должны насторожитьзаболевшего.
Основные рекомендации по профилактике пневмонии. Здесь очень важную роль играет предупреждение респираторных вирусных инфекций:
- Соблюдайте гигиену рук. Мойте руки водой с мылом как можно чаще, особенно после кашля или чихания. Также эффективными являются средства для обработки рук на основе спирта.

- Прикрывайте рот и нос бумажной салфеткой во время кашля или чихания, а не руками.
- Необходимо вести здоровый образ жизни: заниматься физкультурой и спортом, совершать частые прогулки на свежем воздухе. Очень важно не курить в помещении, где могут находиться люди: пассивное курение пагубно сказывается на функции бронхов и иммунитете.
- Необходимо здоровое полноценное питание с достаточным содержанием белков, микроэлементов и витаминов (ежедневно в рационе должны быть свежие овощи, фрукты, мясо, рыба, молоко и молочные продукты).
- До наступления холодов и подъема заболеваемости респираторными инфекциями следует сделать прививку против гриппа, поскольку пневмония часто является осложнением гриппа. Несмотря на то, что привитые люди тоже могут болеть пневмонией, заболевание у них протекает легче, чем у не привитых.
- В холодное время года нужно одеваться по погоде, избегать переохлаждений, а в летнее — сквозняков.
- Следует соблюдать режимы проветривания и влажной уборки в помещениях.

- Как можно чаще мыть руки и промывать носовые ходы солевыми растворами (аквалор, аквамарис, квикс и др.)
- В период подъема заболеваемости гриппом рекомендуется избегать контакта с больными людьми, использовать маску для защиты органов дыхания, воздержаться от посещения мест с большим скоплением людей.
- Возможен прием иммуномодулирующих препаратов, которые можно применять только по назначению врача.
- Важно помнить, что если вы хотите оградить себя и детей от болезни, следите за своим здоровьем, ведь зачастую родители являются источником инфекции для ребенка, особенно при тех заболеваниях, которые передаются при тесном контакте (микоплазменная инфекция, стафилококк, многие вирусные инфекции).
- Если у вас дома или в учреждении, где Вы пребываете длительное время, есть кондиционер, следите за его чистотой.
- За всеми находившиеся в контакте с больными Внебольничной пневмонией устанавливается медицинское наблюдение на 21 день (осмотр, опрос, медицинское наблюдение) с момента изоляции больного.

- Всем контактным лицам назначаются лечащим врачом средства экстренной профилактики из числа противовирусных, антибактериальных, иммуномодулирующих и полиовитаминных препаратов. Для этого необходимо подойти к лечащему врачу.
Необходимо помнить: если заболели Вы или ваш ребенок, Вам необходимо не вести ребенка в сад, школу, а обратиться к врачу. При тяжелом состоянии необходимо вызвать врача на дом, и ни в коем случае не заниматься самолечением.
Здоровья Вам и Вашим близким!
Врач эпидемиолог Надырова О.Н.
Внебольничная пневмония микоплазменной этиологии | ФГБУЗ ЦМСЧ № 31 ФМБА России
Микоплазменная пневмония – заболевание из группы атипичных пневмоний. В практике пульмонолога частота микоплазменных пневмоний составляет от 5 до 50% случаев внебольничных воспалений легких или около трети пневмоний небактериального происхождения.
Возбудителем является Mycoplasma pneumoniae — микроорганизм, обладающий способностью длительно существовать и паразитировать на стенках и мембранах клеток хозяина.
Защитные механизмы возбудителя обеспечивают устойчивость к некоторым антибиотикам.
Источником микоплазменных пневмоний является человек, больной микоплазмозом или здоровый носитель микробов. Заболевание передается воздушно-капельным путем.
Заболевание регистрируется в видеединичных случаев и эпидемических вспышек. Характерны сезонные колебания заболеваемости с пиком в осенне-зимний период. Микоплазменная пневмония наблюдается преимущественно у детей, подростков и молодых пациентов до 35 лет, намного реже – в среднем и зрелом возрасте.
Легочная инфекция чаще встречается в организованных коллективах с тесными контактами (в дошкольных, школьных и студенческих группах, у военнослужащих и др.), возможны семейные случаи инфекции.
Микоплазма провоцирует развитие бронхита и пневмонии у детей и взрослых. Из-за того, что симптомы болезни похожи на распространенные заболевания, выявить микоплазменную пневмонию лишь по внешним признакам невозможно. Поэтому требуются тщательная диагностика и сдача дополнительных анализов для подтверждения диагноза. В связи с тем, что течение такой пневмонии вялое и постепенное, в первую неделю болезни ее диагностика существенно затруднена. По одним клиническим симптомам такую пневмонию диагностировать крайне сложно. Помочь могут только данные о том, что в окружении имеются больные микоплазменной инфекцией. Но и в этом случае необходимо проведение рентгенографии и компьютерной томографии грудной клетки.
Поэтому требуются тщательная диагностика и сдача дополнительных анализов для подтверждения диагноза. В связи с тем, что течение такой пневмонии вялое и постепенное, в первую неделю болезни ее диагностика существенно затруднена. По одним клиническим симптомам такую пневмонию диагностировать крайне сложно. Помочь могут только данные о том, что в окружении имеются больные микоплазменной инфекцией. Но и в этом случае необходимо проведение рентгенографии и компьютерной томографии грудной клетки.
С момента попадания в организм человека M.pneumoniae до появления первых признаков заболевания проходит от 4 до 25 суток (инкубационный период).
Клинически респираторный микоплазмоз может протекать в виде назофарингита, трахеита, бронхита, атипичной пневмонии.
Для микоплазменной пневмонии характерно вялое течение со стертой клинической картиной. Течение микоплазменной пневмонии, как правило, легкое или среднетяжелое. После инкубационного периода наступает непродолжительный период (1-2 суток), в течение которого беспокоит сухость слизистых верхних дыхательных путей, першение в горле, сухой кашель, головная боль и незначительное недомогание, что часто встречается при различных респираторных инфекциях. Клиника собственно атипичной микоплазменной пневмонии характеризуется субфебрильной температурой, не поднимающейся выше 38°С, приступообразным непродуктивным кашлем, который беспокоит около 2-3 недель.
Клиника собственно атипичной микоплазменной пневмонии характеризуется субфебрильной температурой, не поднимающейся выше 38°С, приступообразным непродуктивным кашлем, который беспокоит около 2-3 недель.
При микоплазмозе, протекающем в виде острого респираторного заболевания, возникают синуситы, отиты, а при пневмонической форме болезни – плеврит, тромбофлебит и крайне редко – полиневрит, перикардит, миокардит, отек легкого, гемолитическая анемия, тромбогеморрагический синдром.
Прогноз при всех формах микоплазмозов благоприятный. В большинстве случаев болезнь заканчивается полным выздоровлением. После заболевания образуется иммунитет, но он нестойкий.
Вакцины против возбудителя микоплазменной пневмонии на данный момент не существует. Профилактика микоплазменной пневмонии аналогична профилактике других сезонных респираторных заболеваний. Во время вспышек эпидемии рекомендуется избегать людных мест или пользоваться масками. Также следует избегать контактов с больными пневмонией и другими респираторными инфекциями, часто мыть руки, проветривать помещение.
Микоплазмоз в практике акушера-гинеколога | «Медичні аспекти здоров’я жінки»
В.Ю. Прокопюк, кафедра акушерства и гинекологии №1 Харьковского национального медицинского университета Центр здоровья женщины дорожной клинической больницы, г. Харьков
В течение последних лет все больше ученых и клиницистов проявляют интерес к микоплазменной инфекции [18, 24, 35, 47]. Мнения специалистов о значимости микоплазм в структуре акушерско-гинекологической патологии различны. Одни считают их сапрофитами, обосновывая это широким распространением инфекции; другие – условно патогенными организмами, выделяя критерии необходимости лечения; третьи полагают, что лечение необходимо в любом случае. Однако все авторы признают высокое распространение этих микроорганизмов и необходимость их дальнейшего изучения.
Этиология
Первые представители класса Mollicutes (микоплазмы) были описаны в 1898 г. Nocard и Roux как возбудители атипичной плевропневмонии у крупного рогатого скота.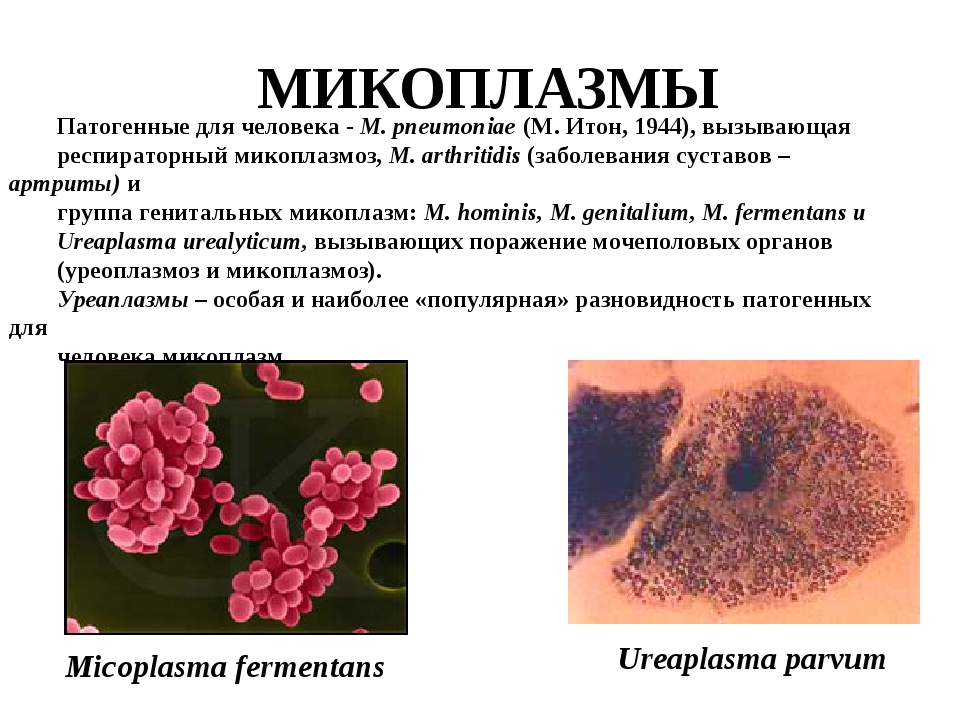 В течение длительного времени оставался открытым вопрос о принадлежности разных видов микоплазм к тому или иному классу бактерий [22]. В 1910 г. Bordet и Bordel впервые описали их морфологию, а Nowac в 1929 г. предложил для этой группы микроорганизмов название «микоплазмы». Выделение этих микроорганизмов из содержимого абсцесса большой вестибулярной железы Dienes, Edsall в 1937 г. положило начало изучению роли микоплазм в патологии мочеполовой системы человека [17, 22]. Внедрение метода ДНК-гибридизации в лабораторную практику в начале 70-х годов позволило установить, что микоплазмы являются самостоятельной группой, составляющей класс Mollicutes [43].
В течение длительного времени оставался открытым вопрос о принадлежности разных видов микоплазм к тому или иному классу бактерий [22]. В 1910 г. Bordet и Bordel впервые описали их морфологию, а Nowac в 1929 г. предложил для этой группы микроорганизмов название «микоплазмы». Выделение этих микроорганизмов из содержимого абсцесса большой вестибулярной железы Dienes, Edsall в 1937 г. положило начало изучению роли микоплазм в патологии мочеполовой системы человека [17, 22]. Внедрение метода ДНК-гибридизации в лабораторную практику в начале 70-х годов позволило установить, что микоплазмы являются самостоятельной группой, составляющей класс Mollicutes [43].
Микоплазмы, патогенные для человека, относятся к царству бактерий, типу Firmicutes, классу Mollicutes, отряду Mycoplasmatales, cемействам Mycoplasma и Ureoplasma. Всего к классу Mollicutes относятся три отряда и четыре семейства. Установлено, что человек может быть хозяином не менее 10 видов микоплазм, 5 из которых являются патогенными: M.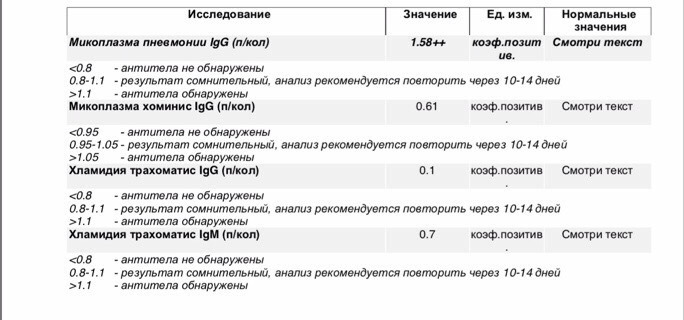 pneumonia, M. hominis, M. genitalis, M. arthritidis, M. incognitos, U. urealiticum. В акушерстве и гинекологии важное значение придается только M. hominis, M. genitalis и U. urealiticum [11, 19, 25].
pneumonia, M. hominis, M. genitalis, M. arthritidis, M. incognitos, U. urealiticum. В акушерстве и гинекологии важное значение придается только M. hominis, M. genitalis и U. urealiticum [11, 19, 25].
Микоплазмы – микроорганизмы, не имеющие клеточной стенки (по причине неспособности синтезировать мурамовую и диаминопимелиновую кислоты), отделенные трехслойной мембраной. Имея размер 150-200 нм, микоплазмы проходят через бактериальные фильтры и являются наименьшими микроорганизмами, которые могут реплицироваться на бесклеточных средах. В своем составе имеют нуклеоид, наименьший среди самореплицирующихся клеток, а также рибосомы, набор ферментов. Микоплазмы могут быть паразитами рыб, земноводных, птиц, млекопитающих и чувствительны к специфическим вирусам, плазмидам [11, 16, 25].
К культуральным особенностям микоплазм относится требовательность к питательным средам, так как они не могут самостоятельно синтезировать все необходимые им вещества, но способны ферментировать углеводы, протеины, фосфолипиды.
На плотных питательных средах микоплазмы образуют колонии в виде яичницы-глазуньи, с плотным центром и ажурной периферией. Рост колоний ингибируется тетрациклинами, макролидами; из-за отсутствия клеточной стенки микоплазмы нечувствительны к β-лактамам [17, 19].
Патогенез
К факторам патогенности микоплазм относят адгезины, эндо- и экзотоксины, гемолизины, ферменты, продукты метаболизма [16, 19].
Адгезины обеспечивают характерную особенность патогенеза микоплазм – мембранный паразитизм с длительной персистенцией на клеточной мембране хозяина, частичный обмен компонентами мембран с хозяином, транспорт через трансмембранные каналы, неполный фагоцитоз. Некоторые исследователи обнаруживали микоплазмы в перинуклеарных зонах клеток.
Экзотоксины выявлены только у М. neurolyticum, существование их у других видов не доказано.
Эндотоксины выделены у M. pneumonia и M. arthritidis.
Гемолизины обнаружены практически у всех видов, чаще всего – это перекиси, однако они не всегда способны лизировать эритроциты человека [18, 19].
Ферментами патогенности являются нейраминидаза, аргинин-дезаминаза, фосфолипаза и нуклеаза; две последние придают микоплазмам особое значение в акушерской практике [16]. Аргининдезаминаза приводит к дефициту аргинина и к цитопатическому действию. Установлено, что при введении в среду избытка аргинина этот эффект нивелируется. Фосфолипаза приводит к избытку арахидоновой кислоты – предшественника простагландинов, которые в свою очередь вызывают сокращение матки и самопроизвольное прерывание беременности. Нуклеаза имеет способность ферментировать ДНК, приводя к врожденным порокам развития. Так, некоторые исследователи отмечают при микоплазмозе повышенный риск возникновения синдрома Дауна [44].
Продукты метаболизма, повреждающие структуры хозяина, могут быть различными: при ферментации мочевины образуется аммиак; при ферментации углеводов – кислоты, приводящие к изменению рН среды [5].
Мембранное паразитирование и способность к синтезу перекисей объясняет активацию перекисного окисления липидов за счет повышения уровня гидроперекисей в плазме крови, снижения общей антиокислительной способности плазмы и активации антиоксидантных систем церулоплазмина и глутатионпероксидазы [20, 21].
По мнению многих исследователей, микоплазмы имеют способность стимулировать все виды иммунного ответа, но долговременная персистенция возбудителя достигается благодаря механизмам ускользания и взаимодействия с иммунной системой [19, 38].
К механизмам ускользания относят существование возбудителя в инвагинатах мембран, где он недосягаем для фагоцитов и антител [12]. Некоторые исследователи описывают внутриклеточное существование микоплазм, которое возможно при ослаблении организма, например вследствие СПИДа. Кроме того, благодаря отсутствию ригидной клеточной стенки, микоплазмы не имеют сильных антигенных детерминант, слабо стимулируют иммунный ответ. В случае неполного фагоцитоза микоплазмы могут распространяться в организме. Выявлено, что завершенный фагоцитоз возможен только в случае опсонизации микоплазм. Также важным свойством микоплазм является способность тесно связываться с клеточной стенкой хозяина и обмениваться с ней компонентами мембран, вследствие чего нарушается определение антигенов, могут развиваться аутоиммунные реакции [3, 19].
К механизмам взаимодействия микоплазм с иммунной системой относят их способность блокировать фагоцитоз, цитотоксическую активность лимфоцитов, способность снижать пролиферацию и активность Т-киллеров [11]. У беременных с микоплазмозом отмечается увеличение общего количества лимфоцитов при сохраненном иммунорегуляторном индексе, снижение их активности в реакции бласттрансформации [9].
При изучении интерлейкинового статуса [3] наблюдается повышение уровней интерлейкина (ИЛ) 2-го типа, ИЛ-6, ИЛ-10, при сохраненных уровнях ИЛ-1 и фактора некроза опухоли, что объясняет изменения в иммунном статусе [5, 20, 38]. Доказанным является способность некоторых микоплазм синтезировать фактор, идентичный ИЛ-6 [35], что исследователи объясняют обменом генетическим материалом в результате длительного эволюционного сосуществования с хозяином. По мнению авторов, это свойство способствует селекции штаммов, индифферентных к селективным иммуноглобулинам [34].
Эпидемиология
Сведения о распространении микоплазм среди различных групп населения довольно разнообразны. Так, по данным California Association оf Healthcare Admissions Management (САНАМ), которая занимается исследованием заболеваний, передающихся половым путем (ЗППП), в России заболеваемость микоплазмозом составляет 81,2 случая на 100 тыс. человек [1-3, 18].
Так, по данным California Association оf Healthcare Admissions Management (САНАМ), которая занимается исследованием заболеваний, передающихся половым путем (ЗППП), в России заболеваемость микоплазмозом составляет 81,2 случая на 100 тыс. человек [1-3, 18].
По данным американских ученых, микоплазменная инфекция обнаруживается у 80% женщин с симптомами урогенитальных инфекций и у 51% – с нарушением репродуктивной функции. У беременных с признаками внутриутробного инфицирования микоплазмы определяли в 40-50% случаев, при этом M. hominis выявляли в 20%, M. genitalis – в 10%, U. Urealiticum – в 40%, несколько возбудителей – в 30% случаев. При этом в половине случаев антитела к микоплазмам определялись в крови новорожденных [32, 39].
По данным К.К. Борисенко, у здоровых женщин различные виды микоплазм встречаются в 13,3% случаев, при кольпитах – в 23,6%, при эндоцервицитах – в 37,9% [2].
Факт передачи микоплазм половым путем не вызывает сомнения. Кроме того, микоплазмоз может передаваться вертикально от матери к плоду (что доказывается наличием микоплазмоза у детей после кесарева сечения) восходящим, гематогенным, транслокационным (из одного органа в другой) путями [24].
Морфология последа
По данным литературы, микоплазменная инфекция выделяется в 65% инфекционно пораженных последов. Типичные черты микоплазменных плацентитов, согласно А.В. Цинзерлингу [26], таковы: поражения эпителиев, вакуолярная дистрофия цитоплазмы по типу пчелиных сот, пикноз ядер и наличие ШИК-позитивных включений. Часто отмечается увеличение ворсин, уменьшение межворсинчатых пространств, увеличение отложения фибриноида. При более выраженных изменениях (фиброз стромы, редукция сосудов) часто наблюдается плацентарная недостаточность, синдром задержки развития плода, антенатальная гибель плода [39]. По данным других авторов, степень поражения плаценты и наличие в ней инфекционных агентов слабо коррелируют с состоянием плода, что говорит о больших защитных возможностях органа. Так, при инфицировании плаценты плод поражается только в каждом третьем случае [26, 27, 30].
Клиника
Одним из наиболее актуальных является вопрос связи микоплазмоза с репродуктивной системой [2, 28, 36, 40]. Доказано, что микоплазма может вызывать негонорейные уретриты у мужчин, нарушения сперматогенеза и влиять на пенетрацию яйцеклетки сперматозоидом [41, 46].
Доказано, что микоплазма может вызывать негонорейные уретриты у мужчин, нарушения сперматогенеза и влиять на пенетрацию яйцеклетки сперматозоидом [41, 46].
Бесплодие у женщин тоже может являться следствием воспалительных заболеваний, вызванных микоплазмами. Наличие микоплазм в эндометрии приводит к инфицированию плодного яйца на ранних этапах эмбриогенеза [4, 32].
По данным разных авторов, угрожающий аборт и угроза преждевременных родов при микоплазмозе встречаются в 56-67% случаев; частота поздних гестозов с преобладанием раннего начала – в 30-62%; многоводие – в 9-19%; маловодие – в 8,2% [1, 23, 28, 42].
В родах у женщин с микоплазмозом аномалии отделения последа наблюдались в 22-25% случаев, кровотечение – в 14-22%, нарушение сократительной способности матки – в 17-31% [22, 29].
При исследовании состояния новорожденных [29, 36] асфиксия отмечалась в 53% случаев, явления дизадаптации – в 30,7%, нарушения психомоторного развития – в 11-21%, внутриутробные пневмонии – в 20% случаев, даже после проведенной антибиотикотерапии [14, 37].
Генерализация микоплазменной инфекции у новорожденных встречается довольно редко – до 5% у доношенных и в три раза чаще у недоношенных [31], что проявляется пневмонией, менингитом, сепсисом, бронхолегочной дисплазией. Высказано мнение, что микоплазмоз не имеет самостоятельного значения в патологии доношенных новорожденных [14].
Вызывает интерес тот факт, что среди детей с врожденными пороками развития инфицированность микоплазмозом, по данным различных авторов, составляет 50-52% [47].
Диагностика
Показанием к обследованию на микоплазмоз могут являться воспалительные заболевания женских половых органов, бесплодие, привычное невынашивание, выявленный микоплазмоз у партнера, отягощенный акушерско-гинекологический анамнез, осложненное течение беременности, ультразвуковые признаки внутриутробного инфицирования. Важным является обследование обоих партнеров на наличие микоплазмоза и других ЗППП [7].
С диагностической целью используется материал из влагалища, уретры, цервикального канала; для серологических методов диагностики – сыворотка крови [8].
Диагностика микоплазмозов может осуществляться культуральным методом с использованием преимущественно плотных питательных сред с определением колониеобразующих единиц, иммуноферментным анализом, с обязательным определением как иммуноглобулина (Ig) A, так и Ig G, либо методом ПЦР. Возможно также использование серологических методов с обязательным определением Ig A и Ig G. Определение чувствительности к антибиотикам целесообразно при неэффективности терапии [13].
В акушерстве важно также определять наличие внутриутробного инфицирования методом УЗД, с выявлением таких признаков, как гиперплазия плаценты, вентрикуломегалия, взвесь в водах, гиперэхогенность кишечника, много- или маловодие и др. [6, 33].
Лечение
Необходимость лечения микоплазмоза при выраженных проявлениях инфекции признается всеми исследователями [1], целесообразность лечения бессимптомных и стертых форм остается дискутабельной. Некоторые авторы, причисляя микоплазмы к условно-патогенным микроорганизмам, отрицают необходимость лечения [17, 18], другие – считают лечение микоплазмоза обязательным [25].
На рабочем совещании по микоплазмозу Российской академии медицинских наук были выработаны рекомендации о необходимости лечения M. genitalis в случае подтвержденного выделения возбудителя любым методом у пациентки либо у полового партнера и лечения остальных микоплазмозов только в случае выраженных проявлений инфекционного процесса и при исключении других инфекционных агентов [17].
В приказе МЗ Украины № 906 от 27.12.2006 г. «Перинатальні інфекції» микоплазмозы не упомянуты, в то же время в приказе № 286 от 07.06.2004 г. «Про удосконалення дерматовенерологічної допомоги населенню України» подчеркивается роль M. hominis и U. urealiticum в развитии внутриутробного инфицирования, невынашивания, бесплодия и даются рекомендации по лечению обоих партнеров без упоминания M. genitalis.
В терапии микоплазмоза первоочередную роль играет антибиотикотерапия. Представители класса Mollicutes чувствительны к тетрациклинам, фторхинолонам, макролидам [45]. Важным считается не увеличение дозы препарата, а соблюдение 14-дневного приема антибиотика при острых формах заболевания и 21-дневного – при хронических [10, 17].
Препаратом выбора у небеременных является доксициклин, чувствительность к которому наиболее высока. Возможно также применение тетрациклина, джозамицина, ципрофлоксацина, азитромицина, кларитромицина [15, 45].
У беременных терапию проводят во ІІ-ІІІ триместре беременности, используя ровамицин; при невозможности его приема – эритромицин, макропен. Необходимо отметить, что отечественные клиницисты рекомендуют ровамицин [15], зарубежные – эритромицин [45].
Антибиотики обычно назначают в пероральных формах, иньекционные формы применяют редко; в приказе МЗ Украины № 286 от 07.06.2004 г. «Про удосконалення дерматовенерологічної допомоги населенню України» описана методика инстилляций раствора тетрациклина в мочевой пузырь.
Кроме антибиотикотерапии, используют еще гепатопротекторы (карсил, хофитол, эссенциале), фунгицидные препараты (флуконазол), антиоксиданты (витаминные комплексы, протефлазид), десенсибилизирующую (реосорбилакт) и симптоматическую терапию [9, 17].
Профилактика
Важное значение в профилактике микоплазменной инфекции принадлежит соблюдению норм гигиены, своевременному обследованию, выявлению, лечению микоплазмоза и сопутствующих инфекций (особенно трихомонадных) не только у пациенток, но и у всех их половых партнеров [15, 17, 45].
Литература
1. Анкирская А.С., Демидова Е.М. Генитальные микоплазмы как фактор риска развития акушерской и перинатальной патологии // Вестник АМН СССР. – 1991. – № 6. – С.17-19.
2. Борисенко К.К., Тоскин И.А., Кисина В.И. О значении колонизации мочеполовых органов M. hominis и U. urealyticum. // ИППП. 1999. – № 3. – С. 28-32.
3. Борхсениус С.Н., Чернова О.А., Чернов В.М. и др. Микоплазмы. Молекулярная и клеточная биология, взаимодействие с иммунной системой млекопитающих, патогенность, диагностика. – СПб.: Наука, 2002. – 256 с.
4. Ветров В.В., Педикарева Е.А., Бугрива О.Г. Влияние микоплазменной инфекции на течение беременности // Вестник АМН СССР. – 1991. – № 6. – С. 19-20.
5. Войно-Ясинецкий М.В. Биология и патология инфекционных процессов. М.: Медицина, 1981. – 208 с.
6. Геппе Н.А., Волощук И.Н., Нестеренко О.С. и др. Особенности клинико-эхографической и морфологической картины у новорожденных с микоплазменной инфекцией // Российский педиатрический журнал. – 1998. – № 3. – С. 44-47.
– 1998. – № 3. – С. 44-47.
7. Гладкова Н.С., Киселева В.И., Доржакова Б.Г. Оценка различных методов лабораторной диагностики урогенитальных микоплазм // Вестник дерматологии и венерологии. – 1999. – № 2. – С. 43-45.
8. Горина Л.Г., Гончарова С.А., Игумов А.В. Лабораторная диагностика микоплазмозов человека // Вестник АМН СССР. – 1991. – № 6. – С. 44-47.
9. Грищенко В.І., Прокопюк В.Ю. Клініко-біохімічні особливості мікоплазмозу у вагітних. // Труды Крымского государственного медицинского университета им. С.И. Георгиевского. – 2008. – Т. 144, часть IV. – С. 44-46.
10. Захаревич Н.Н., Новикова Л.Н., Михилина Е.А. Лечение вильпрофеном и доксициклином микоплазменных и уреоплазменных инфекций // Акушерство и гинекология. – 2002. – № 2. – С. 55-56.
11. Злыдников А.М., Казанцев А.П., Шаманова М.Г. Микоплазмоз человека. – Ленинград: Медицина, 1975. – 232 с.
12. Зубжинская Л.Б., Айламазян Э.К., Парусов В.Н. Электронно-микроскопическое и иммуноморфологическое исследование плаценты при генитальном микоплазмозе // Архив патологии. – 1997. – № 2. – С. 17-22.
– 1997. – № 2. – С. 17-22.
13. Козлова В.И., Пухнер А.Ф. Вирусные, хламидийные и микоплазменные заболевания гениталий: Руководство для врача. – М.: Авиценна, «ЮНИТИ». 1995. – 317 с.
14. Лысенко К.А., Тютюнник В.Л. Перинатальные аспекты микоплазменной инфекции // Акушерство и гинекология. – 2007. – № 4. – С. 8-12.
15. Мавров И.И. Лечение больных хламидиозом и микоплазмозом // Український хіміотерапевтичний журнал. – 2002. – № 2. – С. 47-52.
16. Ноганетян К.Л. Микоплазменная инфекция: эпидемиология, этиология, патогенез. Обзор // Вісник акушерів-гінекологів України. – 2002. – № 1. – С. 3-16.
17. Прилепская В.Н., Кисина В.И., Соколовский Е.В., Савичева А.М., Гомберг М.А., Гущин А.Е., Забиров К.И., Ширшова Е.В. К вопросу о роли микоплазм в урогенитальной патологии // Гинекология. – 2007. – Т. 9. – № 1. Режим доступу до журналу http://www.consilium-medicum.com/magazines.
18. Прилепская В.Н., Фофанова И.Ю. Микоплазменная инфекция и беременность // Акушерство и гинекология. – 2007. – № 4. – С. 5-8.
– 2007. – № 4. – С. 5-8.
19. Прозоровский С.В., Раковская И.В., Вульфович Ю.В. Медицинская микоплазмология. – М.: Медицина, 1995. – 288 с.
20. Прокопюк В.Ю. Клініко-імунологічні аспекти порушень в фетоплацентарному комплексі при мікоплазмозі та можливість їх корекції // Львівський медичний часопис. – 2008. – Т. ХIV, Додаток 1. – С. 153-157.
21. Прокопюк В.Ю., Горюнова Г.И. Патогенетическое обоснование лечения микоплазмоза у беременных. Матеріали науково-практичної конференції «Інфекції в практиці клініциста». – Харків, 2008. – С. 281-282.
22. Тимаков В.Д., Качан Г.Я. Семейство Mycoplasmataceae и L-формы бактерий. – М.: Медицина, 1976 – 336 с.
23. Фомичева Е.Н., Зарубина Е.Н., Минаев В.И. Роль микоплазменной и хламидийной инфекции в акушерской практике // Акушерство и гинекология. – 1997. – № 2. – С. 55-57.
24. Фофанова И.Ю. Особенности течения беременности при наличии урогенитальных микоплазм // Гинекология. – 2007. – Т. 9. – № 1. Режим доступу до журналу http://www. consilium-medicum.com/magazines.
consilium-medicum.com/magazines.
25. Хадсон М.М.Т. Ureaplasma urealyticum // ЗППП. – 1998. – № 1. – С. 3-10.
26. Цинзерлинг В.А., Мельникова В.Ф. Перинатальные инфекции (вопросы патогенеза, морфологической диагностики и клинико-морфологических сопоставлений). Практическое руководство. – СПб.: Элби СПб, 2002. – 352 с.
27. Шабунина Н.Р., Тулакина Л.Г., Полуяхтова М.В. и др. Ультраструктурная патология плаценты при респираторно-синцитиальной вирусной инфекции и микоплазмозе // Архив патологии. – 1993. – Т. 55. – № 6. – С. 54-57.
28. Abele-Horn M., Scholz M., Wolff C. et al. High-density vaginal Ureaplasma urealyticum colonization as a risk factor for chorioamnionitis and preterm delivery // Acta Obst. Gynecol. Scand. – 2000. – № 79. – P. 973-978.
29. Berg T.G., Philpot K.L., Welsh S. et al. – Ureaplasma / Mycoplasma-infected amnionic fluid: pregnancy outcome in treated and nontreated patients // J. Perinatol. – 1999. – № 19 (4). – P. 275-277.
30. Brown M.В., Peltier M.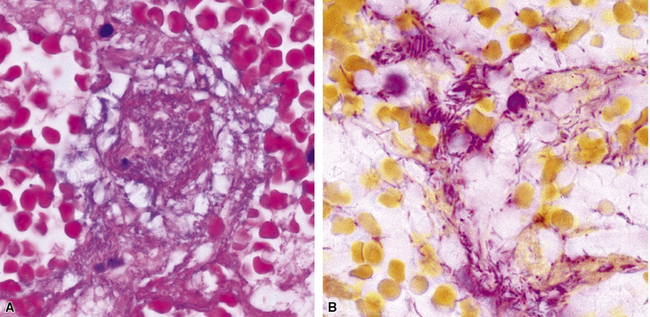 , Hiller M. et al. Genital mycoplasmosis in rats: a model for intrauterine infection // Am. J. Reprod. Immunol. – 2001. – Vol. 46, № 3. – P. 232-241.
, Hiller M. et al. Genital mycoplasmosis in rats: a model for intrauterine infection // Am. J. Reprod. Immunol. – 2001. – Vol. 46, № 3. – P. 232-241.
31. Brus F., Waarde W.M., Schoots C., Oetomo S.B. Fatal Ureaplasmal pneumoniae and sepsis in a newborn infant // Eur. J. Pediatr. – 1991. – № 150. – Р. 82-283.
32. Donders G.G., Van Bulek B., Caudron J. et al. Relationship of bacterial vaginosis and Mycoplasmas to the risk of spontaneous abortion // Amer. J. Obstet. Gynecol. – 2000. – № 183 (2). – P. 431-437.
33. Goldenberg R.L., Andrews W.W., Goepfert A.R. et al. The Alabama Preterm Birth Study: umbilical cord blood Ureaplasma urealyticum and Mycoplasma hominis cultures in very preterm newborn infants // Am. J. Obstet Gynecol. – 2008. – Vol. 198, №1. – Р. 43.e1-5.
34. Hasebe A., Shibata K., Dong L. et al. Partial purification of tlie active entities in the cultural supernatant of Mycoplasma fermentans that induce interteukin-6 production by human gingival fibroblasts: Abst.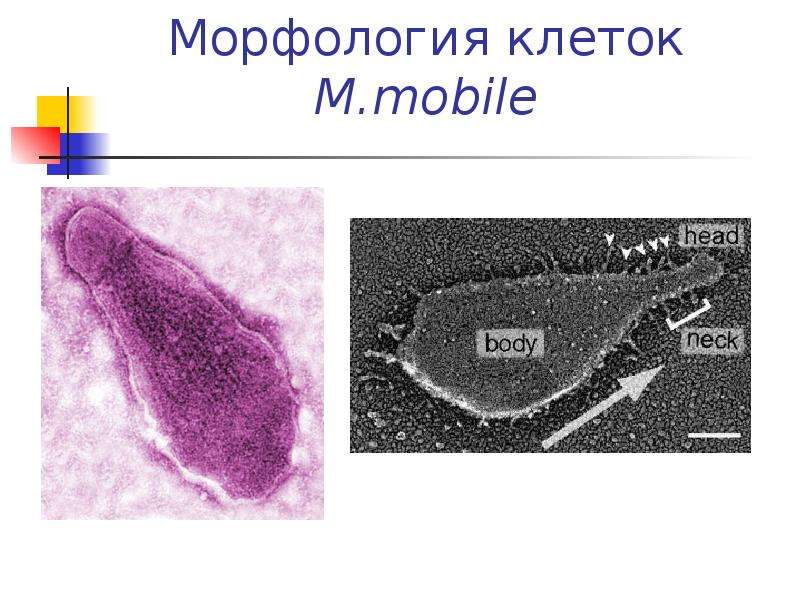 13th Int. Cong. of 10 M Fukuoka, Japan. – 2000. – P. 169.
13th Int. Cong. of 10 M Fukuoka, Japan. – 2000. – P. 169.
35. Himmelreich R., Plagens H., Hilbert H. et al. Comparative analysis of the genome of the bacteria Mycoplasma pneumoniae and Mycoplasma genitalium // Nucl. Acids Res. – 1997. – Vol. 25. – P. 701-712.
36. Fullana Montoro A., Brines Solanes J.E. Ureoplasma ureoliticum and Mycoplasma hominis – incidence and clinical significance of their isolation in perinatal period // An. Esp. Pediatr. – 1992. – Vol. 36. – № 4. – P. 285-288.
37. Kataoka S., Yamada T., Chou K., Nishida R. Association between preterm birth and vaginal colonisation by Mycoplasma in early pregnancy // J. Clin. Microbiol. – 2006. – № 44 (1) – P. 51-55.
38. Krugner T., Baer J. Inductions of neutrophil chemoattractant cytokines by Mycoplasma hominis in alveolar type II cells // Infect. Imunn. – 1997. – Vol. 56, № 12. – P. 5131-5136.
39. Kundsin R.B., Leviton A., Allred E.N., Poulin S.A. Ureaplasma urealyticum infection of the placenta in pregnancies that ended prematurely // Obstet. Gynecol. – 1996. – Vol. 87, № 6. – P. 122-127.
Gynecol. – 1996. – Vol. 87, № 6. – P. 122-127.
40. Mei S., Wang Y. Infection of ureaplasma urealytlcum between parents and their newborns // Zhonghua Fu. Chan. Ke. Za. Zhl. – 1997. – Vol. 32, № 5. – P. 302-304.
41. Naessens A. Les infections a Ureaplasma urealyticum // Microbiologic. Acta Urol. Belg. – 1993. – № 61 (1-2). – P. 153-6.
42. Nguyen D.P., Gerber S., Hohlfeld P. et al. Mycoplasma hominis in mid-trimester amniotic fluid: relation to pregnancy outcome // J. Perinat. Med. – 2004. – № 32 (4). – Р. 323-326.
43. Rasin S., Yogev D., Naot Y. Molecular biology and pathogenicity of Mycoplasmas // Microbiol. Mol. Biol. Rev. – 1998. – № 64. – P. 1064-1066.
44. Redline R.W., Heller D., Keating S., Kingdom J. Placental diagnostic criteria and clinical correlation – a workshop report. Application of pregnancy-related proteins in prenatal and tumor diagnostics – a workshop report // Placenta. – 2005. – Vol. 26. – Supplement A, Trophoblast Reserch. – Vol. 19. – P. S114 – S117.
45. Smorgick N., Frenkel E., Zaidenstein R. et al. Antibiotic treatment of intra-amniotic infection with Ureaplasma urealyticum // Fetal. Diagn. Ther. 2007. – № 22 (2). – Р. 90-93.
46. Uuskula A., Kohl P.K. Genital Mycoplasmas, including Mycoplasma genitalium, as sexually transmitted agents // Int. J. STD. AIDS. – 2002. – № 13 (2). – P. 79-85.
47. Waites K.B., Katz B., Schelonka R.L. Mycoplasmas and ureaplasmas as neonatal pathogens // Clin. Microbiol. Rev. – 2005. – № 18 (4). – P. 757-89.
Сохранить любой ценой: причины прерывания беременности
По данным Википедии, самопроизвольным абортом заканчиваются 15-20 % клинически установленных случаев беременности. Эти цифры являются нижней оценочной границей, так как во многих случаях выкидыш происходит на ранних стадиях — до того, как женщина поймет, что она забеременела. Ведь часто клинические признаки выкидыша ошибочно принимают за обильные месячные или за их задержку.
Каковы причины прерывания беременности на разных сроках? Как подготовиться к беременности после неудачного опыта, завершившегося выкидышем? На эти вопросы ответил врач акушер-гинеколог высшей категории МЦ «Bullfinch» АЛЕКСАНДР ГИЛЬ.
— Александр Вадимович, большинство выкидышей случается в начале беременности, и многие женщины недоумевают: отчего это могло произойти?
— Главная причина выкидышей на сроке до 6 недель — это естественный отбор. Идет закладка беременности с врожденными пороками эмбриона, который уже не жизнеспособен — таким образом, осуществляется естественный отбор, в который мы не можем вмешаться.
Вы никогда не узнаете точную причину выкидыша на этом сроке, даже если после абразии (выскабливания слизистой оболочки матки), содержимое отправят на исследование. Как правило, приходит ответ: «беременность на малом сроке» и больше ничего.
Есть еще одна причина прерывания беременности, особенно если она не первая, — резус-конфликт (когда у женщины кровь резус-отрицательная, а мужчины — резус-положительная).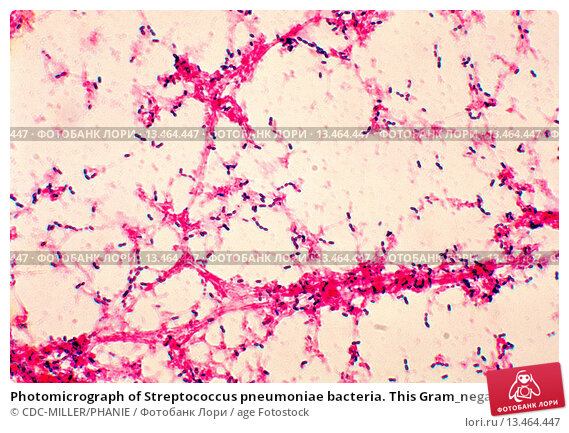 Но в нашей стране применяется эффективная профилактика резус-конфликта, так что неприятностей можно избежать на этапе планирования беременности.
Но в нашей стране применяется эффективная профилактика резус-конфликта, так что неприятностей можно избежать на этапе планирования беременности.
В структуре раннего прерывания беременности никто не исключает инфекции и проблемы, связанные с гормонами. На сроке 6-8 недель перспективные беременности часто прерываются в связи с нехваткой гормонов. При нормальной беременности у женщины в одном из яичников есть так называемое желтое тело, которое вырабатывает эндогенный прогестерон.
К сожалению, функционирование желтого тела заканчивается примерно к 7 неделям беременности, и если изначально не хватало эндогенного прогестерона, беременность перестает развиваться: происходит отслойка плодного яйца и наступает так называемая замершая беременность.
В некоторых случаях при отслойке плодного яйца, беременность можно сохранить, главное: обратиться вовремя к специалисту. Если по результатам УЗИ-исследования врач видит, что эмбрион ещё живой, беременным женщинам назначают экзогенный прогестерон в таблетках или в свечах. Также существует этот гормон в виде инъекций, — используется, чтобы быстрее насытить организм и предотвратить выкидыш.
Также существует этот гормон в виде инъекций, — используется, чтобы быстрее насытить организм и предотвратить выкидыш.
— Согласитесь, когда женщина забеременела, она не может подозревать, что у неё в организме не хватает прогестерона. Что должно её насторожить? Какие признаки на это указывают?
— Любые выделения от скудных тёмно-коричневых до более обильных кровянистых — плохой признак. Стоит, не медля, обратиться к гинекологу.
При появлении мажущих кровянистых выделений показано ультразвуковое исследование, анализ крови на прогестерон.
Хочу сказать, что нехватка прогестерона может быть причиной выкидыша до 15 недель. В 15-16 недель окончательно формируется плацента, которая будет выделять (продуцировать) этот гормон.
— Александр Вадимович, а какие проблемы могут возникнуть с плацентой во время беременности?
— На ранних сроках хорион (несформировавшаяся плацента) может перекрывать внутренний зев, может быть краевое его расположение — это большой риск прерывания беременности. В таком случае женщину кладут в больницу и наблюдают до 16 недель — к этому сроку хорион, как правило, поднимается. Но остается процент беременных, у которых плацента перекрывает зев матки — это называется «центральное расположение плаценты». Для сохранения беременности такие женщины, как правило, все время должны находиться в клинике и под наблюдением.
В таком случае женщину кладут в больницу и наблюдают до 16 недель — к этому сроку хорион, как правило, поднимается. Но остается процент беременных, у которых плацента перекрывает зев матки — это называется «центральное расположение плаценты». Для сохранения беременности такие женщины, как правило, все время должны находиться в клинике и под наблюдением.
— Какова тактика лечения инфекций, появившихся на фоне беременности?
— Инфекции могут появиться даже у тех женщин, которые до беременности тщательно обследовались. Нередко такая проблема возникает из-за кровянистых выделений — это благоприятная среда для развития инфекций.
Эктопия (эрозия) шейки матки — это тоже инфекция, которая является явной угрозой для беременности. Поэтому так важно перед зачатием пройти кольпоскопию и пролечиться от эктопии, если её обнаружат.
Инфекция восходящим путём может проникать внутриутробно и негативным образом отражаться на здоровье плода. Есть такое осложнение, как внутриутробная пневмония плода, которая лечится очень плохо и занимает большой процент в структуре младенческой смертности.
И мы лечим инфекции по возможности любым способом, который прописан в протоколе. Есть такая тактика, которая заключается в приёме антибиотиков. Бояться их не нужно, так как врач назначит только разрешенные для беременных лекарства. Иногда приходится использовать те препараты, польза от которых больше, чем риск появления побочных реакций.
— Какие угрозы могут повлиять на беременность в середине срока?
— Среди многих причин, которые приводят к самопроизвольным выкидышам — истмико-цервикальная недостаточность. Это состояние, при котором перешеек и шейка матки не справляются с возрастающей нагрузкой (растущий плод, околоплодные воды), начинают раскрываться — и ребенок рождается преждевременно.
Есть показания для профилактики этого состояния — наложение кругового подслизистого шва на шейку матки. Самый лучший срок — 16-17 недель. Можно сделать данную процедуру и после 20 недель, но эффект будет меньше.
В середине беременности у женщины может произойти отслойка плаценты. В части случаев беременность можно сохранить при помощи препаратов, влияющих на свёртываемость крови. Но нередко врачи вынуждены прибегать к операции малое кесарево сечение. Как правило, роды до 22 недель заканчиваются гибелью плода, и здесь уже идет речь о спасении жизни матери.
В части случаев беременность можно сохранить при помощи препаратов, влияющих на свёртываемость крови. Но нередко врачи вынуждены прибегать к операции малое кесарево сечение. Как правило, роды до 22 недель заканчиваются гибелью плода, и здесь уже идет речь о спасении жизни матери.
Я призываю женщин в положении воздержаться от перелётов на самолете. В моей врачебной практике было несколько случаев, когда отслойка плаценты у пациенток случилась во время полета. Кто вам окажет квалифицированную помощь в таком случае? Советую не рисковать.
В Беларуси, как и в других европейских странах, роды начинаются со срока 22 недель, но они считаются преждевременными. Врачи делают всё возможное, чтобы любыми способами сохранить перспективную беременность. Главное, всегда быть под наблюдением у специалиста и соблюдать все его рекомендации.
— Александр Вадимович, самовольное прерывание желаемой беременности — всегда большая психологическая травма для женщины. Пережить такое повторно никому не хочется.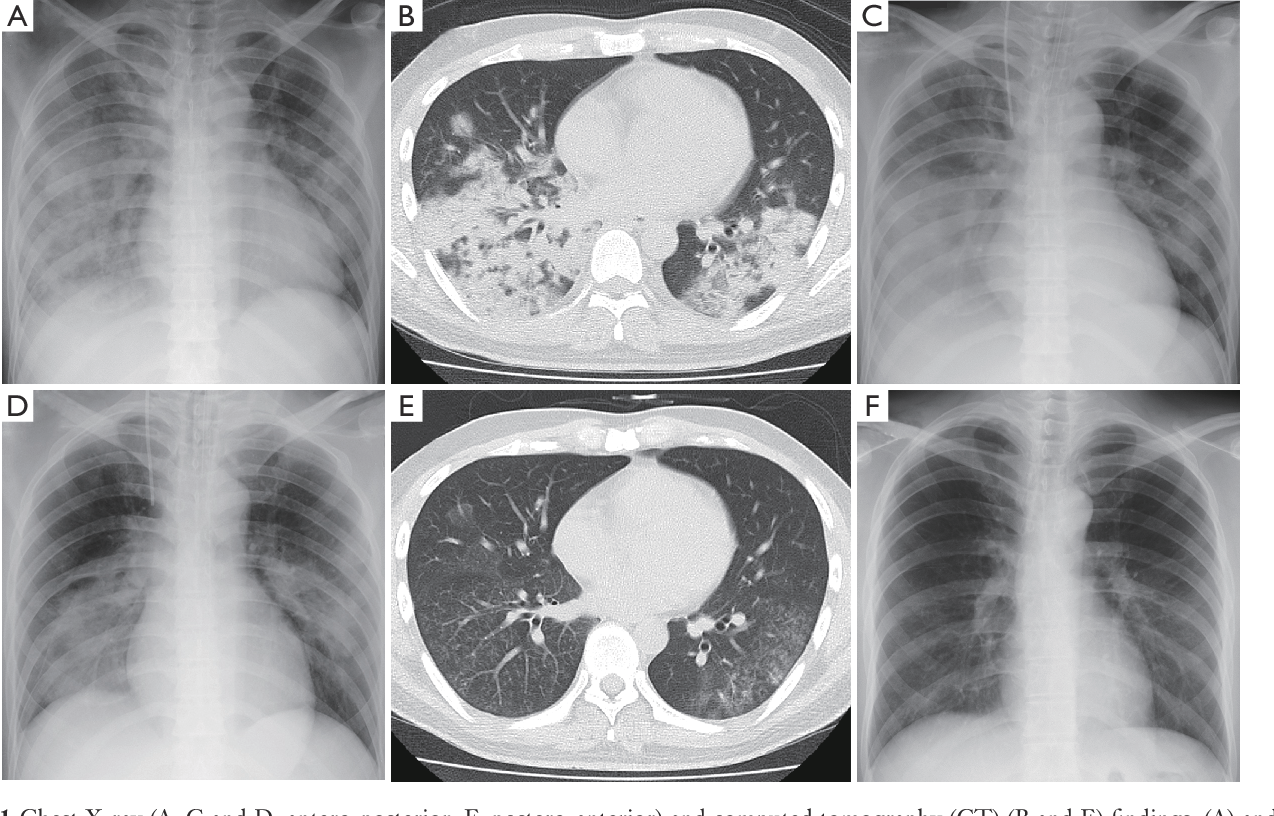 Каковы особенности подготовки к следующей беременности после выкидыша?
Каковы особенности подготовки к следующей беременности после выкидыша?
— Прежде, чем задумываться о повторной беременности, женщинам, которые испытывают душевные муки, целесообразно пройти курс психотерапии. Это очень важно, потому как проблемы психического характера могут быть очень серьезными, особенно у женщин после неудачного экстракорпорального оплодотворения (ЭКО).
Главное правило: не беременеть после выкидыша 6 месяцев. Предохраняться в это время лучше всего оральными контрацептивами, которые назначит врач. Это нужно для того, чтобы восстановить нормальную детородную функцию.
Набор обследований для женщин, у которых был выкидыш, назначается индивидуально. Но общие рекомендации такие:
1. Диагностика инфекций, передающихся половым путем: микоплазмоз, уреаплазмоз, хламидиоз, вирус простого герпеса, папилломавирус человека (ВПЧ).
Также нужно обследоваться на те инфекции, которые были возможной причиной выкидыша при предыдущей беременности.
2. Анализ на половые гормоны — если назначит врач.
3. Гормоны щитовидной железы (ТТГ, Т4 свободный, АТПО), УЗИ щитовидной железы, консультация эндокринолога.
4. По необходимости, консультация терапевта и других специалистов, анализ крови на сахар, на сифилис, ВИЧ.
5. УЗИ брюшной полости и почек. При беременности многие хронические заболевания обостряются, в т.ч. и заболевания почек. Нужно пролечиться до зачатия.
6. Кольпоскопия (осмотр шейки матки под микроскопом).
7. Анализ спермограммы партнера.
Обследование у врача-генетика показано, если при планировании беременности женщине 36 лет, а мужчине 45 лет и выше. Также данного доктора нужно посетить паре, у которой были подряд две неразвивающиеся беременности на раннем сроке.
— Когда женщина забеременела после выкидыша, должна ли она более тщательно наблюдаться у врача?
— Конечно, ведь эта женщина уже входит в группу риска по какой-то определенной группе (невынашивание, инфицирование, преждевременная отслойка и т.д.).
Врачи рекомендуют в такой ситуации женщинам вести более размеренный и спокойный образ жизни, т. е. беречься. Важно оградить беременную от переживаний, не давать ей впечатляться «страшилками» по поводу беременности. Надо четко настроиться, что в этот раз всё будет хорошо.
е. беречься. Важно оградить беременную от переживаний, не давать ей впечатляться «страшилками» по поводу беременности. Надо четко настроиться, что в этот раз всё будет хорошо.
Еще один совет из практики. Многие женщины, едва забеременев, спешат подтвердить это на УЗИ. Конечно, нет прямых доказательств того, что подобное исследование приносит вред плоду, однако нет и обратных доказательств, что оно абсолютно безвредно. Раз вы так желаете эту беременность, рисковать не стоит и грамотный доктор обязательно предостережет женщину от того, чтобы делать УЗИ на раннем сроке без особых к тому показаний.
Определить беременность и её перспективность можно при помощи анализа крови на ХГЧ (хорионический гонадотропин человека), а проще — гормон беременности. Это абсолютно безвредно для беременности. Целесообразно сдать кровь в начале задержки, через неделю — ещё раз. Если прибавка по ХГЧ нормальная, значит, беременность перспективная, не внематочная — и показаний к УЗИ нет.
Первый раз на УЗИ-диагностику женщина должна прийти на сроке беременности — 11-12 недель.
Источник: infodoktor.by
Интервью давал врач акушер-гинеколог высшей гкатегории/врач УЗИ МЦ «Bullfinch» Гиль Александр Вадимович
Другие статьи по этой теме
20 Июля 2020 Стоматология
Как сохранить здоровье зубов? Советы по уходу за зубамиКрасивая улыбка располагает окружающих. Кривые и потемневшие зубы, напротив — провоцируют отвращение и неприязнь. Однако в отношении зубов важна не только эстетическая сторона вопроса. Подорванное здоровье ротовой полости вредит всему организму. Чтобы избежать неприятных последствий, необходима регулярная гигиена.
20 Июля 2020 Гинекология
Заболевания МВС у пациентов пожилого возраста Старение населения — одна из глобальных проблем.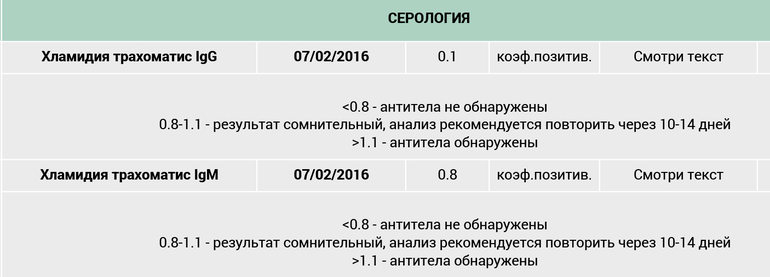 Увеличение продолжительности жизни и снижение рождаемости так или иначе приводит к старению наций. В этой связи возникают вопросы, касающиеся повышения качества жизни пожилых и людей старческого возраста.
Увеличение продолжительности жизни и снижение рождаемости так или иначе приводит к старению наций. В этой связи возникают вопросы, касающиеся повышения качества жизни пожилых и людей старческого возраста.
8 Июня 2020 Гинекология
5 фактов о физической активности, которые помогут Вам начать заниматьсяГиподинамия — проблема XXI века. От недостатка активности страдают и взрослые, и дети. Современный образ жизни, популярность интернета и распространенность дистанционных технологий приводят к ежегодному снижению физической активности у людей по всему миру. Уже давно доказано, что гиподинамия — фактор риска для развития многих заболеваний. Низкая активность провоцирует психические нарушения, онкологические заболевания, снижает качество и продолжительность жизни!
Диагностика и лечение микоплазменной и хламидийной пневмоний | #08/04
Cреди всех видов пневмоний практическому врачу наиболее часто приходится сталкиваться с внебольничной пневмонией. По данным официальной статистики МЗ РФ, заболеваемость внебольничной пневмонией в России среди лиц старше 18 лет составляет 3,9%. Зарубежные исследователи установили, что заболеваемость внебольничной пневмонией среди лиц молодого и среднего возраста варьирует от 1 до 11,6%, а в старшей возрастной группе достигает 25–44% [11, 13].
По данным официальной статистики МЗ РФ, заболеваемость внебольничной пневмонией в России среди лиц старше 18 лет составляет 3,9%. Зарубежные исследователи установили, что заболеваемость внебольничной пневмонией среди лиц молодого и среднего возраста варьирует от 1 до 11,6%, а в старшей возрастной группе достигает 25–44% [11, 13].
Наиболее распространенной причиной внебольничных пневмоний является Streptococcus pneumoniae (30–50%) [5, 11, 13]. Однако все большее значение среди этиологических факторов внебольничной пневмонии в последние годы придается так называемым атипичным микроорганизмам, прежде всего Mycoplasma pneumoniae и Chlamydophila (Chlamidia) pneumoniae, на долю которых приходится от 8 до 25% случаев заболевания [5, 9, 12].
Mycoplasma pneumoniae в структуре внебольничных пневмоний варьирует в пределах 5–50% [7, 11, 13]. Наиболее часто микоплазменная пневмония диагностируется у детей старше 5 лет и лиц молодого возраста (до 25 лет) [3, 4, 7, 10]. Каждые 3–5 лет наблюдаются эпидемиологические подъемы заболеваемости, которые длятся несколько месяцев. Вспышки заболевания характерны для изолированных и полуизолированных групп населения (военнослужащие, студенты, школьники и др., семейные вспышки) [10, 11]. Признается наличие сезонных колебаний, а именно большая распространенность инфекции в осенне-зимний период [6, 10, 13]. Источником инфекции являются как больные, так и носители. Механизм передачи инфекции — аэрогенный, путь передачи — воздушно-капельный. Инкубационный период длится 2–3 нед. Летальность при микоплазменной пневмонии составляет 1,4% [4, 11].
Каждые 3–5 лет наблюдаются эпидемиологические подъемы заболеваемости, которые длятся несколько месяцев. Вспышки заболевания характерны для изолированных и полуизолированных групп населения (военнослужащие, студенты, школьники и др., семейные вспышки) [10, 11]. Признается наличие сезонных колебаний, а именно большая распространенность инфекции в осенне-зимний период [6, 10, 13]. Источником инфекции являются как больные, так и носители. Механизм передачи инфекции — аэрогенный, путь передачи — воздушно-капельный. Инкубационный период длится 2–3 нед. Летальность при микоплазменной пневмонии составляет 1,4% [4, 11].
Mycoplasma pneumoniae занимает промежуточное положение между вирусами, бактериями и простейшими и является мембрано-ассоциированным (но может быть и внутриклеточным) анаэробом, имеет трехслойную цитоплазматическую мембрану вместо клеточной стенки, что обусловливает резистентность к различным агентам, подавляющим синтез клеточной стенки, прежде всего к пенициллину и другим β-лактамам [6, 10]. С помощью терминальной структуры микоплазма прикрепляется к клеткам хозяина (эритроцитам, клеткам реснитчатого эпителия бронхов и др.) [6]. Микоплазма также обладает механизмом мимикрии под антигенный состав клетки-хозяина, что способствует длительной персистенции возбудителя и вызывает образование аутоантител и развитие аутоиммунных процессов при микоплазменной инфекции [6, 10]. Предполагается, что именно с формированием аутоантител связано развитие нереспираторных проявлений Mycoplasma pneumoniae-инфекции.
С помощью терминальной структуры микоплазма прикрепляется к клеткам хозяина (эритроцитам, клеткам реснитчатого эпителия бронхов и др.) [6]. Микоплазма также обладает механизмом мимикрии под антигенный состав клетки-хозяина, что способствует длительной персистенции возбудителя и вызывает образование аутоантител и развитие аутоиммунных процессов при микоплазменной инфекции [6, 10]. Предполагается, что именно с формированием аутоантител связано развитие нереспираторных проявлений Mycoplasma pneumoniae-инфекции.
Считается, что от 5 до 15% внебольничных пневмоний вызываются хламидиями, а в период эпидемии эти показатели могут увеличиваться до 25% [4, 5, 10]. Наиболее часто хламидийная пневмония встречается у взрослых, особенно у лиц среднего и пожилого возраста [2, 10]. Описаны эпидемиологические вспышки в изолированных и полуизолированных коллективах, случаи внутрисемейной передачи хламидийной инфекции [7, 10, 13]. Сезонной закономерности распространения этой инфекции не выявлено. Единственным известным резервуаром инфекции является человек. Механизм передачи — аэрогенный, путь передачи — воздушно-капельный. Инкубационный период составляет 2–4 нед. Летальность при хламидийных пневмониях достигает 9,8% [4, 5, 13].
Единственным известным резервуаром инфекции является человек. Механизм передачи — аэрогенный, путь передачи — воздушно-капельный. Инкубационный период составляет 2–4 нед. Летальность при хламидийных пневмониях достигает 9,8% [4, 5, 13].
Chlamydophila pneumoniae — это патогенные облигатные внутриклеточные грамотрицательные бактерии, способные к латентному существованию или персистенции в организме хозяина. Характеризуются двухфазным циклом развития, состоящим из чередования функционально и морфологически различных форм — элементарных и ретикулярных телец [2, 4, 7, 10].
Клинические проявления микоплазменнойи хламидийной пневмоний
У 30–40% пациентов, заболевших микоплазменной и/или хламидийной пневмонией, диагноз ставится лишь в конце первой недели болезни; первоначально у них чаще всего ошибочно диагностируются бронхит, трахеит или ОРЗ. Это связано с тем, что, в отличие от бактериальных пневмоний, микоплазменная и хламидийная не имеют отчетливых физикальных и рентгенологических признаков инфильтрации, а культуральная диагностика их невозможна, так как микоплазмы и хламидии являются внутриклеточными возбудителями. Поэтому диагностика микоплазменной и хламидийной пневмоний основывается в первую очередь на выявлении особенностей клинико-рентгенологических данных и подтверждается серологически или с помощью полимеразно-цепной реакции (ПЦР).
Поэтому диагностика микоплазменной и хламидийной пневмоний основывается в первую очередь на выявлении особенностей клинико-рентгенологических данных и подтверждается серологически или с помощью полимеразно-цепной реакции (ПЦР).
Обычно микоплазменная и хламидийная пневмонии начинаются с респираторного синдрома, проявляющегося трахеобронхитом, назофарингитом, ларингитом; протекают с субфебрильной температурой, малопродуктивным, мучительным кашлем, скудными аускультативными данными; характеризуются наличием внелегочных проявлений — кожных, суставных, гематологических, гастроэнтерологических, неврологических и других, а также нетипичными лабораторными показателями — отсутствием лейкоцитоза и нейтрофильного сдвига в периферической крови [3, 4, 7, 10, 11]. Рентгенологические изменения в легких отмечаются усилением легочного рисунка, перибронхиальной или субсегментарной инфильтрацией [5, 10, 11, 13].
Нами были обследованы 60 пациентов: 44 — с микоплазменной пневмонией и 16 — с хламидийной пневмонией. Анализ клинического материала показал, что начало заболевания при микоплазменной и хламидийной пневмониях может быть как острым, так и постепенным (табл. 1). При подостром течении пневмония начинается с поражения верхних дыхательных путей, ухудшения общего состояния и познабливания. Температура тела может быть нормальной или субфебрильной в течение 6–10 дней и лишь потом повышается до 38–39,9°С при микоплазменной и до 38–38,9°С при хламидийной пневмонии. При остром начале симптомы интоксикации появляются уже в первый день и достигают максимума к 3-му дню болезни. У пациентов с постепенным началом болезни интоксикация наиболее выражена на 7–12-й день от начала заболевания. Характерными признаками интоксикации для микоплазменной и хламидийной пневмоний являются умеренная головная боль, миалгия, общая слабость.
Анализ клинического материала показал, что начало заболевания при микоплазменной и хламидийной пневмониях может быть как острым, так и постепенным (табл. 1). При подостром течении пневмония начинается с поражения верхних дыхательных путей, ухудшения общего состояния и познабливания. Температура тела может быть нормальной или субфебрильной в течение 6–10 дней и лишь потом повышается до 38–39,9°С при микоплазменной и до 38–38,9°С при хламидийной пневмонии. При остром начале симптомы интоксикации появляются уже в первый день и достигают максимума к 3-му дню болезни. У пациентов с постепенным началом болезни интоксикация наиболее выражена на 7–12-й день от начала заболевания. Характерными признаками интоксикации для микоплазменной и хламидийной пневмоний являются умеренная головная боль, миалгия, общая слабость.
Одним из постоянных признаков микоплазменной и хламидийной пневмоний, по нашим данным, является кашель, который возникает одновременно с лихорадкой. У больных микоплазменной пневмонией, в отличие от хламидийной, наблюдается частый, преимущественно непродуктивный, навязчивый, мучительный, приступообразный кашель (см. табл. 1). Наряду с кашлем, у пациентов с хламидийной и микоплазменной пневмониями наблюдаются умеренные признаки поражения верхних дыхательных путей — ринит, фарингит, ларингит. Ринит чаще всего встречается у больных хламидийной пневмонией (75,0 ± 10,8%, р < 0,001) и проявляется заложенностью носа и нарушением носового дыхания, у части больных наблюдаются небольшие либо умеренные слизисто-серозные или слизисто-гнойные выделения из носа. У пациентов же с микоплазменной пневмонией чаще регистрируются явления фарингита и ларингита, проявляющиеся гиперемией ротоглотки и осиплостью голоса (77,3 ± 6,3%, р < 0,05).
табл. 1). Наряду с кашлем, у пациентов с хламидийной и микоплазменной пневмониями наблюдаются умеренные признаки поражения верхних дыхательных путей — ринит, фарингит, ларингит. Ринит чаще всего встречается у больных хламидийной пневмонией (75,0 ± 10,8%, р < 0,001) и проявляется заложенностью носа и нарушением носового дыхания, у части больных наблюдаются небольшие либо умеренные слизисто-серозные или слизисто-гнойные выделения из носа. У пациентов же с микоплазменной пневмонией чаще регистрируются явления фарингита и ларингита, проявляющиеся гиперемией ротоглотки и осиплостью голоса (77,3 ± 6,3%, р < 0,05).
Из внелегочных проявлений при микоплазменной пневмонии чаще отмечались миалгия (63,6%), макуло-папулезная сыпь (22,7%), явления желудочно-кишечного дискомфорта (25%), при хламидийной — артралгия (18,8%) и миалгия (31,3%).
Изменения в легких, характерные для уплотнения легочной ткани, при физикальном обследовании пациентов с пневмониями, вызванными атипичными возбудителями (в отличие от больных с бактериальными пневмониями), определялись не всегда. В частности, укорочение перкуторного звука у больных микоплазменной и хламидийной пневмониями наблюдалось в 68,2 и 68,8% случаев соответственно (табл. 1). Этот признак всегда выявлялся у больных с сегментарной, полисегментарной, долевой пневмонией и лишь у 1/3 пациентов с перибронхиальной инфильтрацией. У больных микоплазменной пневмонией над зоной поражения чаще выслушивались ослабленное дыхание (40,9%), сухие и влажные хрипы (47,7%), у пациентов с хламидийной пневмонией — как ослабленное (37,5%), так и бронхиальное дыхание (31,2%) и влажные хрипы (62,5%).
В частности, укорочение перкуторного звука у больных микоплазменной и хламидийной пневмониями наблюдалось в 68,2 и 68,8% случаев соответственно (табл. 1). Этот признак всегда выявлялся у больных с сегментарной, полисегментарной, долевой пневмонией и лишь у 1/3 пациентов с перибронхиальной инфильтрацией. У больных микоплазменной пневмонией над зоной поражения чаще выслушивались ослабленное дыхание (40,9%), сухие и влажные хрипы (47,7%), у пациентов с хламидийной пневмонией — как ослабленное (37,5%), так и бронхиальное дыхание (31,2%) и влажные хрипы (62,5%).
При рентгенографии органов грудной клетки у больных микоплазменной и хламидийной пневмониями выявлялись и типичные пневмонические инфильтрации и интерстициальные изменения. При микоплазменной пневмонии чаще наблюдается двустороннее поражение легких (40,9%) с усилением легочного рисунка (22,7%) и перибронхиальной инфильтрацией (50%), при хламидийной пневмонии — наоборот, чаще полисегментарная инфильтрация (43,7%) и реже интерстициальные изменения (31,3%).
В общем анализе крови у больных микоплазменной и хламидийной пневмониями чаще отмечается нормальное количество лейкоцитов и умеренное повышение СОЭ (в среднем 37,1 ± 1,9 мм/ч).
По нашим наблюдениям, для микоплазменной и хламидийной пневмоний характерно затяжное рецидивирующее течение.
Таким образом, согласно клинико-рентгенологическим данным и с учетом эпидемиологической ситуации, из общего числа пациентов с внебольничными пневмониями можно выделить больных с микоплазменной и/или хламидийной пневмониями. В нашем исследовании таких больных оказалось 80, из них у 60 (75%) в дальнейшем лабораторным методом была установлена микоплазменная или хламидийная этиология пневмонии.
Диагностика микоплазменной и хламидийной пневмоний
Решающая роль в выявлении микоплазменной и хламидийной инфекции отводится лабораторной диагностике.
Самым специфичным и чувствительным методом лабораторной диагностики микоплазменной и хламидийной инфекции является выделение культуры Mycoplasma pneumoniae и Chlamydophila pneumoniae («золотой стандарт») [1, 2, 5, 6, 10, 11], однако это чрезвычайно трудоемкий и длительный процесс: микроорганизмы растут медленно (не менее 7–14 сут), требуют специальных сред [11, 13]. В связи с этим общепринятым методом диагностики является серотипирование, т. е. выявление специфических IgM- и IgG-антител к Chlamydophila pneumoniae, Mycoplasma pneumoniae. Чаще всего используются метод иммуноферментного анализа (ИФА) (Thermo Electron, Beckman Coulter, Abbot Laboratories, Medac Diagnostica), реакция микроиммунофлюоресценции (МИФ). Стандартом серологической диагностики микоплазменной инфекции на сегодня является ИФА-метод обнаружения специфических IgM- и IgG-антител (>1:64), хламидийной инфекции — тест ИФА-метод и реакция МИФ, позволяющие идентифицировать специфические IgМ, IgG и IgА в диагностически значимых титрах (>1:16, >1:512 и >1:256 соответственно) и/или 4-кратное повышение титра IgG или IgА в парных сыворотках крови [1, 4, 7, 10]. По динамике уровня специфических антител, определяемых ИФА-методом (табл. 2), можно установить характер и стадию заболевания [10, 11, 13].
В связи с этим общепринятым методом диагностики является серотипирование, т. е. выявление специфических IgM- и IgG-антител к Chlamydophila pneumoniae, Mycoplasma pneumoniae. Чаще всего используются метод иммуноферментного анализа (ИФА) (Thermo Electron, Beckman Coulter, Abbot Laboratories, Medac Diagnostica), реакция микроиммунофлюоресценции (МИФ). Стандартом серологической диагностики микоплазменной инфекции на сегодня является ИФА-метод обнаружения специфических IgM- и IgG-антител (>1:64), хламидийной инфекции — тест ИФА-метод и реакция МИФ, позволяющие идентифицировать специфические IgМ, IgG и IgА в диагностически значимых титрах (>1:16, >1:512 и >1:256 соответственно) и/или 4-кратное повышение титра IgG или IgА в парных сыворотках крови [1, 4, 7, 10]. По динамике уровня специфических антител, определяемых ИФА-методом (табл. 2), можно установить характер и стадию заболевания [10, 11, 13].
Также в последнее время для этиологической диагностики микоплазменной и хламидийной инфекции используется ПЦР, основанная на определении ДНК возбудителя с применением метода генных зондов [3, 4, 5, 7, 10].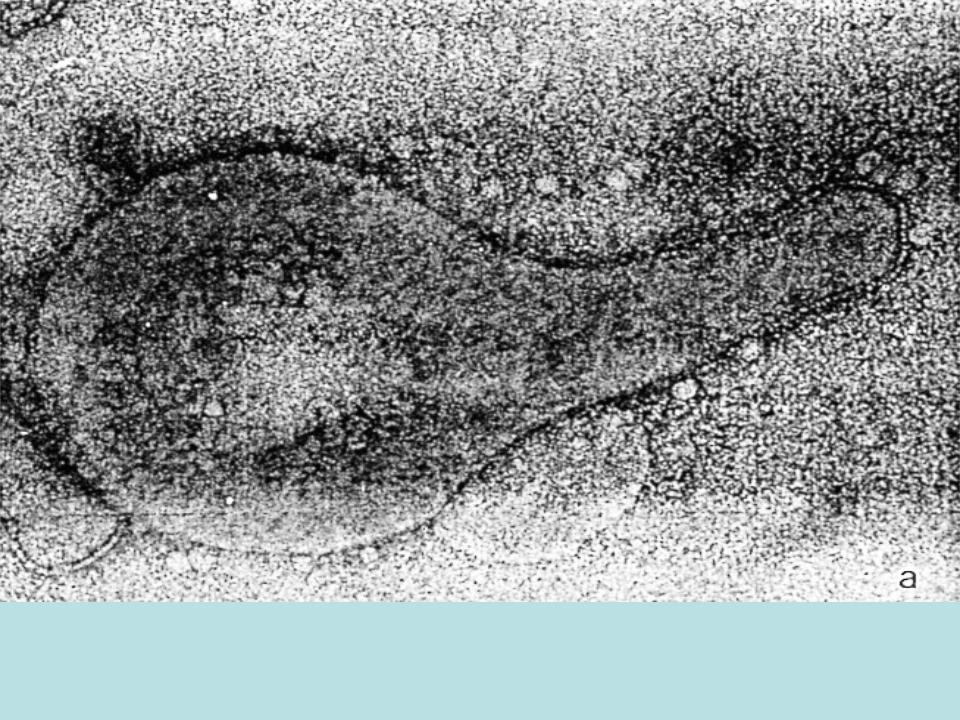 С помощью ПЦР возможна быстрая диагностика микоплазменной и хламидийной инфекции, но этот метод не позволяет отличить активную инфекцию от персистирующей [1, 7, 10, 11].
С помощью ПЦР возможна быстрая диагностика микоплазменной и хламидийной инфекции, но этот метод не позволяет отличить активную инфекцию от персистирующей [1, 7, 10, 11].
Таким образом, для достоверной этиологической идентификации микоплазменной и хламидийной пневмоний необходимо проведение серологических тестов в комплексе с методами, основанными на выявлении ДНК микроорганизма.
Лечение микоплазменной и хламидийной пневмоний
Рассмотренные выше микробиологические особенности Mycoplasma pneumoniae и Chlamydophila pneumoniae (главным образом внутриклеточный цикл развития) объясняют неэффективность широко используемых в клинической практике β-лактамных антибиотиков (пенициллины и цефалоспорины) и обусловливают необходимость применения антимикробных препаратов, способных проникать и накапливаться в пораженных клетках, а также блокировать внутриклеточный синтез белка. Такими свойствами обладают макролиды, фторхинолоны и тетрациклины, которые и являются средствами эрадикационной терапии при Mycoplasma pneumoniae— и Chlamydophila pneumoniae-инфекции [3, 4, 7, 10, 11].
С учетом особенностей спектра антимикробной активности и фармакокинетики препаратами первого ряда считаются макролиды [5, 10, 11]. К тому же макролиды по сравнению с тетрациклинами и фторхинолонами безопаснее при лечении новорожденных, детей и беременных. Механизм действия макролидов связан с нарушением синтеза белка в клетках чувствительных микроорганизмов. Кроме того, для большинства этих препаратов характерен постантибиотический эффект, в основе которого лежат необратимые изменения в рибосомах микроорганизма. Благодаря этому антибактериальное действие усиливается и пролонгируется, сохраняясь в течение срока, необходимого для ресинтеза новых функциональных белков микробной клетки. Более того, макролиды обладают противовоспалительными и иммуномодулирующими свойствами, которые обусловлены несколькими механизмами [11]. Во-первых, макролиды оказывают модулирующее влияние на такие функции нейтрофилов, как фагоцитоз, хемотаксис, киллинг. Под влиянием 14-членных макролидов происходит ингибирование окислительного «взрыва», в результате чего уменьшается образование высокоактивных окисляющих соединений, способных повреждать не только бактериальные клетки, но и собственные ткани [10, 11]. Кроме того, взаимодействуя с клетками иммунной системы, макролиды могут ингибировать синтез и/или секрецию таких провоспалительных цитокинов, как интерлейкины-1, -6, -8, фактор некроза опухоли α, и, наоборот, усиливать секрецию противовоспалительных интерлейкинов-2, -4, -10. Установлено, что макролиды препятствуют адгезии бактерий к поверхности клеток макроорганизма, а также тормозят экспрессию факторов вирулентности некоторых микробов [5, 10, 11].
Кроме того, взаимодействуя с клетками иммунной системы, макролиды могут ингибировать синтез и/или секрецию таких провоспалительных цитокинов, как интерлейкины-1, -6, -8, фактор некроза опухоли α, и, наоборот, усиливать секрецию противовоспалительных интерлейкинов-2, -4, -10. Установлено, что макролиды препятствуют адгезии бактерий к поверхности клеток макроорганизма, а также тормозят экспрессию факторов вирулентности некоторых микробов [5, 10, 11].
В России макролиды представлены широким спектром препаратов (см. табл. 3). Среди них наиболее активным в отношении Mycoplasma pneumoniae признан азитромицин, имеющий ряд преимуществ перед эритромицином и кларитромицином [4, 10, 11]. В отношении Chlamydophila pneumoniae наиболее активным средством признается кларитромицин [10]. Также эффективны в отношении этих внутриклеточных патогенов и некоторые другие представители макролидов: джозамицин, спирамицин. Старый антимикробный препарат из этой группы — эритромицин — также обладает антимикоплазменной и антихламидийной активностью, но, несомненно, уступает в этом отношении вышеперечисленным антибиотикам, обладая при этом целым рядом побочных эффектов [5, 10, 11].
Значительной активностью по отношению к Mycoplasma pneumoniae и Chlamydophila pneumoniae обладают фторхинолоны — офлоксацин (заноцин, таривид, офло), ципрофлоксацин (ципробай, ципролет, цифран, сифлокс, медоциприн, цифлоксинал), в связи с чем эти антимикробные препараты рассматриваются в качестве альтернативы макролидам при данной инфекции. Высокую активность проявляют новые фторхинолоны — левофлоксацин (таваник) и моксифлоксацин (авелокс). Моксифлоксацин и левофлоксацин успешно подавляют практически любую флору, вызывающую пневмонии.
При лечении микоплазменных и хламидийных пневмоний эффективны и тетрациклины, однако антибиотики этой группы не применяются при беременности, а также печеночной недостаточности. Вероятность проявления побочных эффектов при их применении может быть выше. Из тетрациклинов активны в отношении атипичных микроорганизмов доксициклин и моноциклин (см. табл. 3).
Продолжительность антимикробной терапии неосложненных бактериальных внебольничных пневмоний составляет 5–10 дней. Для лечения микоплазменной и хламидийной пневмоний рекомендуется применять антимикробные средства не менее 2–3 нед [4, 5, 10, 11]. Сокращение сроков лечения чревато развитием рецидива инфекции [4, 10].
Для лечения микоплазменной и хламидийной пневмоний рекомендуется применять антимикробные средства не менее 2–3 нед [4, 5, 10, 11]. Сокращение сроков лечения чревато развитием рецидива инфекции [4, 10].
При нетяжелом течении микоплазменной и хламидийной пневмоний антимикробные препараты назначаются внутрь в среднетерапевтических дозах. Естественно, при тяжелых пневмониях предпочтение следует отдавать внутривенному применению антибиотика. Эритромицин фосфат назначается до 1–2 г/сут в 2–3 введения (максимально по 1 г каждые 6 ч). Спирамицин используется внутривенно по 1,5 млн МЕ 3 раза в сутки, а кларитромицин — по 250 мг 2 раза в сутки с равными интервалами. Для разведения спирамицина и кларитромицина следует применять 5%-ный раствор глюкозы.
Стоимость внутривенного лечения антибиотиками (в частности, макролидами) весьма высока, поэтому используют ступенчатую терапию, при которой лечение начинается с внутривенного применения антибиотиков, а по достижении клинического эффекта (обычно через 2–3 дня) пациент переводится на пероральную терапию тем же препаратом или другим макролидом. Ступенчатая монотерапия макролидами может проводиться эритромицином, кларитромицином, спирамицином, т. е. препаратами, которые выпускаются в двух формах: для внутривенного введения и для приема внутрь.
Ступенчатая монотерапия макролидами может проводиться эритромицином, кларитромицином, спирамицином, т. е. препаратами, которые выпускаются в двух формах: для внутривенного введения и для приема внутрь.
Несмотря на большой спектр противомикробных препаратов, эффективное лечение микоплазменных и хламидийных пневмоний представляет до настоящего времени большую проблему [2, 6, 10, 11]. Это связано с тем, что их развитие, как правило, происходит на фоне снижения антиинфекционной резистентности организма, обусловленного угнетением иммунитета [8, 9, 10, 12]. Проведенное нами исследование показателей иммунограммы у пациентов с внебольничной пневмонией микоплазменной и хламидийной этиологии выявило снижение абсолютного числа лимфоцитов, зрелых Т-лимфоцитов (CD3+), Т-хелперов (CD4+), абсолютного числа Т-супрессоров (CD8+), угнетение функциональной активности Т-системы, проявляющееся снижением плотности рецепторов к IL-2 (CD25+), способности к бласттрансформации (CD71+ — лимфоциты) и апоптозу (CD95+), а также активацию гуморального иммунитета, что проявлялось повышением числа В-лимфоцитов (CD20+), уровня IgM и ЦИК.
Микоплазмы и хламидии на разных стадиях развития располагаются как внутриклеточно, так и внеклеточно, что требует для их элиминации участия гуморальных и клеточных механизмов иммунитета [8, 9, 10, 12]. Большинство антимикробных средств действует преимущественно на внеклеточную форму возбудителей. Это приводит к персистенции возбудителей, диссеминации ее в организме, хронизации процесса, формированию осложнений. Применение лишь антимикробных средств означает лишь временное подавление возбудителей, так как на фоне такой терапии происходит сохранение и даже усугубление иммунологических расстройств, что повышает риск рецидива заболеваний [14]. Так, по результатам наших исследований, к концу курса традиционной терапии происходило усугубление Т-клеточной депрессии: снижалось относительное и абсолютное количество Т-лимфоцитов (CD3+), Т-хелперов (CD4+), Т-супрессоров (CD8+) на фоне повышения уровня IgG, ЦИК, фагоцитарного индекса и уменьшения IgA.
В связи с этим хотелось бы подчеркнуть, что терапия микоплазменной и хламидийной пневмоний должна быть комплексной и включать, помимо антимикробных средств, препараты, действие которых направлено на коррекцию иммунного ответа.
С этой целью у больных микоплазменной и хламидийной пневмониями нами применяются иммуномодуляторы (ронколейкин, ликопид, тималин, тимоген).
Включение иммуномодуляторов в комплексное лечение микоплазменных и хламидийных пневмоний позволяет добиться ярко выраженного иммунологического эффекта. Последний сочетается с выраженным клиническим воздействием, проявляющимся сокращением сроков достижения клинико-лабораторной ремиссии в среднем на 3 койко-дня, уменьшением интоксикационных симптомов через 1–3 сут после начала лечения, сокращением лихорадочного периода в 2 раза, четкой положительной рентгенологической динамикой к 12-му дню лечения у 76,7% больных; значительным уменьшением вероятности развития повторных рецидивов и хронизации процесса.
Литература
- Бочкарев Е. Г. Лабораторная диагностика хламидийной инфекции // Иммунопатология, аллергология, инфектология. — 2000. — № 4. — С. 65–72.
- Гранитов В. М. Хламидиозы.
 — М., 2000. — 48 с.
— М., 2000. — 48 с. - Новиков Ю. К. Атипичные пневмонии // Русский медицинский журнал. — 2002. — Т. 10. — № 20. — С. 915–918.
- Ноников В. Е. Диагностика и лечение атипичных пневмоний // CONSILIUM medicum. — 2001. — T. 3. — № 12. — C. 569–574.
- Проект практических рекомендаций МЗ РФ. Внебольничная пневмония у взрослых: диагностика, лечение, профилактика. — М., 2002. — 51 с.
- Прозоровский С. В., Раковская И. В., Вульфович Ю. В. Медицинская микоплазмология. — М.: Медицина, 1995. — 285 с.
- Синопальников А. И. Атипичная пневмония // Русский медицинский журнал. — 2002. — Т. 10. — № 23. — С. 1080–1085.
- Справочник по иммунотерапии для практического врача / Под ред. А. С. Симбирцева. — СПб.: Диалог, 2002. — 480 с.
- Хаитов Р. М., Игнатьева Г. А., Сидорович И. Г. Иммунология. — М.: Медицина, 2000. — 432 с.
- Хаитов Р. Ф., Пальмова Л. Ю. Mycoplasma pneumoniae и Chlamydophila pneumoniae инфекции в пульмонологии: актуальные вопросы клиники, диагностики и лечения.
 — Казань, 2001. — 64 с.
— Казань, 2001. — 64 с. - Чучалин А. Г., Синопальников А. И, Чернеховская Н. Е. Пневмония. — М.: Экономика и информатика, 2002. — 480 с.
- Boym A. Separation of leucocytes from blood und bone marrow // Scand J Clin. Lad. Jnvest. — 1968. — V. 21. — Suppl. 87. — P. 77–82.
- Guidelines for management of adult community-acquired lower respiratory tract infections. European Study in Community-acquired Pneumonia (ESOCAP) Committee // Eur Resp J. — 1998. — № 11. — Р. 986–991.
- Kawamoto M., Oshita Y., Yoshida H. et al. Two cases hypoxemic acute broncholitis due to Mycoplasma pneumoniae // Kansenshogaku Zasshi. — 2000. — V. 74. — № 3. — P. 259–263.
Г. Г. Мусалимова, кандидат медицинских наук
В. Н. Саперов, доктор медицинских наук, профессор
Т. А. Никонорова
Чувашский ГМУ, г. Чебоксары
Обследование при планировании беременности не ЗППП
Вы планируете беременность, значит, вы должны знать, что вам необходимо пройти обследование перед беременностью на инфекции, которые передаются половым путем. Как же грамотно сдать все анализы, какое именно лечение необходимо, если инфекцию все-таки обнаружат?
Как же грамотно сдать все анализы, какое именно лечение необходимо, если инфекцию все-таки обнаружат?
В этой статье будут освящены только те инфекции, которые часто становятся предметом споров — как их лучше выявлять, всегда ли их нужно лечить, какое лечение лучше назначать женщине. Очень часто пациенты занимаются самообманом, всецело доверившись результатам единственного анализа. Будут освящены пять инфекций — хламидиоз, микоплазмоз, урепаплазмоз, герпес, цитомегаловирус.
Если у вас обнаружили хламидиоз
Хламидиоз — инфекционное заболевание, которое передается половым путем при незащищенном коитусе. Причиной хламидиоза могут стать бактерии хламидии. Вероятность того, что вы заразитесь ими бытовым путем — посидев на унитазе, поплавав в бассейне — очень низка, так как хламидии быстро погибают вне организма человека.
Симптомы хламидиоза
Инкубационный период составляет от 7 до 30 дней. У женщины: белые, желтые, прозрачные выделения из влагалища, болезненность при мочеиспускании, при половом акте, боли внизу живота, в области поясницы. У мужчины: выделения из уретры — прозрачные, скудные, боль при мочеиспускании и коитусе.
У мужчины: выделения из уретры — прозрачные, скудные, боль при мочеиспускании и коитусе.
Хламидиоз часто протекает бессимптомно, обнаружить его можно на основании сданных анализов. Хламидийная инфекция может быть причиной осложнения. Для женщин она чревата воспалительными заболеваниями матки и придатков, что может привести к бесплодию. Для мужчин она чревата воспалением придатка яичка — эпидидимит. Для того, чтобы выявить эту инфекцию, нужно сдать анализа на хламидии с помощью метода ПЦР — ДНК-диагностика. Если врач обнаружит хламидии, то назначит курс лечения, который нужно пройти обязательно обоим партнерам.
Лечение хламидиоза: назначается курс антибиотиков длительностью 21 день. Если хламидиоз обнаружен во время беременности, то женщине также назначают антибиотики, которые разрешены во время беременности — курс 2 недели, но это можно делать только после 20 недели беременности.
Чем хламидиоз опасен при беременности
При хламидиозе возрастает риск прерывания беременности. Если заразиться плод, то это приведет к хламидийной пневмонии новорожденного, к тому, что у него возникнут воспалительные заболевания глаз. Лечение хламидийной инфекции во время беременности обязательно!
Если заразиться плод, то это приведет к хламидийной пневмонии новорожденного, к тому, что у него возникнут воспалительные заболевания глаз. Лечение хламидийной инфекции во время беременности обязательно!
Уреаплазмы — бактерии, обитающие в организме человека, на слизистых половых органов, мочевыводящих путях. Эти микроорганизмы можно отнести к числу условно-патогенных, это означает, что они есть у каждого человека. Если количество бактерий резко растет, то начинает превышать допустимые пределы, у человека возникают болезненные симптомы. Это происходит при ослаблении иммунитета.
Микоплазмоз и уреаплазмоз передаются половым путем. Также еще один из способов передачи — от ребенка к матери, при этом человек может до определенного возрасти даже и не подозревать о том, что это заболевание — причина ослабления иммунитета. Симптомы уреплазмоза: воспалительные заболевания матки и придатков, цистит, пиелонефрит, камни в почках, бактериальный вагиноз.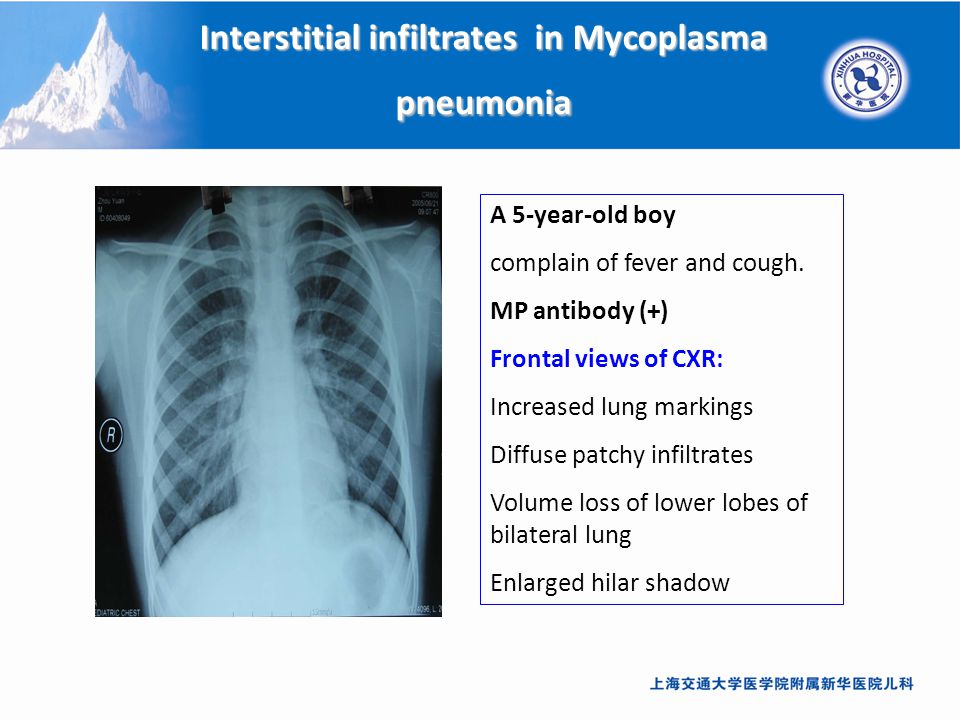 У мужчин эти бактерии чаще всего быстро размножаются при уретрите, пиелонефрите, камнях в почках.
У мужчин эти бактерии чаще всего быстро размножаются при уретрите, пиелонефрите, камнях в почках.
Диагностика уреплазмоза
Для того, чтобы выявить уреплазмоз нужно сдать анализы, используя ПЦР или культуральный посев.
Культуральный метод показывает более объективную картину — количество бактерий. ПЦР дает информацию о том, что эти микроорганизмы находятся в мочеполовых путях, однако их количество не устанавливает. Если у женщины обнаружат микоплазмы или уреаплазмы в количестве 102, то не нужно лечение, если же в количестве 104, то лечить нужно. С помощью культурального посева также можно установить, какой антибиотик пригодится для того, чтобы лечение оказалось эффективнее. При выявлении уреаплазм и микоплазм по анализу крови часто бывают ложноположительные результаты.
Лечение уреаплазмоза. Лечат обычно тогда, когда у женщины есть проблемы со здоровьем — воспаление матки, придатков, цистит, пиелонефрит. Если женщины не испытывает боли, то пролечить эти инфекции не нужно.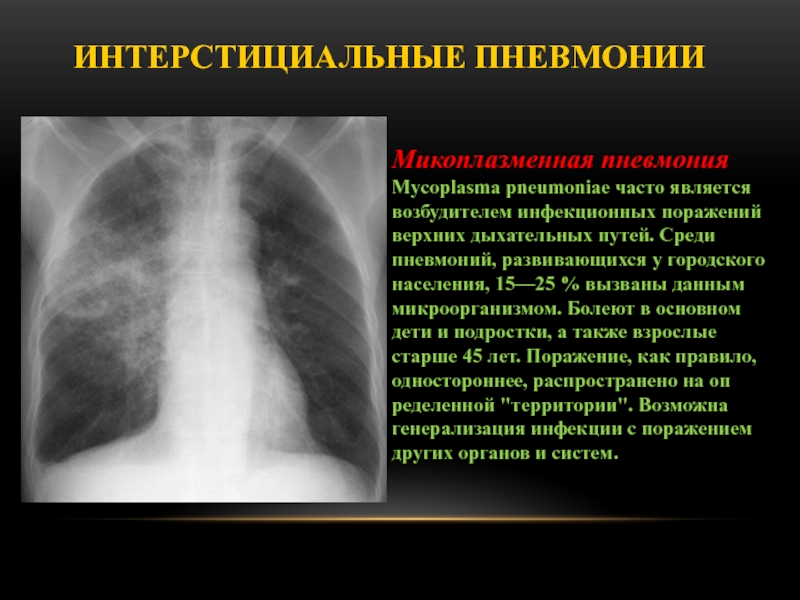 Немотивированное употребление антибиотиков приведет лишь к нарушению микрофлоры влагалища.
Немотивированное употребление антибиотиков приведет лишь к нарушению микрофлоры влагалища.
Если же мы говорим о планировании беременности, то лечить нужно обязательно, даже если у женщины нет симптомов заболевания. Лечение заключается в приеме антибиотиков-курс 10 дней. Для того, чтобы начать прием, нужно сделать посев на чувствительность к антибиотикам, чтобы определиться с выбором нужного препарата. Курс должны пройти и муж, и жена.
Если же уреаплазма обнаруживается во время беременности, то женщине также назначается антибиотик. Лечение проводится только после 20 недели беременности. До этого женщине назначают терапию иммуноглобулином (с 10 недели беременности).
Чем опасна уреаплазма и микоплазма
Уреаплазма и микоплазма могут привести к прерыванию беременности или же преждевременным родам, также ребенок может быть инфицирован. Также у детей могут развиться патологии мочевыводящих путей, циститы, пиелиты.
Если обнаружили герпес генитальный
Вирус простого герпеса опасен для вашего еще не родившегося ребенка.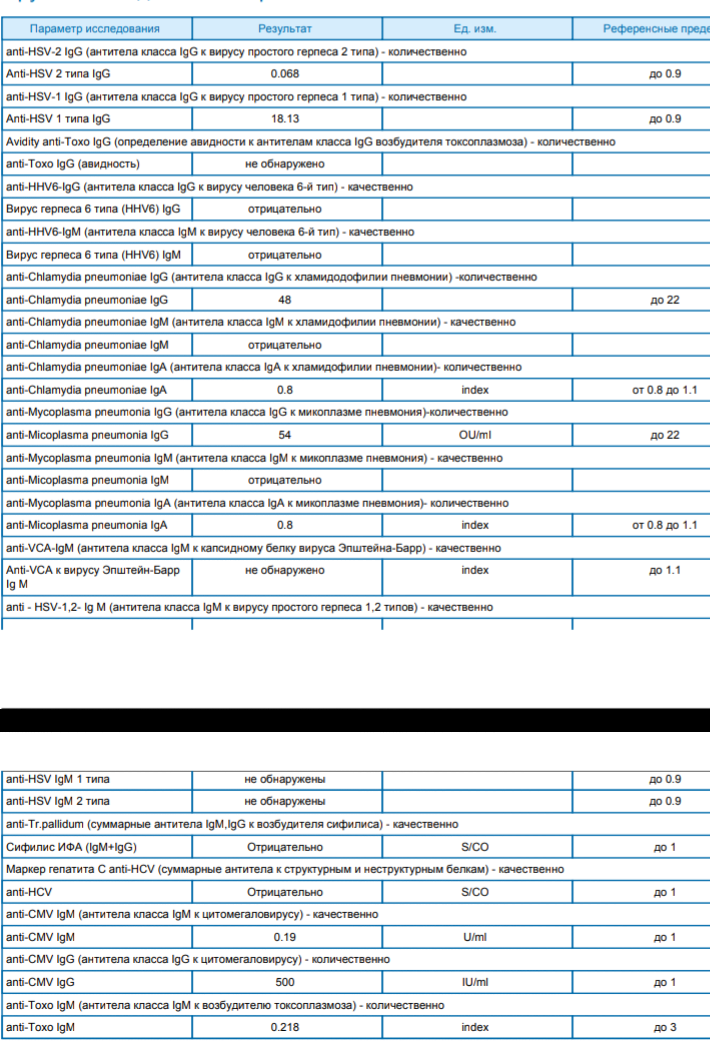 Генитальный ребенок передается половым путем, может быть передан матерью ребенку. Человек живет и не знает о том, что в нем живет инфекция, а при ослаблении иммунитета герпес вдруг проявляется.
Генитальный ребенок передается половым путем, может быть передан матерью ребенку. Человек живет и не знает о том, что в нем живет инфекция, а при ослаблении иммунитета герпес вдруг проявляется.
Симптомы генитального герпеса — при заражении герпесом появляется боль, жжение, отечность в области половых органов. Эти симптомы сопровождаются общим недомоганием, подъемом температуры, головной болью. На половых органах появляются маленькие пузырьки, которые наполнены жидкостью. Пузырьки лопаются и образуются болезненные красные язвочки. Заживают в течение двух недель.
Если случается рецидив заболевания, то он сопровождается подъемом температуры, к рецидивам может привести переохлаждение, стресс. Генитальный герпес протекает бессимптомно, возможно заражение мужа женой или наоборот.
Диагностика генитального герпеса: если вы планируете беременность, то вам нужно сдать анализ крови из вены на антитела класса IgM и IgG к вирусы простого герпеса.
Если согласно результатам анализа выявят антитела класса G – организм уже сталкивался с генитальным герпесом. Если же присутствуют антитела к иммуноглобулинам класса М — генитальный герпес находится в острой стадии.
Если же присутствуют антитела к иммуноглобулинам класса М — генитальный герпес находится в острой стадии.
Лечение генитального герпеса: лечиться нужно противовирусными препаратами, партнер также должен сдать анализ — он может быть не инфицирован. Во время беременности противовирусные препараты принимать нельзя, но обязательно проходить терапию иммуноглобулинами.
Чем опасен генитальный герпес при беременности
Первичное заболевание герпесом во время беременности самое опасное. Оно ведет к прерыванию беременности, а также к серьезным поражениям плода. Если беременная заражается этим вирусом незадолго до предполагаемого появления ребенка на свет, то врач отказывает в естественных родах, женщине делают кесарево сечение. При естественных родах же велик риск заражения ребенка при прохождении через родовые пути матери. Если заболевание находится в острой фазе, то ребенок с высокой вероятностью может заразиться, поэтому нужно пролечить своевременно.
Если обнаружили цитомегаловирус
Цитомегаловирус передается половым путем, также может быть передан от матери к плоду, возможна передача вируса через поцелуи, через кровь.
Цитомегаловирус протекает бессимптомно, через месяц-два мононуклеозоподобный синдром. Он похож на ОРВИ и грипп, сопровождается высокой температурой, ознобом, человек сильно утомляется, испытывает недомогание, у него болит голова.
Если же иммунитет ослаблен, то цитомегаловирус может стать причиной тяжелых заболеваний — поражения глаз, легких, пищеварительной системы и головного мозга.
Диагностика цитомегаловируса: он может быть выявлен по результатам анализа крови из вены на антитела класса IgM и IgG к цитомегаловирусу. Если фиксируются антитела к иммуноглобулинам класса М, то болезнь в острой стадии, если обнаружены антитела к иммуноглобулинам класса G, то организм уже встречался с данной инфекцией.
Лечение цитомегаловируса: женщине назначаются иммунные препараты, во время беременности проводится иммунотерапия с использованием разрешенных к применению препаратов.
Чем опасен цитомегаловирус во время беременности: опасно первичное заражение цитомегаловирусом во время беременности, оно может привести к инфицированию плода, к прерыванию беременности, к порокам развития плода.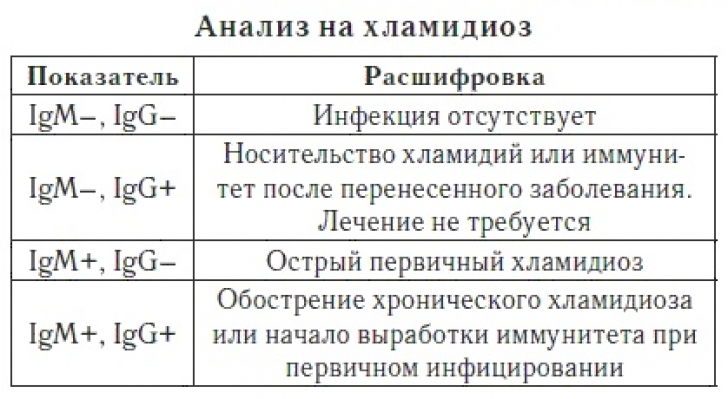 Лечение цитомегаловируса до беременности и во время беременности обязательно.
Лечение цитомегаловируса до беременности и во время беременности обязательно.
Как правильно сдавать анализа на выявление заболеваний, передающихся половым путем
Делайте это перед менструацией, сразу после нее. В такие дни иммунитет женщины снижается. За 20 дней до сдачи анализов нужно прекратить прием антибиотиков, перестать ставить свечи и т. д. Перед посещением врача не нужно подмываться, принимать душ.
Когда сдаются анализы?
В первый раз — до наступления беременности. Если обнаружат инфекцию, то нужно пройти лечение, затем повторно сдать анализы. В течение 3 недель половую жизнь нужно вести с презервативами. Одни из партнеров может не вылечиться.
После наступления беременности, вы встанете на учет к акушеру-гинекологу, врач еще раз предложит сдать анализы. Новые всплески возможны в период беременности, так как иммунитет женщины сильно ослабляется.
Если врач назначит несколько курсов антибиотиков подряд, чтобы пролечить одну и ту же инфекцию, то стоит задуматься — продолжать ли лечение у него, стоит поискать другую клинику.
Врач-акушер-гинеколог Куриленко Елена Георгиевна
Лабораторная диагностика микоплазменной инфекции — сдать анализы в СЗЦДМ
Микоплазменная инфекция (микоплазмоз) ― это болезнь, вызываемая бактериями микоплазмами. Они поражают многие ткани и внутренние органы. Могут долго и бессимптомно жить внутри организма, паразитируя на стенках и мембранах клеток. Но, как только иммунитет ослабевает, микоплазмы начинают активно размножаться.
Бактерии могут вызвать микоплазменную пневмонию, уретриты, пиелонефриты и другие воспалительные поражения в матке и маточных трубах, в суставах, кровотоке, нервной системе. Если процесс поражения микоплазмами будет генерализованным, возникнет риск развития ДВС-синдрома с поражением жизненно важных органов.
СимптомыПневмония, вызванная размножением микроплазмов, характеризуется следующей симптоматикой:
-
непродуктивный кашель;
-
першение в глотке и гортани;
-
ринит;
-
боль в ушах;
-
головная боль;
-
повышенная температура тела до +38 С;
-
общее недомогание, симптомы интоксикации.

Микоплазмы способствуют развитию синусита, отита, пневмонии и бронхита. Симптомы схожи с сезонными ОРВИ, поэтому диагностировать микоплазменную пневмонию только по внешним признакам нельзя.
Симптомы микоплазменного мочеполового поражения:
-
У мужчин:
-
прозрачные выделения по утрам;
-
покраснение, жжение уретры;
-
частое мочеиспускание (иногда ложные позывы).
-
У женщин:
-
усиление болезненности месячных;
-
увеличение количества влагалищных выделений;
-
дискомфорт при половом контакте.

Часто микоплазмоз и уреаплазмоз протекает малосимптомно, поэтому пациенты обращаются к врачу с уже запущенной болезнью. Воспалительные процессы негативно сказываются на течении беременности, могут стать причиной выкидыша, послеродовые и послеабортные осложнения. У мужчин приводят к значительным изменениям сперматозоидов, у беременной женщины способны вызывать необратимую трансформацию в хромосомном аппарате клеток плода.
Возбудитель заболеваний ― бактерии Микоплазмы (Mycoplasma). Открыто несколько видов микроорганизмов, 10 из них являются частью нормальной микрофлоры человека, но некоторые виды патогенные. К паразитирующим бактериям относятся:
-
Mycoplasma pneumonia вызывает болезни органов дыхания, среди которых трахеит, бронхит, атипичная пневмония. У 10 % больных заболевание приводит к воспалению легких. Инфицирование происходит при близком контакте, воздушно-капельным способом.

-
Mycoplasma genitalium и Ureaplasma urealyticum вызывает воспаления мочеполовой системы. Среди них уретрит, простатит, пиелонефрит, воспаление матки, маточных труб, яичников и придатков. Мужчинам передается исключительно половым путем.
-
Mycoplasma hominis считается условно патогенной бактерией. Пока официально не доказано ее влияние на развитие патологических процессов. Одни исследователи считают ее паразитирующим микроорганизмом, другие отрицают существенную роль в патогенезе человека.
Микоплазменная пневмония относится к группе атипичных пневмоний, которые большей частью проходят в легкой форме. Источником заражения служит больной человек и здоровый носитель. Заболевание передается воздушно-капельным путем. В основном болеют дети и взрослые до 35 лет.
Регистрируется болезнь в виде единичных случаев, но случаются эпидемические вспышки.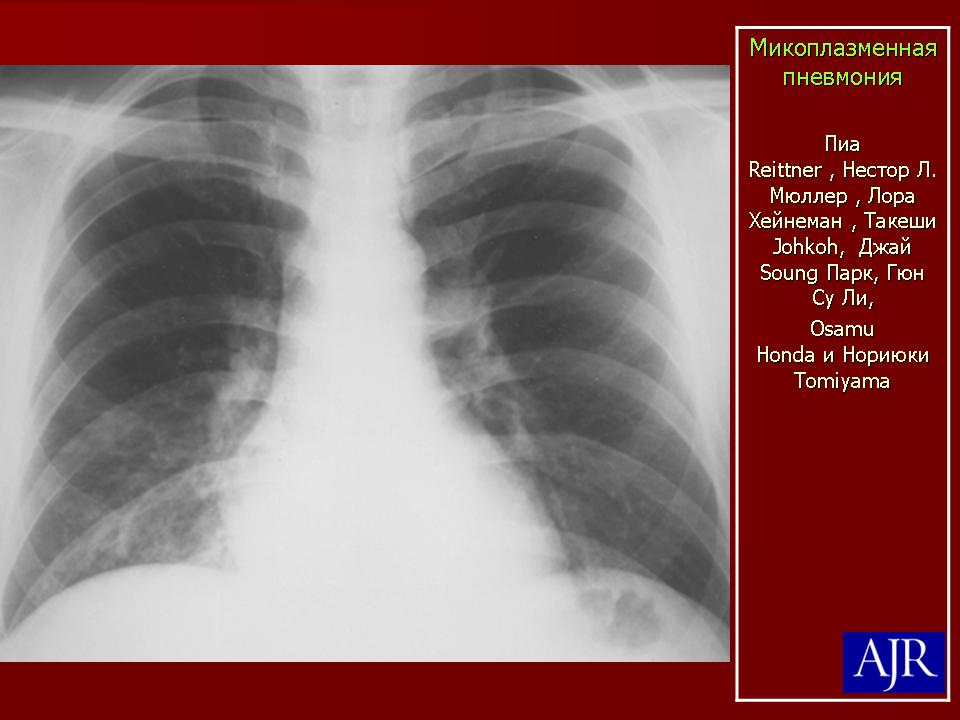 Например, в организованных рабочих, школьных и студенческих коллективах, в рамках одной семьи или военной части. Число больных увеличивается в осенне-зимний период.
Например, в организованных рабочих, школьных и студенческих коллективах, в рамках одной семьи или военной части. Число больных увеличивается в осенне-зимний период.
При микоплазменной пневмонии могут быть затронуты разные органы и ткани:
Иногда возникают аллергические реакции, выражающиеся в виде сыпи, покраснений, пузырьков. Увеличивается риск развития анемии, нарушение системы свертывания крови.
Микоплазменный бронхит встречается чаще, чем пневмония. Нередко приобретают затяжное течение до 8 недель. Кашель сухой, мучительный, сопровождающийся боль в горле и насморком. Иногда возникает конъюнктивит и отит. По симптоматике схож с другими сезонными заболеваниями. Для идентификации возбудителя и постановки правильного диагноза недостаточно одной клинической картины. Требуется проведение лабораторных анализов, рентгенографии и компьютерной томографии грудной клетки.
Инкубационный период микоплазменного бронхита и пневмонии индивидуальный, зависит от состояния организма. Длится от 5 до 28 суток, после чего начинают проявляться первые симптомы. Если болезнь протекает как сезонная простуда, развиваются синуситы и отиты, если в форме пневмонической болезни – плеврит, тромбофлебит, полиневрит, миокардит, тромбогеморрагический синдром и другие формы.
Длится от 5 до 28 суток, после чего начинают проявляться первые симптомы. Если болезнь протекает как сезонная простуда, развиваются синуситы и отиты, если в форме пневмонической болезни – плеврит, тромбофлебит, полиневрит, миокардит, тромбогеморрагический синдром и другие формы.
Прогноз при любом течении благоприятный, болезнь заканчивается полным выздоровлением. Образуется нестойкий, ослабевающий со временем иммунитет к микоплазмам. Вакцины не изобретено.
Инфекцию, вызываемую микоплазмами, называют уреаплазмозом. Источником заражения служит больной человек и здоровый носитель. Инфекция чаще передается половым путем при отсутствии средств контрацепции, реже бытовым через предметы общего и личного пользования. Например, заразиться микоплазмозом можно через полотенца, средства гигиены, мочалки, нестерильные медицинские шприцы, используя чужое белье.
Человек может длительное время быть бессимптомным носителем. Но, под воздействием внешних факторов болезнь рано или поздно даст о себе знать. Это произойдет в случае снижения иммунитета, например, из-за стресса, беременности, переохлаждения и других заболеваний.
Но, под воздействием внешних факторов болезнь рано или поздно даст о себе знать. Это произойдет в случае снижения иммунитета, например, из-за стресса, беременности, переохлаждения и других заболеваний.
В большинстве случаев микоплазмоза протекает в хронической форме, имеет слабо выраженную симптоматику. Скрытый период может длиться как несколько дней, так и несколько лет. У мужчин патологические процессы затрагивают мочеиспускательный канал, простату, семенники, мочевой пузырь, яички. У женщин страдают уретра, вестибулярные железы, влагалище, яичники, матка и маточные трубы. Часто больные обращаются за медицинской помощью, когда симптоматика становится явной.
У мужчин на фоне микоплазмоза развиваются следующие заболевания:
У большинства женщин заболевание также проходит бессимптомно. Только некоторые отмечают, что менструации стали более болезненными, возникает тянущее чувством внизу живота, болит в районе поясницы. Микоплазменная инфекция может стать причиной выкидыша, преждевременных родов. У инфицированных новорожденных микоплазмоз может вызвать воспаление легких, оболочек головного мозга.
У инфицированных новорожденных микоплазмоз может вызвать воспаление легких, оболочек головного мозга.
Длительное носительство бактерий приводит к бесплодию у представителей обоих полов.
Определить наличие инфекции, вызванной микоплазмами можно лабораторными анализами. Основное значение имеют молекулярно-биологические методы диагностики ПЦР, направленные на выявление генетического материала патогена. Для анализа берут такие биоматериалы, как мазок урогенитальный и из носоглотки, мокрота, эякулят, спинномозговой ликвор, суставная жидкость и иное.
Второй по важности, один из наиболее часто используемых методов ― серологическая иммуноферментная диагностика (ИФА). Его используют для выявления нарастания антител в динамике заболевания. Биоматериал ― венозная кровь. Результат зависит от того, какие титры антител повышены:
-
Если IgM ― значит, человек впервые заболел микоплазменной инфекцией в острой форме.
 Возбудитель присутствует в организме непродолжительное время.
Возбудитель присутствует в организме непродолжительное время.
-
Если IgA ― показатель повышается при наличии инфекции, длящейся какое-то время.
-
Если IgG ― недавно была перенесена инфекция либо болезнь перешла в хроническую стадию.
Для диагностирования микоплазменной и уреаплазменной инфекции, выявления локализации и степени воспаления проводят следующие тесты:
-
Общий анализ крови. Во время инфицирования микоплазмами повышается уровень лейкоцитов.
-
СОЭ. Значение повышается при наличии микоплазменной инфекции.
-
Общий анализ мочи. Позволяет выявить наличие воспалений мочеполовой системы. Характер изменения мочи показывает какой орган наиболее поражен.
Отдельно стоит выделить анализ на посев. Его особенность состоит в том, что собранный биоматериал помещают в питательную среду. Затем, выращенные микоплазмы можно разделить и опробовать на них разные антибактериальные препараты. Таким образом, анализ позволяет не только диагностировать микоплазменную инфекцию, но и подобрать оптимальные для лечения медикаменты.
Немаловажный этап ― выявление осложнений в органах мочеполовой системы. Необходимо определить состояние мочевого пузыря, простаты, семенных пузырьков у мужчин. Для этого проводят исследование мочи, секрета простаты, выполняют спермограмму, урофлоуметрию, УЗИ. Женщины также сдают мочу, проходят кольпоскопию и УЗИ органов малого таза.
После перенесенной пневмонии и бронхита стоит выполнить рентгенографию органов грудной клетки. Это позволит выявить наличие изменения в легочной ткани. Определить наличие изменений внутренних органов, наличие патологических новообразований, вызванных микоплазменной инфекции поможет комплексное ультразвуковое исследование.
Микоплазмы погибают от антибиотиков. Поэтому лечение базируется на приеме антибактериальных препаратов подобранных в индивидуальном порядке. Как правило, используют следующие препараты, вводимые внутримышечно и внутривенно.
Симптоматическая терапия включает обильное питье, витамины, иммунобиологические медикаменты, жаропонижающие средства, антигистамины, бронхолитические и отхаркивающие препараты. Длительность и интенсивность лечения зависит от клинической картины. Легкие формы заболевания наблюдаются амбулаторно, у терапевта, педиатра, уролога, гинеколога. Может потребоваться полупостельный режим.
Тяжелые случаи микоплазмоза наряду с наличием острых осложнений, вызванных инфекцией, подлежат терапии в условиях стационара. Как правило, это больные бронхитом, пневмонией, ларинготрахеитом и пациенты не получившие терапевтического эффекта от надомного лечения. Иногда размещение в стационаре выбирают по эпидемическим показаниям. Запрещается заниматься самолечением, принимать препараты следует только по назначению врача, в указанных дозах.
После прохождения лечения у пациентов нарушается микрофлора в качественных и количественных показателях. Поэтому врач назначает прием пробиотических средств в течение 14 дней. Для восстановления микрофлоры стоит отдать предпочтение препаратам, включающим сразу несколько видов пробиотиков.
Профилактика
Снизить вероятность инфицирования органов дыхания микоплазменной инфекцией можно соблюдая правила, используемые при эпидемиях гриппа и ОРВИ. К ним относится:
-
исключение посещения многолюдных мест;
-
исключение контакта с инфицированными людьми;
-
ношение одноразовых масок;
-
соблюдение норм гигиены;
-
соблюдение режима дня;
-
правильное, сбалансирование питание;
-
проветривание помещения, прогулки на свежем воздухе.
Для предотвращения заражения мочеполовой системы необходимо использовать презервативы. Если произошел незащищенный контакт, обратиться к медику для сдачи анализов. Также следует исключить из пользования чужое белье, одежду, средства гигиены.
В Северо-Западном центр доказательной медицины можно сдать комплекс анализов на микоплазменную инфекцию. Сдать биоматериал можно в Центре или на дому, вызвав медработника.
Исследования проводятся в собственная лаборатории с новейшим оборудованием, а потому вам гарантировано:
В АО «СЗЦДМ» работает доброжелательный персонал и квалифицированные специалисты. Лабораторные терминалы и медицинские центры расположены в места с удобной транспортной развязкой. Они присутствую в Санкт-Петербурге и городах Ленинградской области, Великом Новгороде и Новгородской области, Пскове, Калининграде и Балтийске.
Анализы
Согласно новому исследованиюНовое австралийское исследование показало, что если женщины принимают антибиотики во время беременности, риск инфицирования младенцев выше, если беременные мамы принимают антибиотики, по сравнению с тем детям, мамы которых не принимали лекарство.
Ключевые моменты:
- Дети, рожденные от мам, принимающих антибиотики, подвержены более высокому риску заражения
- Риск увеличивается, если дети мужского пола и родились естественным путем
- Исследователи говорят, что беременным женщинам не следует прекращать прием антибиотиков
Профессор Дэвид Бургнер из Детского научно-исследовательского института Мердока провели исследование, в котором рассматривались данные о более чем 750 000 беременностей с 1997 по 2009 год в Дании.
Ученые сверяли записи о рождении с использованием антибиотиков матерью и госпитализацией детей с инфекциями.
«Мы обнаружили, что дети, рожденные от матерей, которым во время беременности прописывали антибиотики, могут иметь на 20 процентов более высокий риск госпитализации с инфекцией», — сказал он.
Они обнаружили, что чем больше антибиотиков принимала мама и чем ближе была дата родов, тем выше риск.
«Мужчины подвергались более высокому риску заражения, если их матери принимали антибиотики, и повышенный риск для обоих полов сохранялся на протяжении всего детства», — сказал он.
Получили конфиденциальную новость?
- Отправить электронное письмо ABC Investigations по адресу [email protected]
Для получения более конфиденциальной информации:
- Текстовое сообщение с помощью телефонного приложения Signal +614369 072
Нет системы 100 на cent secure, но приложение Signal использует сквозное шифрование и может защитить вашу личность. Пожалуйста, ознакомьтесь с условиями.
Но исследователи подчеркнули, что результаты следует интерпретировать с осторожностью.
«Мы не говорим беременным женщинам« не принимайте антибиотики », просто их следует использовать осторожно во время беременности», — сказал профессор Бургнер.
Ведущий автор доктор Джессика Миллер сказала, что исследователи не совсем уверены в причине повышенного риска.
Они сказали, что, возможно, антибиотики влияют на состав бактерий в кишечнике матери, известный как микробиом кишечника.
«Воздействие на микробиом кишечника может повысить восприимчивость к инфекциям в раннем детстве, возможно, из-за неоптимального развития», — сказала она.
Объяснение устойчивости к антибиотикам
Почему ваши решения важны в борьбе с супербактериями.
ПодробнееСпособ рождения ребенка также имеет значение, поскольку у детей, рожденных естественным путем, риск развития инфекций несколько выше.
Причина в том, что при естественных родах младенцы подвергаются воздействию микробиома матери, а младенцы, рожденные путем кесарева сечения, — нет.
Президент Австралийской медицинской ассоциации и акушер доктор Майкл Гэннон сказал, что врачи не могут прекратить давать беременным женщинам антибиотики.
«Беременным женщинам необходимо принимать антибиотики при инфекциях, таких как инфекции мочевыводящих путей, или при хирургических вмешательствах», — сказал он.
«Но весьма вероятно, что антибиотики могут изменить бактерии матери».
Профессор Бургнер сказал, что результаты показывают, что прием антибиотиков во время беременности может иметь более долгосрочные последствия как для матери, так и для младенцев.
«Если затронут микробиом кишечника, вы можете вмешаться и дать матери и ребенку пробиотики», — сказал он.
Но он предупредил, что пока недостаточно научных данных, чтобы рекомендовать пробиотики для снижения риска детских инфекций.
Исследователи обнаружили, что у детей от новорожденных до 14 лет, рожденных от женщин, которым прописали антибиотики ближе к рождению или прописали более одного курса антибиотиков во время беременности, был еще больший риск заражения.
Старший химик-исследователь Центра по борьбе с насекомыми при Университете Квинсленда, доктор Марк Бласкович, сказал, что исследование выявило связанные и неожиданные опасности, вызванные приемом антибиотиков.
«Один из побочных эффектов заключается в том, что антибиотики могут убить полезные бактерии, которые естественным образом живут в вашем теле, особенно в кишечнике», — сказал он.
«Авторы обнаружили, что этот эффект« изменения микробиома », вызванный приемом антибиотиков во время беременности, может передаваться и подвергать риску здоровье родившегося ребенка на протяжении всего его детства».
Он сказал, что, хотя повышенный риск невелик, он показывает, что использование антибиотиков может иметь непредвиденные и потенциально долгосрочные последствия.
Исследование было опубликовано в Международном журнале эпидемиологии.
Mycoplasma — Лабораторные тесты онлайн AU
Как это используется?
Тестирование на микоплазмы в основном используется для определения того, является ли Mycoplasma pneumoniae причиной инфекции дыхательных путей. Его также можно использовать для диагностики инфекции, причиной которой, как считается, является микоплазма.
Анализы крови на антитела к M. pneumoniae
Два типа произведенных в ответ на M.pneumoniae можно измерить в крови и. Альтернативно, во многих лабораториях общее количество продуцируемых антител можно измерять вместе. Антитела IgM первыми вырабатываются организмом в ответ на инфекцию. Уровни IgM повышаются в течение короткого периода времени, а затем снижаются, часто обнаруживаясь в крови в течение нескольких месяцев. Продукция антител IgG следует за производством IgM, со временем возрастая, а затем стабилизируясь. После заражения микоплазмой у человека обычно остается некоторое измеримое количество антител IgG к микоплазме в крови на всю оставшуюся жизнь.Чтобы диагностировать активную инфекцию M. pneumoniae , врач может назначить тесты на антитела M. pneumoniae IgM и IgG, а затем через две-четыре недели собрать еще один тест M. pneumoniae IgG в качестве a. Эта комбинация тестов организована таким образом, чтобы можно было оценить изменение количества антител IgG и потому, что некоторые люди, особенно младенцы и люди с ослабленной иммунной системой, могут не производить ожидаемых количеств IgG или IgM.
Прямое обнаружение
M.Обнаружение pneumoniae включает обнаружение микроорганизма в респираторном секрете, крови, жидкости или образце ткани. Это может быть сделано либо микоплазмой в поддерживающей среде, либо путем обнаружения ее генетического материала ().
Посев на микоплазмы — традиционный метод обнаружения, но он может быть проблематичным для лаборатории и поэтому выполняется нечасто. Существуют определенные потребности в питании, которые необходимо удовлетворить, чтобы способствовать росту микроорганизмов, и они могут расти медленно.Например, отрицательная культура M. pneumoniae на должна храниться в течение трех-четырех недель, чтобы подтвердить отсутствие микоплазмы. Тестирование на антитела или ДНК-тестирование обычно заказывают в дополнение к культуре M. pneumoniae или вместо нее.
ДНК-тестирование является быстрым и чувствительным и все чаще используется для диагностики микоплазменных инфекций. ДНК может быть обнаружена после того, как симптомы инфекции исчезнут и организмы станут нежизнеспособными. М.pneumoniae ДНК может быть заказан вместе с другими тестами, такими как тестирование на Chlamydia pneumoniae , Bordetella pertussis и Legionella видов , чтобы помочь различить эти организмы как причину респираторной инфекции.
Иногда можно использовать анализ ДНК, чтобы определить, является ли Mycoplasma hominis , Mycoplasma genitalium или Ureaplasma urealyticum причиной инфекции половых или мочевыводящих путей.Образцы гениталий M. hominis и U. urealyticum обычно тестируются с использованием метода культивирования, который занимает несколько дней для восстановления микроорганизмов, но M. genitalium , рост которого может занять от одного до двух месяцев, обнаруживается более надежно. с тестированием ДНК.
Выбор тестов и собранных образцов тела зависит от возраста пациента, его общего состояния здоровья и симптомов, а также от клинических данных врача и подозрений на поражение органов.Человек с подозрением на микоплазменную инфекцию может лечиться на основании клинических данных и визуальных исследований с лабораторным тестированием или без него.
Когда это требуется?
Исследование M. pneumoniae может быть назначено, если у кого-то есть респираторные симптомы, не связанные с типичной инфекцией, например пневмококковой пневмонией. Некоторые из этих симптомов могут включать:
- непродуктивный кашель, который может сохраняться в течение нескольких недель
- лихорадка
- ангина
- головные и мышечные боли
Тестирование также может быть выполнено для выявления причины сыпи, артрита, энцефалита, воспаления сердечной мышцы или внутренней оболочки сердца или гемолитической анемии.Ему также может быть приказано отслеживать и контролировать распространение инфекции M. pneumoniae во время вспышки.
Как правило, тестирование проводится, когда врач подозревает, что у кого-то есть активная инфекция M. pneumoniae , и через две-четыре недели можно провести еще один тест на IgG, чтобы зафиксировать повышение уровня антител в ответ на инфекцию. При подозрении на активную инфекцию можно также назначить M. pneumoniae или тест.
Анализ образцов гениталий проводится нечасто, поскольку микоплазмы часто являются частью половых путей.Однако культивирование на M. hominis и U. urealyticum или тест на ДНК M. genetalium иногда назначают, когда у сексуально активного мужчины наблюдается воспаление, которое не связано с гонореей или хламидиозом (негонококковой инфекцией). уретрит, NGU) или когда у женщины есть подозрение на инфекцию генитальной или тазовой микоплазмы.
Микоплазмы — частые причины инфицирования околоплодных вод во время беременности. Это может привести к преждевременным родам, повышению температуры после родов и инфекциям у новорожденного.Тестирование на другие виды микоплазмы может проводиться в дополнение к тесту M. pneumoniae , когда у очень маленьких детей и детей с ослабленной иммунной системой есть легкие и / или инфекции или осложнения, которые могут быть вызваны инфекцией микоплазмы.
Что означает результат теста?
Тестирование антител
Значительные концентрации M. pneumoniae и / или четырехкратное увеличение уровней между исходным образцом и концентрацией указывают на активный или недавний M. pneumoniae .pneumoniae инфекция. Повышение уровня IgG без IgM также можно увидеть при повторном инфицировании.
Если ни IgM, ни IgG не присутствуют в определяемых концентрациях, это означает, что у человека нет активной инфекции, не было инфекции микоплазмы (недавней или в прошлом), или что иммунная система человека не вырабатывала антитела в ответ на микроорганизм.
Прямое обнаружение
Обнаружение одной из микоплазм или U.urealyticum в культуральном образце может указывать на то, что у кого-то есть инфекция микоплазмы, особенно если образец взят из места в организме, которое обычно является стерильным, например суставной жидкости или крови. Однако, если образец взят из дыхательных путей или половых путей, положительный результат посева может также означать, что микоплазма присутствует как часть. Например, U. urealyticum присутствует в половых путях примерно у 60 процентов здоровых женщин, а M. hominis присутствует примерно у 20 процентов.
Если микоплазма не обнаружена в культуре, это может означать, что соответствующее лицо не инфицировано этим микроорганизмом или что организм не присутствует в достаточном количестве для обнаружения в исследуемой пробе.
При тестировании ДНК на M. pneumoniae , если микоплазма присутствует в образце, у человека может быть M. pneumoniae или это может быть организм. Если он не обнаружен, у них может не быть инфекции M. pneumoniae , или же микроорганизм присутствовал в слишком малом количестве, чтобы его можно было обнаружить.
Что еще мне следует знать?
Инфекции, вызванные микоплазмами, часто вызывают симптомы, напоминающие инфекции, но они поддаются лечению антибиотиками.
Инфекция микоплазмы не дает иммунитета. Человек может заразиться повторно.
Микоплазмы нельзя увидеть под микроскопом при окраске по Граму — тест, который часто используется для идентификации.
Иногда можно заказать более старый тест, называемый холодными агглютининами, для обнаружения M.pneumoniae инфекция. Он основан на концепции, что во время активной микоплазменной инфекции в крови вырабатывается в крови, которая вызывает слипание эритроцитов при охлаждении. Этот тест не специфичен для микоплазмы, но более половины пациентов с инфекцией M. pneumoniae будут иметь значительное количество холодовых агглютининов.
ПрименениеXENLETA® (лефамулин) обеспечивает быстрое время до клинического ответа у госпитализированных пациентов с внебольничной бактериальной пневмонией (CABP)
ДУБЛИН, Ирландия, 5 мая 2020 г. (GLOBE NEWSWIRE) — Nabriva Therapeutics plc (NASDAQ: NBRV), биофармацевтическая компания, занимающаяся коммерциализацией и разработкой инновационных противоинфекционных средств для лечения серьезных инфекций, объявила сегодня, что Open Forum Infectious Diseases , официальный журнал Общества инфекционных болезней Америки (IDSA), опубликовал результаты ретроспективного анализа клинических данных пациентов, начавших лечение в больнице, по результатам основных клинических испытаний Lefamulin Evaluation Against Pneumonia (LEAP) 1 и LEAP 2 Phase 3.Анализы показывают, что лефамулин дает быстрое и сходное время до клинического ответа, что является показателем «готовности к выписке» по сравнению с моксифлоксацином.
«Существует очевидная потребность в новых антибиотиках для пациентов с CABP, которые приводят к таким же результатам в реальном мире, как фторхинолоны, без проблем с безопасностью», — сказал д-р Томас Лодис, фармацевт, PhD Колледж фармации и здравоохранения Олбани, и руководитель автор исследования. «Лефамулин не уступает моксифлоксацину в лечении взрослых с CABP в двух международных клинических испытаниях.Текущий анализ показывает, что госпитализированные взрослые с CABP, получавшие лефамулин, быстро достигают критериев готовности к выписке. Учитывая опасения по поводу безопасности фторхинолонов, эти результаты добавляют к растущему количеству доказательств того, что лефамулин следует рассматривать как потенциальную замену монотерапии респираторными фторхинолонами ».
В ретроспективном анализе исследователи изучили объединенные данные 926 стационарных пациентов из испытаний LEAP; 468 пациентов получали лефамулин и 458 — моксифлоксацин.В ходе анализа оценивались три исхода среди исследуемой популяции: время до клинического ответа, время до клинической стабильности и время до клинического улучшения.
Из 926 включенных пациентов исследователи смогли оценить время до клинического ответа у 918, клиническую стабильность у 925 и клиническое улучшение у 923. Анализы показали, что время до клинического ответа было почти одинаковым в обеих группах лечения со средним значением ( межквартильный размах) время от начала лечения до клинического ответа 4 (3-4) дня для лефамулина и 4 (3-5) дней для моксифлоксацина.Среднее время от начала лечения до клинической стабильности или клинического улучшения составляло 3 (2-4) дня в группах как лефамулина, так и моксифлоксацина.
Учитывая связь между временем до клинического ответа и готовностью к выписке у пациентов с CABP, полученные данные подтверждают потенциал лефамулина как эффективной внутривенной и пероральной краткосрочной монотерапии CABP, которая может способствовать ранней выписке.
«При лечении госпитализированных пациентов с CABP продолжительность пребывания является основным фактором, влияющим на стоимость лечения», — сказал д-р.Лодис. «Инновационные антибиотики, такие как лефамулин, которые являются безопасными и эффективными, и, как было доказано, обеспечивают быстрое время до клинического ответа, имеют решающее значение для предоставления нашим пациентам наиболее рентабельной и высококачественной помощи».
XENLETA ™ — это первый в своем классе антибиотик плевромутилин, одобренный Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA) для лечения внебольничной бактериальной пневмонии. Он доступен в виде внутривенных и пероральных форм, позволяющих начать лечение в больнице, перейти к амбулаторному лечению или начать лечение по месту жительства.XENLETA обладает новым механизмом действия, направленным на сайт связывания бактерий, который отличается от существующих антибиотиков, который, как было показано, не приводит к перекрестной устойчивости к другим классам антибиотиков, обычно назначаемых для CABP, и имеет низкий потенциал для развития устойчивости.
Полные результаты апостериорного анализа данных испытаний LEAP включены в документ под названием: Пост-хирургическая оценка времени до клинического ответа среди взрослых, госпитализированных с внебольничной бактериальной пневмонией, которые получали лефамулин или моксифлоксацин в двух рандомизированных фазах III. , Double-Blind, Double-Dummy Clinical Trials , опубликовано в Open Forum Infectious Diseases, 24 апреля 2020 г.
О CABP
Пневмония — это инфекция легких, которая может быть серьезной и смертельной, особенно у пожилых пациентов с сопутствующими заболеваниями. Ежегодно в США регистрируется около пяти миллионов случаев пневмонии, при этом пневмония является пятой по значимости причиной госпитализации и одной из основных причин смерти, связанной с инфекциями. Streptococcus pneumoniae является наиболее частой причиной бактериальной пневмонии в США.Согласно последним данным программы SENTRY Antimicrobial Surveillance Programme в США, США.S. примерно от 30 до 60 процентов из S. pneumoniae , в зависимости от региона, устойчивы к макролидам. Помимо макролидов, фторхинолоны — еще один распространенный вариант лечения CABP. Этот класс широкого спектра — эффективный вариант; тем не менее, фторхинолоны содержат предупреждения о некоторых серьезных проблемах безопасности.
О XENLETA
XENLETA (лефамулин) — первый в своем классе полусинтетический антибиотик плевромутилин для применения у людей, открытый и разработанный группой Nabriva Therapeutics.Он разработан для подавления синтеза бактериального белка, необходимого для роста бактерий. Связывание XENLETA происходит с высокой аффинностью, высокой специфичностью и на молекулярных сайтах, которые отличаются от других классов антибиотиков. Эффективность XENLETA была продемонстрирована в двух многоцентровых, многонациональных, двойных слепых, двойных манекенах, не меньшей эффективности, в которых оценивали в общей сложности 1289 пациентов с АКШ. В этих испытаниях XENLETA сравнивали с моксифлоксацином, а в одном испытании — с моксифлоксацином с линезолидом и без него.Пациенты, получавшие XENLETA, имели те же показатели эффективности, что и пациенты, принимавшие только моксифлоксацин или моксифлоксацин плюс линезолид. Наиболее частые побочные реакции, связанные с XENLETA, включают диарею, тошноту, реакции в месте инъекции, повышение ферментов печени и рвоту. Для получения дополнительной информации посетите www.xenleta.com .
О компании Nabriva Therapeutics plc
Nabriva Therapeutics — биофармацевтическая компания, занимающаяся коммерциализацией и разработкой инновационных противоинфекционных средств для лечения серьезных инфекций.Nabriva Therapeutics получила одобрение Управления по санитарному надзору за качеством пищевых продуктов и медикаментов США на XENLETA (лефамулин), первый плевромутилин-антибиотик от внебольничной бактериальной пневмонии (CABP). Nabriva Therapeutics также разрабатывает Contepo ™ (фосфомицин) для инъекций, потенциальный первый в своем классе эпоксидный антибиотик для лечения осложненных инфекций мочевыводящих путей (cUTI), включая острый пиелонефрит. Для получения дополнительной информации посетите https://www.nabriva.com .
ПОКАЗАНИЯ И ВАЖНАЯ ИНФОРМАЦИЯ ПО БЕЗОПАСНОСТИ
ПОКАЗАНИЯ
XENLETA — это антибактериальный препарат плевромутилина, показанный для лечения взрослых с внебольничной бактериальной пневмонией (CABP), вызванной следующими восприимчивыми микроорганизмами (пневмококками, стрептококками) -чувствительные изоляты), Haemophilus influenzae, Legionella pneumophila, Mycoplasma pneumoniae и Chlamydophila pneumoniae.
ИСПОЛЬЗОВАНИЕ
Чтобы уменьшить развитие лекарственно-устойчивых бактерий и сохранить эффективность XENLETA и других антибактериальных препаратов, XENLETA следует использовать только для лечения или предотвращения инфекций, которые, как доказано или сильно подозреваются, вызваны чувствительными бактериями.
ВАЖНАЯ ИНФОРМАЦИЯ ПО БЕЗОПАСНОСТИ
ПРОТИВОПОКАЗАНИЯ
XENLETA противопоказан пациентам с известной гиперчувствительностью к XENLETA или плевромутилинам.
Таблетки XENLETA противопоказаны для использования с субстратами CYP3A4, которые удлиняют интервал QT.
ПРЕДУПРЕЖДЕНИЯ И МЕРЫ ПРЕДОСТОРОЖНОСТИ
XENLETA может увеличивать интервал QT. Избегайте применения XENLETA у пациентов с известным удлинением интервала QT, желудочковой аритмией и пациентов, получающих препараты, которые могут удлинить интервал QT.
На основании исследований на животных, XENLETA может нанести вред плоду. Сообщите женщинам о репродуктивном потенциале потенциального риска для плода и используйте эффективную контрацепцию.
О диарее, связанной с Clostridium-difficile (CDAD), сообщалось при применении почти всех системных антибактериальных средств, включая XENLETA, с степенью тяжести от легкой диареи до фатального колита. Определите, возникает ли диарея.
ПОБОЧНЫЕ РЕАКЦИИ
Наиболее частыми побочными реакциями (≥2%) для (a) инъекции XENLETA являются реакции в месте введения, повышение уровня печеночных ферментов, тошнота, гипокалиемия, бессонница и головная боль и (b) таблетки XENLETA — диарея, тошнота, рвота и повышение уровня печеночных ферментов.
ИСПОЛЬЗОВАНИЕ В КОНКРЕТНЫХ ГРУППАХ НАСЕЛЕНИЯ
У пациентов с тяжелой печеночной недостаточностью уменьшите дозу инъекции XENLETA до 150 мг, вводимой в течение 60 минут каждые 24 часа. Таблетки XENLETA не рекомендуются пациентам с умеренной или тяжелой печеночной недостаточностью из-за недостаточной информации для предоставления рекомендаций по дозировке.
Избегайте инъекций XENLETA и таблеток с сопутствующими сильными или умеренными индукторами CYP3A или P-gp. Следите за снижением эффективности XENLETA.
Избегайте таблеток XENLETA с сильными ингибиторами CYP3A или P-gp.
Монитор побочных реакций чувствительных субстратов CYP3A, вводимых с таблетками XENLETA.
XENLETA не изучалась у беременных. Проверьте статус беременности у женщин до начала приема XENLETA и посоветуйте женщинам использовать контрацепцию во время лечения и в течение 2 дней после последней дозы. Кормящим женщинам следует сцеживать молоко и отказываться от него на время лечения XENLETA и в течение 2 дней после последней дозы.
Чтобы сообщить о ПОДОЗРЕВАЕМЫХ ПОБОЧНЫХ РЕАКЦИЯХ или применении во время беременности, свяжитесь с Nabriva Therapeutics US, Inc. по телефону 1-855-5NABRIVA или FDA по телефону 1-800-FDA-1088 или www.fda.gov/medwatch .
См. Полную информацию о предписаниях для XENLETA.
Заявления о перспективах
Любые заявления в этом пресс-релизе о будущих ожиданиях, планах и перспективах Nabriva Therapeutics, включая, помимо прочего, заявления о ее способности успешно запустить и коммерциализировать XENLETA для лечения CABP, включая наличие и простота доступа к XENLETA через основные U.S. специализированные дистрибьюторы, эксклюзивность маркетинга и патентная защита для XENLETA, разработка CONTEPO для cUTI, клиническая применимость XENLETA для CABP и CONTEPO для cUTI, планы и сроки рассмотрения нормативных документов для CONTEPO, усилия по внедрению CONTEPO выхода на рынок, рыночных возможностей и потенциального принятия на рынке XENLETA для CABP и CONTEPO для cUTI, разработки XENLETA и CONTEPO для дополнительных показаний, разработки дополнительных формулировок XENLETA и CONTEPO, планов по выпуску лефамулина в Китае, планы для проведения исследований и разработок других продуктов-кандидатов, ожиданий относительно способности клиентов удовлетворить спрос на XENLETA с их существующими запасами, достаточности существующих денежных ресурсов Nabriva Therapeutics и ее ожиданий в отношении ожидаемых доходов от продаж продуктов и того, как далеко в будущем существующие денежные ресурсы будут использоваться для финансирования текущих операций и других государственных nts, содержащие слова «предполагать», «полагать», «оценивать», «ожидать», «намереваться», «может», «планировать», «прогнозировать», «проект», «цель», «потенциал», «вероятно» , »« Будет »,« будет »,« мог бы »,« должен »,« продолжать »и подобные выражения составляют прогнозные заявления в значении Закона о реформе судебных разбирательств по частным ценным бумагам 1995 года.Фактические результаты могут существенно отличаться от тех, которые указаны в таких прогнозных заявлениях в результате различных важных факторов, включая: способность Nabriva Therapeutics успешно реализовать свои планы коммерциализации XENLETA и соответствие рыночного спроса на XENLETA ее ожиданиям, Nabriva Therapeutics ‘способность создавать и поддерживать торговый персонал для XENLETA, содержание и сроки решений, принимаемых Управлением по контролю за продуктами и лекарствами США и другими регулирующими органами, неопределенности, присущие началу и проведению клинических испытаний, доступность и время получения данных из клинических испытания, будут ли результаты ранних клинических испытаний или исследований по различным показаниям заболевания указывать на результаты текущих или будущих испытаний, неопределенности, связанные с регулирующим обзором клинических испытаний и заявок на получение маркетинговых разрешений, доступность или коммерческий потенциал CONTEPO для лечения cUTI, способность сохранять и нанять ключевой персонал, наличие адекватного дополнительного финансирования на приемлемых условиях или вообще, а также другие важные факторы, указанные в годовых и квартальных отчетах Nabriva Therapeutics и других документах, хранящихся в U.S. Комиссия по ценным бумагам и биржам. Кроме того, заявления о перспективах, включенные в этот пресс-релиз, отражают точку зрения Nabriva Therapeutics на дату этого пресс-релиза. Nabriva Therapeutics ожидает, что последующие события и события приведут к изменению ее взглядов. Однако, хотя Nabriva Therapeutics может решить обновить эти прогнозные заявления в какой-то момент в будущем, она специально отказывается от каких-либо обязательств в отношении этого. На эти прогнозные заявления не следует полагаться как на представление взглядов Nabriva Therapeutics на любую дату, следующую за датой этого пресс-релиза.
КОНТАКТЫ:
Инвесторам
Гэри Сендер
Nabriva Therapeutics plc
[email protected]
Для СМИ
Майк Бейер
Sam Brown Inc.
[email protected] 900 -961-2502
Когда кашель просто не проходит — Harvard Health Blog
У кого никогда не было кашля? Бьюсь об заклад, никто не может поднять руку. Мы постоянно наблюдаем это в клинике.Но хронический кашель, который длится не менее восьми недель, может быть трудным для пациентов и врачам трудно понять.
В выпуске журнала New England Journal of Medicine от 20 октября 2016 года специалисты по легочным заболеваниям описывают пошаговый подход, который врачи могут использовать для лечения пациентов с хроническим кашлем. Чаще всего продолжительный кашель происходит из-за одного из «обычных подозреваемых». Но когда это не так, у нас есть длинный список все более редких состояний, которые мы должны пройти и исключить.Если это не из-за какого-либо из и тех , эксперты теперь признают, что виновником может быть гиперактивность нервов, вызывающая повышенную реакцию кашля на определенные триггеры.
«Обычные подозреваемые», у которых может быть хронический кашельАвторы описывают типичную пациентку с хроническим кашлем, и она очень похожа на многих моих пациентов. Это женщина средних лет, у которой много месяцев кашель. Конечно, сначала мы хотим задать много вопросов.
- Были ли у нее симптомы хронической аллергии, такие как зуд, слезотечение и нос, заложенность носа и постназальное выделение? Если да, то стоит попробовать антигистаминные препараты и назальные стероиды.Недостаточное лечение аллергии может привести к хронической инфекции носовых пазух, которая вызывает кашель из-за постназального выделения, поэтому мы можем лечить и от этого заболевания.
- Может ли она болеть «кашлевой» астмой, которая вызывает кашель, но не хрипит? Многие из моих пациентов предпочли бы не ждать приема у легочного специалиста и проходить необычные тесты. Итак, если мы подозреваем кашлевую астму, мы просто начинаем использовать ингаляторы. Несколько недель ингаляционного приема альбутерола для открытия дыхательных путей и стероидного ингалятора для подавления воспаления могут помочь как в диагностике, так и в лечении проблемы.
- У нее симптомы изжоги? Кислотный рефлюкс также может спровоцировать кашель, и если кто-то описывает симптомы изжоги или даже если мы не уверены, что вызывает кашель, мы часто назначаем восьминедельные препараты, снижающие кислотность.
- Принимает ли она лекарства, побочным эффектом которых является кашель? Лизиноприл или другое лекарство от артериального давления из класса ингибиторов АПФ может вызывать кашель у 20% пациентов.Может потребоваться испытательный период для этого лекарства.
- Находится ли она среди 17% американцев, которые курят сигареты ? Если это так, то ее кашель может быть вызван хроническим бронхитом, когда кумулятивное повреждение легких препятствует нормальной способности организма очищать частицы, дыхательные пути набухают и выделяют чрезмерное количество слизи, и в конечном итоге участки отмирают и оставляют «мертвое пространство». У курильщика другие симптомы кашля могут вызывать опасения по поводу легочной инфекции или даже рака.
- Есть ли у нее другие риски или состояния для здоровья? Если она находилась в заключении или в приюте, или, возможно, из страны с ограниченными ресурсами, мы рассматриваем туберкулез (ТБ). Если у нее также ослаблена иммунная система из-за ВИЧ или длительного приема кортикостероидов, в список входят туберкулез и множество других необычных организмов.
- Мы в тупике? Редкие состояния, которые следует учитывать, включают фиброз легких, саркоидоз, аутоиммунные заболевания и анатомические аномалии.Дополнительное обследование должно включать осмотр легких и ЛОР.
Но что мы делаем для пациентов, которые либо не реагируют на лечение своих общих состояний, либо для которых тщательная оценка исключает менее распространенные причины хронического кашля? Что ж, теперь исследователи описывают новую группу состояний дыхания и кашля, вызванных дисфункцией нервов.
Новые данные свидетельствуют о том, что постназальный отек, кислотный рефлюкс или даже сильный кашель сами по себе могут ухудшить состояние нервных окончаний в «кашлевых центрах» дыхательных путей.Эти обостренные нервные окончания затем чрезмерно реагируют на многие другие триггеры, такие как дым, духи или перепады температуры, вызывая непреодолимое желание кашлять. Они называют это состояние «синдромом гиперреактивности нейронов» и описывают несколько подходов к лечению.
Но подождите, это еще не все. Другие исследователи описывают аналогичную концепцию на уровне гортани, семейства расстройств под «синдромом дисфункции гортани», которое может включать «гиперреактивность гортани». Многие из описываемых ими методов лечения похожи на методы лечения «гиперреактивности нейронов», и наиболее многообещающими являются противосудорожные препараты габапентин и прегабалин, антидепрессант амитриптилин, логопедия или их комбинация.
По сути, медицинские эксперты описывают новую причину хронического кашля, основанную на обострении нервов и дисфункции дыхательных путей, и дальнейшие исследования приведут к лучшему лечению.
FDA одобрило новый антибиотик от внебольничной пневмонии
Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA) вчера объявило об одобрении лефамулина, нового антибиотика для лечения внебольничной бактериальной пневмонии (CABP). Было одобрено как пероральное, так и внутривенное (IV) лекарственное средство, разработанное Nabriva Therapeutics из Дублина.
Лефамулин — первый в своем классе полусинтетический антибиотик плевромутилина, разработанный для подавления синтеза бактериального белка, необходимого для роста бактерий. Он показан для лечения CABP, вызванного наиболее распространенными грамположительными и грамотрицательными бактериями, связанными с этим заболеванием, включая Streptococcus pneumoniae , метициллин-чувствительные Staphylococcus aureus , Mycoplasma pneumonia, и Haemophilus influenzae.
Новый инструмент устойчивости к противомикробным препаратам
«Этот новый препарат представляет собой еще один вариант лечения пациентов с внебольничной бактериальной пневмонией, серьезным заболеванием», — сказал Эд Кокс, доктор медицины, магистр здравоохранения, директор Управления противомикробных препаратов FDA в выпуске новостей.«Для борьбы с этим серьезным заболеванием важно, чтобы врачи и пациенты имели варианты лечения. Это одобрение подтверждает нашу неизменную приверженность лечению инфекционных заболеваний путем содействия разработке новых антибиотиков».
CABP — одна из наиболее частых инфекционных причин болезней и госпитализаций, особенно у пожилых людей. По данным Центров по контролю и профилактике заболеваний, около 1 миллиона человек ежегодно обращаются за помощью в больницу по поводу CABP, и 50 000 человек умирают от этого заболевания.CABP обычно лечат антибиотиками из группы макролидов и фторхинолонов.
Официальные лица Набривы говорят, что новый метод действия лефамулина приводит к низкой склонности к развитию резистентности. Они также считают, что пероральные и внутривенные формы препарата, которые будут продаваться под торговой маркой Xenleta, могут сделать его препаратом первой линии для лечения CABP.
«Сегодняшнее одобрение Xenleta является значительным прорывом в коллективной борьбе с растущей угрозой устойчивости к противомикробным препаратам и обеспечивает крайне необходимый вариант эмпирической монотерапии внутривенно и перорально для взрослых с CABP», — заявил генеральный директор Nabriva Тед Шредер в пресс-релизе компании .
Безопасность и эффективность, продемонстрированные в клинических исследованиях
Одобрение было подтверждено двумя клиническими испытаниями фазы 3, известными как LEAP 1 и LEAP 2, в которых оценивалась безопасность и эффективность внутривенного и перорального лефамулина у 1289 пациентов с CABP по сравнению с моксифлоксацином. обычное лечение первой линии. В LEAP 1, 5-7 дней внутривенного / перорального приема лефамулина продемонстрировали не меньшую эффективность по сравнению с 7-дневным внутривенным / пероральным приемом моксифлоксацина с линезолидом или без него. В исследовании LEAP 2 5-дневный пероральный прием лефамулина продемонстрировал не меньшую эффективность, чем 7-дневный пероральный прием моксифлоксацина.В обоих исследованиях препарат в целом хорошо переносился.
Наиболее частыми побочными реакциями, о которых сообщалось в исследованиях, были диарея, тошнота, рвота, реакции в месте инъекции и повышение уровня печеночных ферментов. FDA заявило, что следует избегать приема препарата пациентам с нерегулярным сердечным ритмом, пациентам с известной гиперчувствительностью к лефамулину или другим антибиотикам плевромутилина, а также беременным женщинам.
Доступно в США через 1 месяц
Лефамулин получил от FDA статус квалифицированного препарата для лечения инфекционных заболеваний (QIDP), который присваивается антибактериальным и противогрибковым препаратам, которые лечат серьезные или опасные для жизни инфекции.Целью обозначения QIDP, созданного Конгрессом в 2012 году в соответствии с Законом о создании стимулов для использования антибиотиков (GAIN), является стимулирование разработки новых антибиотиков для лечения трудноизлечимых инфекций путем предоставления производителям лекарств дополнительных 5 лет на маркетинг. эксклюзивность.
Препарат также получил статус приоритетного обзора FDA, который присваивается лекарствам, которые могут иметь преимущества в клиническом лечении.
Набрива ожидает, что лефамулин будет доступен в США к середине сентября.Оптовый препарат для внутривенного введения будет стоить 205 долларов в день, а пероральное лечение будет стоить 275 долларов в день.
См. Также:
19 августа Пресс-релиз FDA
19 августа Пресс-релиз Набривы
Расскажите мне о пневмонии у детей
Вопрос
У моей двухлетней дочери была высокая температура и рвота, как правило, примерно раз в неделю в течение последних трех месяцев. Это всегда происходит ночью.
Изначально у нее была диагностирована вирусная инфекция, но после нескольких инцидентов, описанных выше, ее отправили на рентген и анализ крови.
Врач сказал, что оба вышеперечисленных теста показали, что у моей дочери легкая форма пневмонии у основания легкого, и что антибиотики должны ее устранить.
Будучи очень встревоженным и шокированным, я не стал задавать ему никаких вопросов.
Не могли бы вы предоставить дополнительную информацию об этом состоянии, а также рассказать мне, что может произойти дальше, если инфекция не исчезнет.
Ответ
Инфекция грудной клетки или пневмония могут возникнуть у ранее здорового ребенка просто в результате «невезения».
Если определенные вирусы и бактерии вдыхаются и им удается пройти вниз по основным трубкам в легких и откладываться в ткани легких, они могут размножиться и вызвать серьезную инфекцию, которая может вызвать следующие симптомы:
- кашель
- Мутная мокрота
- затрудненное дыхание
- высокотемпературный
- рвота
- потеря аппетита
- общее недомогание.
Антибиотики часто быстро избавляют от такой инфекции, и ребенок может быстро поправиться и больше не будет.
Лечащий врач вашей дочери, несомненно, скоро осмотрит ее, чтобы убедиться, что антибиотики излечивают ее инфекцию.
Помимо прослушивания ее груди с помощью стетоскопа, чтобы увидеть, чисты ли легкие, можно сделать еще один рентген грудной клетки, чтобы убедиться, что больше нет видимых признаков инфекции.
Если инфекция не исчезла с помощью первого курса антибиотиков, это может просто означать, что ответственное насекомое устойчиво к этому лечению, и, вероятно, будет назначен другой антибиотик.
Если инфекция грудной клетки вашей дочери все еще не улучшилась или если в течение следующих нескольких месяцев у нее развились другие инфекции грудной клетки, ваш врач может направить ее к специалисту больницы для дальнейших анализов.
Они будут разработаны для поиска основной проблемы с грудной клеткой (например, кистозного фиброза), которая может сделать ребенка более склонным к развитию инфекций грудной клетки, или более общей проблемы с ее иммунной системой, которая может сделать ее более уязвимой для инфекций.
На данный момент меня бы не слишком пугали, особенно если это первая инфекция грудной клетки, перенесенная вашей дочерью.
Один из моих сыновей внезапно заболел пневмонией, когда ему было два года, быстро отреагировал на антибиотики, и с тех пор у него не было серьезных проблем с легкими.
Так что на данном этапе я с оптимизмом смотрю, что ваша дочь последует ее примеру, но, естественно, вам нужно будет следить за тем, чтобы за ней наблюдала терапевт, пока инфекция не будет ликвидирована.
С уважением
Медицинская бригада NetDoctor
Последнее обновление
Этот контент создается и поддерживается третьей стороной и импортируется на эту страницу, чтобы помочь пользователям указать свои адреса электронной почты. Вы можете найти дополнительную информацию об этом и подобном контенте на сайте piano.io.
Обзоры и рейтинги кларитромицина на Drugs.com
- Лекарства от А до Я
- Кларитромицин
- Отзывы пользователей
Также известен как: Биаксин XL
Кларитромицин имеет средний рейтинг 5.4 из 10 из 715 оценок на Drugs.com. 36% пользователей, которые рассматривали Кларитромицин, сообщили о положительном эффекте, а 35% сообщили о отрицательном эффекте.
Фильтр по условию Все условия Профилактика бактериального эндокардита (2) Бронхит (130) Абсцесс зубов (11) Фолликулярная лимфома (1) Инфекция Helicobacter Pylori (76) Легионеллезная пневмония (1) Mycobacterium avium-intracellulare, Профилактика Mycobacterium avium-intracellularecoplasma (1) Mycobacterium avium-intracellularecoplasma, Лечение (1) ) Негонококковый уретрит Средний отит (34) Коклюш (4) Профилактика коклюша (1) Фарингит (5) Пневмония (52) Синусит (175) Инфекция кожи и структур (11) Инфекция кожи или мягких тканей (47) Стрептококковая инфекция (58) Тонзиллит / Фарингит (41) Токсоплазмоз Инфекция верхних дыхательных путей (60)
Обзоры могут быть модерированы или отредактированы перед публикацией для исправления грамматики и орфографии или для удаления ненормативной лексики и содержания.Обзоры, которые, как представляется, созданы сторонами, заинтересованными в лекарстве, не будут публиковаться. Поскольку обзоры и рейтинги являются субъективными и самопровозглашенными, эту информацию не следует использовать в качестве основы для любого статистического анализа или научных исследований.
Отзывы для Кларитромицин
Сортировать по Самые последниеСамые полезныеНаивысший рейтингНизкий рейтингВремя приема лекарств
Часто задаваемые вопросы
Больше FAQ
Эта информация НЕ предназначена для поддержки какого-либо конкретного лекарства.Хотя эти обзоры могут быть полезны, они не заменяют опыт, знания и суждения практикующих врачей.
Подробнее о кларитромицине
Потребительские ресурсы
Другие бренды: Biaxin, Biaxin XL

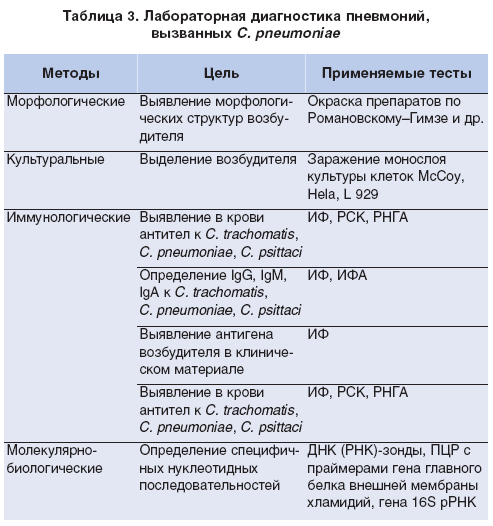


 — М., 2000. — 48 с.
— М., 2000. — 48 с. — Казань, 2001. — 64 с.
— Казань, 2001. — 64 с.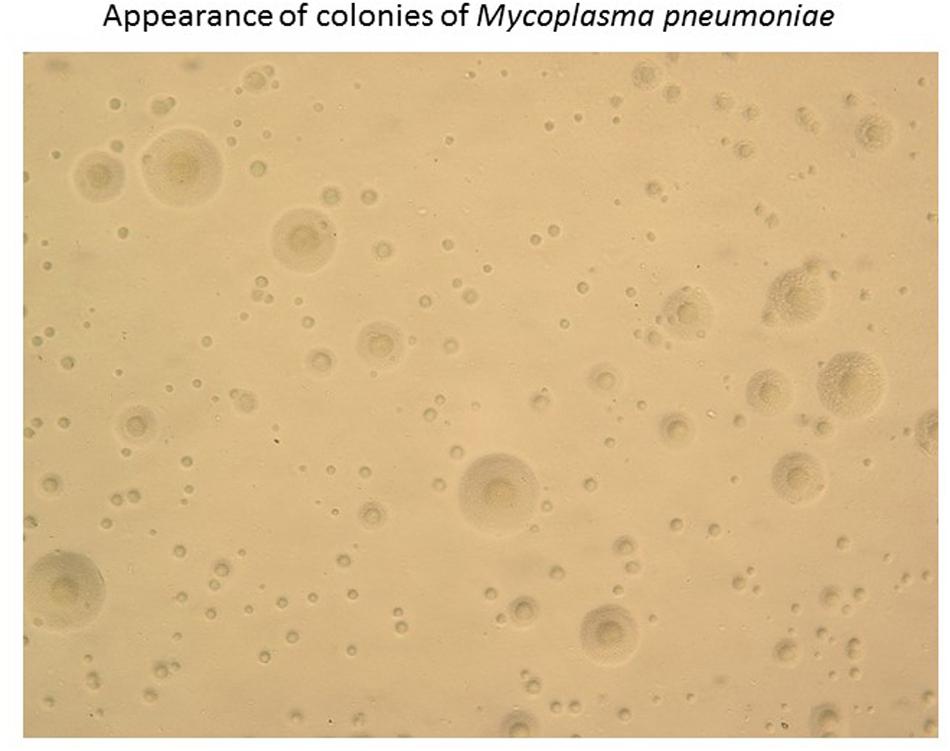


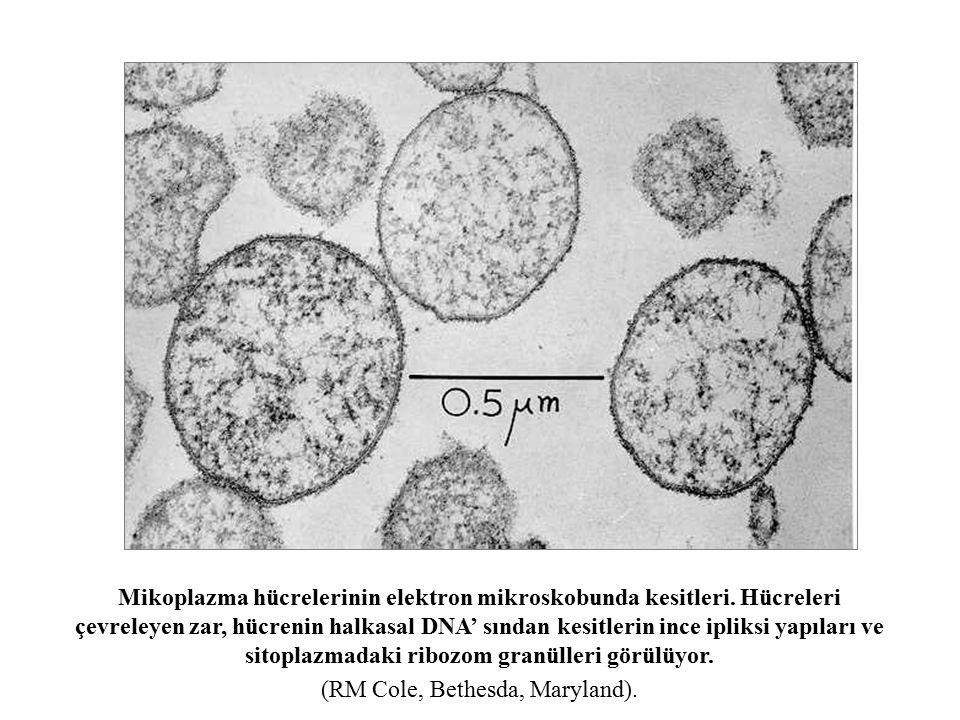 Возбудитель присутствует в организме непродолжительное время.
Возбудитель присутствует в организме непродолжительное время.