Выкидыш на ранних сроках: новые данные о целесообразности назначения прогестерона
Согласно результатам нового исследования, назначение прогестерона женщинам с кровотечением на ранних сроках беременности не предотвращает потерю беременности, за исключением случаев, когда у женщины уже есть история выкидышей. В исследовании приняли участие 4153 женщины, проходившие лечение в 48 больницах Великобритании.
«Это хорошая новость для пациентов. Данное открытие предотвратит ошибочное лечение прогестероном большинства женщин и даст дополнительную надежду пациенткам, которые сталкиваются со вторым, третьим или четвертым выкидышем», – отметил ведущий автор исследования доктор Арри Кумарасами (Arri Coomarasamy), профессор гинекологии в Университете Бирмингема (University of Birmingham), Великобритания.
Кровотечение, которое может указывать на проблемы в первые месяцы беременности, возникает примерно у 25% беременных. Из них в 10–20% случаев кровотечение может стать предвестником прерывания беременности.
На протяжении многих лет препараты прогестерона использовались для устранения угрозы выкидыша не по прямому назначению. Частично такие назначения были оправданы снижением уровня гормонов непосредственно перед выкидышем.
Новое исследование, опубликованное 8 мая 2019 г. в издании «New England Journal of Medicine», сообщает о том, когда прием гормонов эффективен, а когда нет.
«Вполне вероятно, что первоначальное обоснование гормональной терапии – то есть снижение уровня гормонов беременности до выкидыша – на самом деле было скорее следствием, чем причиной потери беременности», – подчеркнул доктор Майкл Грин (Michael Green).
В исследовании принимали участие 2238 беременных, у которых не было опыта потери беременности. Пациентки с кровотечением на раннем сроке принимали либо микронизированный прогестерон в дозе 400 мг 2 раза в сутки, либо плацебо. В результате у пациенток с риском выкидыша, которые принимали прогестерон, частота успешных родов после 34-й недели составила 75%, у тех, кто принимал плацебо, – 72%.
Однако в исследовании также участвовали женщины с историей выкидышей на ранних сроках. Те участницы, которые принимали прогестерон и в анамнезе у них отмечали от 1 до 2 случаев выкидышей, успешно рожали в 75% случаев. Те, кто принимал плацебо, – в 70% случаев.
В свою очередь, у участниц с 3 выкидышами и более отмечали успешную беременность в 72% случаев. У тех, кто принимал плацебо, – в 57% случаев.
Ученые считают, что разница в показателях между приемом прогестерона и плацебо подтверждает эффективность применения прогестерона у женщин с угрозой выкидыша на ранних сроках, которые уже имеют опыт потери беременности.
Ожидается, что полученные результаты повысят уровень применения препаратов прогестерона в Великобритании, где опрос 2012 г. показал, что данные лекарственные средства назначается только в 4,5% случаев кровотечений на ранних сроках беременности.
Наряду с этим ожидается снижение использования препаратов прогестерона в некоторых странах, где в случае возникновения кровотечения на ранних сроках беременности до 90% женщин получают данные лекарственные средства.
По материалам www.medscape.com
Цікава інформація для Вас:
Прогестоген для предотвращения выкидыша | Cochrane
В чем суть проблемы?
Прерывание беременности на ранних сроках, также известное как выкидыш, чаще всего случается в первом триместре. У некоторых женщин и их партнеров выкидыши могут случаться неоднократно, что также известно как привычное невынашивание. Хотя в некоторых случаях причину выкидышей можно определить, зачастую установить ее не удается. Гормон, называемый прогестероном, готовит матку к имплантации и укреплению недавно оплодотворенной яйцеклетки на начальном этапе беременности. Было высказано предположение о том, что у некоторых женщин, у которых случаются выкидыши, может вырабатываться недостаточно прогестерона на начальном этапе беременности.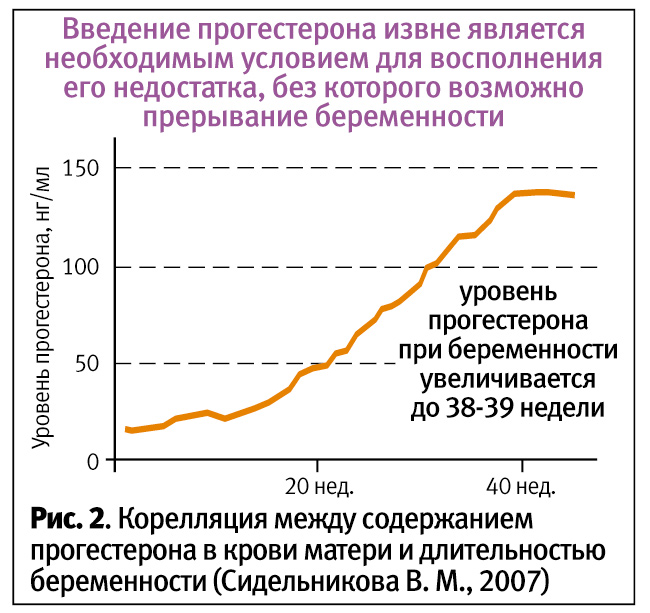
Почему это важно?
Выкидыши могут быть как физическим, так и эмоциональным потрясением для женщин и их партнеров. Поиск лечения для предотвращения повторных выкидышей мог бы помочь им избежать выкидышей и иметь ребенка.
Какие доказательства мы обнаружили?
6 июля 2017 года мы провели поиск доказательств и нашли 13 клинических испытаний с участием 2 556 женщин с повторными выкидышами в анамнезе. Эти испытания показали, что на ранних сроках беременности прием прогестогена женщинами с повторными выкидышами в анамнезе может сократить частоту выкидышей при текущей беременности с 26,3 до 19,4 %. Мы считаем, что эти результаты основаны на доказательствах лишь умеренного качества, а потому не можем быть уверены в них. Мы обнаружили, что лечение прогестогеном может быть наиболее полезным для женщин с не менее чем тремя выкидышами к началу исследования.
Что это значит?
В рандомизированных контролируемых испытаниях мы нашли доказательства того, что прогестогены, вероятно, могут предотвращать выкидыши у женщин с привычным невынашиванием.
Самопроизвольный выкидыш | «СМ-Клиника»
Самопроизвольный выкидыш — самостоятельное прерывание беременности до достижения плодом сроков жизнеспособности.
Причины самопроизвольного выкидыша
- Гормональные нарушения. Наиболее частой гормональной причиной, провоцирующей сампроизвольный выкидыш, является недостаток прогестерона — гормона , синтезируемого желтым телом яичника в ранние сроки беременности. В более поздние сроки (после 12 недель беременности) прогестерон вырабатывается плацентой. Основная цель прогестерона при беременности — снижение тонуса миометрия и предотвращение отторжения плодного яйца. При дефиците прогестерона мышцы матки становятся легко возбудимы, возникает гипертонус миометрия — угроза прерывания беременности. Причины снижения уровня прогестерона многообразны — нарушение процесса овуляции, дефект формирования желтого тела, нарушение формирования плаценты, нарушения кровообращения в малом тазу и т.

- Вторым по частоте гормональным фактором, провоцирующим самопроизвольный выкидыш, является гиперандрогения — повышенный уровень мужских половых гормонов. Избыточный уровень андрогенов при беременности подавляет синтез прогестерона и эстрогенов, повышая тем самым риск прерывания беременности.
- Нарушение баланса гормонов щитовидной железы — гипотиреоз, либо тиреотоксикоз также могут существенно повышать вероятность неблагоприятного исхода беременности.
- Генетические аномалии являются частыми причинами ранних самопроизвольных выкидышей. В таких случаях у формирующегося эмбриона регистрируется неправильный набор хромосом. Аномальный хромосомный набор может стать как следствием генетических нарушений одного из родителей, так и результатом единичной случайной мутации, произошедшей под влиянием вредных факторов среды Большинство хромосомных нарушений приводит к тяжелым порокам развития внутренних органов плода и являются несовместимыми с жизнедеятельностью, и в таких случаях в силу вступает естественный отбор, всеми силами способствуя прерыванию подобной беременности.

- Инфекционные причины. Наибольшую опасность для беременности представляют вирусные инфекции, особенно если беременная женщина во время беременности перенесла из впервые в жизни. К таким инфекциям относится вирус простого герпеса 1 и 2 типов, краснуха, цитомегаловирус, токсоплазмоз. Значительно повышают риск прерывания беременности и инфекции, передающиеся половым путем — хламидиоз, микоплазмоз, некоторые виды уреаплазменной инфекции и т. д. Осложненное течение респираторных вирусных инфекций, особенно вируса гриппа, также могут привести к неблагоприятному завершению беременности.

- Анатомические факторы. Нарушение анатомии матки приводят к деформации полости матки, тем самым нарушая процесс имплантации плодного яйца; а в случае наступления беременности механически воздействуют на плодное яйцо, нарушая его развитие. К таким анатомическим факторам относятся врожденные аномалии развития матки — седловидная матка с деформацией полости, перегородки в матке, двурогая матка. Наиболее частым приобретенным анатомическим фактором, способствующим самопроизвольному выкидышу, является миома матки. Наибольшей опасности подвергаются женщины с миоматозными узлами больших размеров (более 5 см), множественными и аномально расположенными узлами (шеечная, перешеечная локализация), а также с миоматозными узлами, деформирующими полость матки.
- Анатомическим фактором, повышающим вероятность самопроизвольного выкидыша в поздние сроки является патология шейки матки — цстмико — цервикальная недостаточность, процесс, когда укорочение и открытие шейки матки происходит раньше срока предполагаемых родов.

- Аутоимунные, гемостазиологические нарушения. Наличие аутоиммунных заболеваний (процессов, когда собственная иммунная система выделяет антитела против своих органов и тканей) достоверно повышает риск неблагоприятных исходов беременности на ранних и поздних сроках.
Что делать, если беременность завершилась самопроизвольным выкидышем? В первую очередь, важен позитивный настрой на последующую беременность. Достижения современной медицины позволяют справится со всеми причинами и последствиями выкидыша, и, после определенной подготовки, выносить и родить здорового малыша.
- Сразу после случившегося самопроизвольного выкидыша необходимо пройти курс антибактериальной терапии, который всегда назначается в таких случаях гинекологом. Цель приема данных препаратов — профилактика инфекционных осложнений в органах малого таза после перенесенного вмешательства.
- Контрацепция.
 После перенесенного выкидыша не рекомендуется планировать следующую беременность минимум 3 месяца, оптимальный же срок контрацепции — полгода. При отсутствии противопоказаний лучшим способом контрацепции являются гормональные препараты — помимо высочайшей контрацептивной эффективности они позволяют восстановить нарушенный гормональный фон после прервавшейся беременности.
После перенесенного выкидыша не рекомендуется планировать следующую беременность минимум 3 месяца, оптимальный же срок контрацепции — полгода. При отсутствии противопоказаний лучшим способом контрацепции являются гормональные препараты — помимо высочайшей контрацептивной эффективности они позволяют восстановить нарушенный гормональный фон после прервавшейся беременности. - Комплексное обследование. Перед планированием следующей беременности необходимо установить причину самопроизвольного выкидыша, и устранить ее. Для этого необходимо пройти комплексное обследование, составить план которого индивидуально в зависимости от ситуации вам поможет опытный и квалифицированный врач — гинеколог. В план данного обследования всегда входит полный инфекционный скрининг, исследование гормонального фона, выявление аутоимунных и гемостазиологических нарушений. У супружеских пар старше 35 лет проводится генетическое исследование — определение кариотипа с консультацией генетика. Остальные пункты дообследования составляются гинекологом индивидуально в зависимости от особенностей каждого конкретного случая.

Прерывание беременности: что мы можем сделать для профилактики? | Ди Ренцо Дж.К., Доброхотова Ю.Э., Маркова Э.А.
ВведениеВ настоящее время известно множество предпосылок к угрозе выкидыша, к выкидышу, к привычному прерыванию беременности и к преждевременным родам. Потеря или досрочное прерывание беременности может быть обусловлено целым рядом причин, это: генетические поломки кариотипа родителей, эмбриона, эндокринные нарушения, пороки развития матки, истмико-цервикальная недостаточность, инфекционные факторы с персистенцией условно-патогенных микроорганизмов и/или вирусов, аутоиммунные нарушения, наследственные тромбофилии и др.
Сегодня имеется возможность пролонгировать беременность до доношенного срока. Мы способны дать плоду множество шансов для выживания, особенно после 22 нед., когда плод уже может адаптироваться и выжить, у нас для этого есть потенциал и все ресурсы. Поэтому, касаясь темы угрожающего и привычного выкидыша, обсудим многие моменты: возможности терапии угрозы прерывания беременности, профилактику привычного выкидыша, терапию преждевременных родов.
В настоящее время в медицинской литературе представлено большое количество данных по рассматриваемой теме, но всякий раз, обращаясь к результатам исследований, мы задаемся вопросом о степени их достоверности. Возможно, они содержат ложную информацию. Причем не имеет значения, где эти данные опубликованы, в научных журналах или на веб-сайтах. А вероятность, что нас привлекут именно альтернативные факты и недостоверные данные, довольно высока, и это может изменить наше мнение и сформировать неверную точку зрения на существующие вопросы. Некоторые исследователи публикуют единичные данные, методологически слабые исследования, результаты которых, скорее всего, будут недостоверными по причине некорректного протокола. Такие данные не подвергаются грамотной статистической обработке, что не позволяет руководствоваться ими в практической деятельности.
Таким образом, необходимость клинических исследований не подвергается сомнению, но они должны быть качественными, иначе можно прийти к неверным клиническим выводам. Ключевым вопросом является достоверность публикуемых данных.
Ключевым вопросом является достоверность публикуемых данных.
Сегодня доказательная медицина — это система сбора, обобщения и анализа всех имеющихся знаний (гипотез, результатов исследований) о профилактике, диагностике и лечении заболеваний. Это наиболее полная и объективная картина современной медицины. Доказательная медицина — это концепция принятия врачебных и управленческих решений с учетом результатов качественных клинических исследований, клинического опыта и интересов пациента [1]. Символическая пирамида доказательной медицины — это иерархия доказательств (рис. 1) [2].
Структура пирамиды представлена несколькими ступенями. В самом низу находятся экспертные мнения и идеи одного человека. Сегодня, в эпоху доказательной медицины, одно мнение ничего не значит. На следующих ступенях располагаются отдельные клинические случаи и серии клинических случев, далее — когортные исследования и рандомизированные контролируемые исследования. Вершину пирамиды венчают двойные слепые рандомизированные плацебо-контролируемые исследования и систематические обзоры и метаанализы, которые публикуются на основании предыдущих исследований. Качество доказательств растет с увеличением ступеней пирамиды.
Вершину пирамиды венчают двойные слепые рандомизированные плацебо-контролируемые исследования и систематические обзоры и метаанализы, которые публикуются на основании предыдущих исследований. Качество доказательств растет с увеличением ступеней пирамиды.
Согласно данным, полученным в исследованиях, формируются уровни доказательности. Таким образом, чем выше уровень исследований, тем достовернее их результаты. Однако выводы, вытекающие из метаанализов, зависят от качества анализируемых исследований. Положительным примером может служить публикация R. Romero et al. [3], представляющая собой метаанализ клинических наблюдений по использованию вагинальной формы прогестерона для профилактики преждевременных родов и неблагоприятных перинатальных исходов при одноплодной беременности и короткой шейке матки. Данная работа является обзором пяти больших исследований, включивших 1016 пациенток. Авторы провели скрининг тысяч публикаций по нескольким критериям и только пять публикаций соответствовали необходимым критериям качества. Их результаты и были затем проанализированы. Другая ситуация с метаанализами по вопросам угрожащего выкидыша. Например, в одном из недавних метаанализов основной ряд исследований был довольно беден по своей методологии, исследования не были слепыми для участников, был неясен метод рандомизации. Слабый дизайн исследования, в свою очередь, лишает его надежных выводов. Очевидно, что данные этих исследований недостаточно корректны и высока вероятность их неправильной оценки (рис. 2) [4].
Их результаты и были затем проанализированы. Другая ситуация с метаанализами по вопросам угрожащего выкидыша. Например, в одном из недавних метаанализов основной ряд исследований был довольно беден по своей методологии, исследования не были слепыми для участников, был неясен метод рандомизации. Слабый дизайн исследования, в свою очередь, лишает его надежных выводов. Очевидно, что данные этих исследований недостаточно корректны и высока вероятность их неправильной оценки (рис. 2) [4].
Таким образом, глядя на рисунок 2, можно сказать, что сравнивать данные в этих исследованиях, это как сравнивать яблоки с грушами: и те и другие — фрукты, но фрукты совершенно разные.
Например, в одном исследовании, Gerhard (1987), женщинам в основной группе назначался прогестерон в дозе 25 мг дважды в день, пациенткам контрольной группы предписывался постельный режим. В другом исследовании, Palagiano (2004), применялся прогестерон (Крайнон 8%) в дозировке 90 мг один раз в день, в контрольной группе пациентки получали плацебо. При этом длительность первого исследования составляла несколько недель, а второго — 5 дней. Сравнивать эти исследования и делать по ним какие-либо выводы невозможно, так как априори они будут ошибочными. Мы сравниваем яблоки и груши. Это не наука, это лженаука [5].
При этом длительность первого исследования составляла несколько недель, а второго — 5 дней. Сравнивать эти исследования и делать по ним какие-либо выводы невозможно, так как априори они будут ошибочными. Мы сравниваем яблоки и груши. Это не наука, это лженаука [5].
В процессе нашей работы было оценено еще одно исследование 2019 г. Это большой метаанализ исследований эффективности прогестерона у женщин с привычным невынашиванием беременности (ПНБ) неясной этиологии, применяемого для профилактики репродуктивных потерь. В данную работу вошли 10 исследований (1684 пациентки), которые получали препараты прогестерона перорально или вагинально. Группы в исследованиях были сопоставимы по данным анамнеза и путям введения препарата. Исследование можно охарактеризовать как более качественное, и по нему могут быть сформулированы правильные выводы [6]. Данный метаанализ показал, что эффективность препарата не зависит от пути введения.
Профилактика привычного выкидыша
Cамопроизвольный выкидыш — это прерывание беременности в сроке до 22 нед.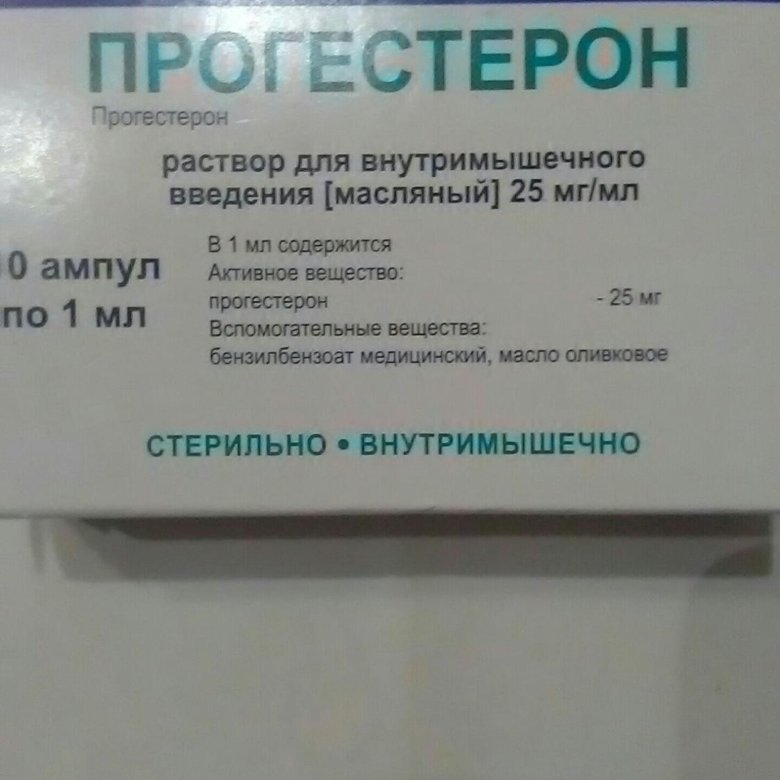 [7]. Доказано, что одна из пяти женщин, которые столкнулись с проблемой самопроизвольного выкидыша, имеет высокий уровень тревожности, подобный тому, который можно наблюдать у пациенток с психиатрической патологией. К сожалению, одна из четырех беременностей заканчивается самопроизвольным прерыванием. К несчастью, одна из трех женщин, у которых случались репродуктивные потери, имеет клиническую депрессию.
[7]. Доказано, что одна из пяти женщин, которые столкнулись с проблемой самопроизвольного выкидыша, имеет высокий уровень тревожности, подобный тому, который можно наблюдать у пациенток с психиатрической патологией. К сожалению, одна из четырех беременностей заканчивается самопроизвольным прерыванием. К несчастью, одна из трех женщин, у которых случались репродуктивные потери, имеет клиническую депрессию.
Риск выкидыша у женщин с неблагоприятным акушерско-гинекологическим репродуктивным анамнезом был оценен в метаанализе, проведенном по ряду исследований [8–10]. Оценивали количество выкидышей в анамнезе и частоту выкидышей, которая нарастает с увеличением числа репродуктивных потерь от 11,3% при отсутствии выкидышей в анамнезе до 63,9% при наличии неблагоприятного анамнеза по потерям беременности. В отдельно взятых исследованиях цифры были схожи.
Еще одно исследование касалось генетического фактора невынашивания: оценивали кариотип эмбриона (хромосомные аномалии) по отношению к числу предыдущих выкидышей в структуре репродуктивных потерь [11]. На рисунке 3 показано соотношение благоприятно завершенных беременностей, эуплоидных выкидышей и анеуплоидных выкидышей и количества предыдущих выкидышей в анамнезе. Мы видим, что генетический фактор является основной причиной потерь при первых беременностях, но при возрастании количества потерь беременностей в анамнезе все большее количество выкидышей обусловлены другими, негенетическими причинами. Основным фактором невынашивания в этих случаях можно назвать плацентарный сосудистый фактор.
Хорошо известно, что прогестерон играет важную роль во время беременности. Он необходим для ее благоприятного течения, стимулирует рост матки и дифференцировку эндометрия, ингибирует маточные сокращения. Низкие уровни прогестерона ассоциированы с угрозой прерывания беременности и спонтанным выкидышем [12]. Сывороточные уровни прогестерона растут с увеличением срока беременности.
Как же работает прогестерон? Мы изучаем этот вопрос почти 20 лет. Биоидентичный прогестерон обладает уникальными фармакодинамическими свойствами, обеспечивающими поддержание беременности [13–21]. Его уникальным свойством является модулирование материнского иммунного ответа. Кроме того, он улучшает маточно-плацентарный кровоток, снижает тонус матки, являясь антагонистом окситоцина, ингибирует синтез простагландинов, способствует секреторной трансформации и децидуализации эндометрия, вызывая вазодилатацию и развитие экстравазатов трофобласта при его инвазии в материнскую оболочку, ремоделируя локальную сосудистую сеть.
Изучению роли прогестерона был посвящен ряд исследований [22, 23]. Одно из когортных исследований касалось определения прогестерона в крови для оценки исхода беременности у женщин с болями и кровяными выделениями. Другая работа была посвящена вопросу: действительно ли профилактическое назначение прогестерона в I триместре беременности повышает благоприятный исход у женщин с неясным генезом ПНБ? Метаанализ клинических испытаний прогестерона/прогестагенов у пациенток с ПНБ показал неоспоримую пользу прогестерона, которая была доказана.
Однако у ранее полученных данных были недостатки: качество ряда исследований было плохим, количество пациенток, принимавших участие в исследовании, — небольшим. Кроме того, применялись широкие доверительные интервалы, отсутствовал стандартизированный протокол, допускались погрешности в стратификации по возрасту и репродуктивному анамнезу женщин, использовались различные несопоставимые схемы приема препаратов прогестерона/прогестагенов. Проводя анализ, всегда помним про яблоки и груши! Таким образом, про эти исследования можно забыть.
В последние годы очень интересное и большое исследование было выполнено группой английских ученых в г. Бирмингеме. В протокол исследования PROMISE были включены женщины с ПНБ неясного генеза (основная группа, n=790), которые пытались забеременеть естественным путем. Им был назначен прогестерон в дозе 400 мг вагинально дважды в день в период с 4-й по 12-ю неделю. Женщины в группе сравнения получали плацебо. В результате исследования были получены данные по живорождению в сроках более 24 нед. С учетом того, что количество предыдущих выкидышей в основной группе варьировало от трех до шести, статистические расчеты показали, что у пациенток, принимавших прогестерон, доля живорождений после 24 нед. начиналась от 67,9% при наличии трех выкидышей в анамнезе и от 57,4% при шести выкидышах. Тенденция к увеличению положительных исходов в группе прогестерона возрастала с увеличением числа выкидышей в анамнезе. То есть чем больше количество выкидышей в анамнезе, тем более оправдано и назначение прогестерона, так как его применение повышает шанс благоприятного исхода беременности на 7,4% [23, 24].
В пользу микронизированного прогестерона говорит еще один систематический обзор и метаанализ, включающий 82 статьи (26 726 пациенток) [25]. Установлено, что на благоприятный исход беременности повлияло назначение прогестерона с первого дня после получения ооцитов в программах ВРТ. Этим обоснована оптимальность назначения прогестерона на прегравидарном этапе, что является клиническим выводом в данной работе.
Итак, когда же начинать терапию при привычном невынашивании? Гипотеза состоит в том, что прием препаратов прогестерона у женщин с ПНБ оптимально начинать с лютеиновой фазы на прегравидарном этапе, когда есть возможность повлиять на процессы имплантации. Это было с блеском подтверждено в двух рандомизированных исследованиях, опубликованных в декабре 2016 г. и в апреле 2017 г. [26, 27]. Результаты отмеченных исследований были включены в последние клинические рекомендации ESHRE (European Society of Human Reproduction and Embryology) за 2017 г. [28].
Возникает вопрос: почему так важен прогестерон? В исследовании [29] проводилась гистологическая оценка состояния эндометрия. Пациенткам выполняли биопсию эндометрия на 9–11-й день цикла после пика уровня лютеинизирующего гормона. Окраску проводили гематоксилином и эозином. У ряда пациенток выявлялись аномальные изменения эндометрия. Им назначали терапию вагинальной формой микронизированного прогестерона в дозе 200–400 мг/сут во вторую фазу менструального цикла. Повторная гистологическая оценка состояния эндометрия проводилась через месяц. На фоне терапии наблюдалась нормализация циклической трансформации эндометрия и его гистологической структуры.
Следующее исследование также подтверждает, что начало терапии прогестероном в лютеиновую фазу у женщин с ПНБ необходимо для благоприятного исхода последующей беременности [26]. Так, в подгруппах женщин, получавших вагинальную форму микронизированного прогестерона, благоприятных исходов беременности было достоверно больше: 86 из 126 против 19 из 37 в группе плацебо.
Таким образом, прогестерон важен именно во время имплантации эмбриона, он оказывает благоприятный эффект и положительное действие препарата может быть наиболее полно реализовано при его назначении именно в лютеиновую фазу еще до получения положительного теста на беременность.
Протокол и клинические рекомендации по терапии угрозы прерывания беременностиК врачам-клиницистам часто обращаются пациентки с жалобами на тянущие боли в низу живота и кровяные выделения из половых путей. Как мы можем им помочь? Был проведен метаанализ семи исследований, включивших в целом 744 женщины. Эти исследования были небольшими и не имели хорошего дизайна, но в целом показали благоприяное действие прогестинов в сравнении с плацебо.
В еще один метаанализ, проведенный совсем недавно, включены работы последних десятилетий [30]. Оценка в целом показала, что клинические эффекты прогестерона статистически значимы. В данном случае исследования были длительными и (помним о пирамиде доказательной медицины!) могут расцениваться как достоверные.
Вопрос лекарственной безопасности: какая разница между прогестероном и прогестагенами? Что касается прогестерона, то существует большое количество качественных исследований, проведенных с микронизированным прогестероном, в отношении прогестагенов информации намного меньше. Вагинальный прогестерон, который применяли пациентки, показал свою высокую эффективность и лекарственную безопасность. Сравнивая данные малых исследований с небольшой выборкой и данные крупных исследований, таких как PRISM, видим, что ни в одном из них не было указаний на отрицательные и побочные эффекты прогестерона, превосходящие такие показатели в группе плацебо. В отношении развития врожденных патологий и прерывания беременности на фоне приема препаратов прогестерона можно отметить, что неблагоприятные исходы для плода никак не зависели от того, на каком сроке пациентка начинала терапию и до какого срока она ее применяла — до 16 нед. или до 22 нед. В исследованиях безопасности прогестерона принимали участие более 5000 женщин, и не было выявлено отрицательного влияния препарата на плод на сроках от 4–6 нед. до 36 нед. по сравнению с плацебо [31].
Данные по дидрогестерону: в статье «Взаимосвязь между пероральным применением дидрогестерона во время беременности на ранних сроках и развитием врожденных пороков сердца», опубликованной в журналах Pediatric Cardiology в 2015 г. и Lancet в 2017 г., было показано, что у женщин, применявших дидрогестерон во время беременности, достоверно чаще, чем у женщин, не применявших этот препарат, рождались дети с пороками сердца (скорректированное отношение шансов 2,71; 95% ДИ 1,54–4,24; p<0,001) [31, 32]. Еще одно исследование [33] подтвердило этот вывод и показало, что при приеме во время беременности дидрогестерона достоверно чаще регистрировались не только пороки сердца (врожденная аортальная недостаточность и мальформации сердца), но и гипоспадия, расщелина позвоночника (spina bifida) и гидроцефалия (p<0,05). Авторы исследования сделали вывод, что на основании имеющихся совокупных данных можно утверждать, что применение дидрогестерона в период беременности ассоциируется с достоверно более высоким риском развития специфических врожденных мальформаций у плода, включающих прежде всего тяжелые дефекты развития сердечно-сосудистой системы. Несмотря на то что в двух ранее проведенных рандомизированных контролируемых исследованиях указано на отсутствие различий в частоте развития врожденных аномалий в случае приема дидрогестерона по сравнению с натуральным прогестероном, экспертная группа GDG считает эти данные недостаточными для однозначного утверждения и указывает на отсутствие долгосрочных исследований влияния дидрогестерона на здоровье потомства [34].
Возвращаясь к клинической практике, обратимся к клиническому протоколу [35] по ведению пациенток с клиническими проявлениями спонтанного выкидыша. На рисунке 4 представлен клинический алгоритм врачебной тактики при угрозе выкидыша. Алгоритм разработан Национальным институтом здоровья и клинического совершенствования (National Institute for Health and Care Excellence, NICE) Великобритании на основании проведенных исследований и рекомендован к применению в ежедневной практике акушеров-гинекологов в амбулаторных и стационарных условиях.
Роль прогестерона в физиологии беременной женщины — ключевая с момента зачатия и до родов.
Выраженное биологическое действие экзогенного прогестерона поддерживает организм женщины, обеспечивая профилактику повторного выкидыша.
Вопросы оптимальной дозы, путей введения и продолжительности приема остаются предметом обсуждения.
Вагинальные капсулы микронизированного прогестерона теперь имеют уровень доказательности 1 ввиду отсутствия побочных эффектов на плод и его здоровье, наличия экономической эффективности и положительных стоимостных характеристик.
Профилактика преждевременных родов. Стратегии веденияМы можем делать многое для профилактики преждевременных родов (ПР). В разных странах тактика ведения и стратегии различаются, потому что причин ПР много и в разных регионах преобладают свои этиологические факторы, которые будут доминировать и вызывать осложнения, ассоциированные с беременностью. Стратегии профилактики ПР складываются в зависимости от факторов риска: анамнеза ПР, многоплодной беременности, укорочения шейки матки по данным ультразвукового исследования. Возникают вопросы: какие у нас есть инструменты для профилактики ПР, какая тактика? В настоящее время мы назначаем прогестерон, можем выполнить серкляж или установить пессарий. Главное: корректно определить показания к тому или иному методу лечения конкретно для каждой пациентки.
Обратимся к данным клинических исследований с участием женщин с ПР в анамнезе. Исследование J.M. Dodd et al. [36] включало оценку 8523 женщин с анамнезом ПР, получавших прогестерон или плацебо. Также оценивали 12 515 рожденных детей. Данная работа базировалась на 36 исследованиях. Было показано отсутствие принципиального значимого влияния схемы приема препарата, способа его введения, длительности терапии и дозы прогестерона на исходы беременности.
В исследовании A. Abdelaziz et al. [37] показано, что прогестерон обладает максимальной эффективностью именно при вагинальном способе введении по сравнению с внутримышечным, при том что и побочных эффектов в первом случае меньше.
Обратимся к недавнему мультицентровому интернациональному рандомизированному двойному слепому исследованию по оценке эффективности 17-ОПК у пациенток с привычной потерей одноплодной беременности [38]. Исследование длилось 12 лет, при этом не было достоверно показано значимой эффективности этой формы прогестерона, хотя в показаниях к применению этого препарата значится профилактика ПР. Более того, хочется отметить, что внутримышечная терапия 17-ОПК одобрена FDA у женщин с анамнезом спонтанного выкидыша при одноплодной беременности. Между тем внутримышечное введение сопровождалось болью (более чем у 30% пациенток), местными реакциями (припухлость, уплотнение в месте инъекций). Кроме того, это довольно дорогой метод лечения и экономически невыгодный для страховых компаний, а сама терапия в 3 раза повышает риск развития гестационного сахарного диабета [39–42].
Тактика ведения пациенток при укорочении шейки маткиВ связи с тем, что этиологических факторов развития данного состояния довольно много, трудно поверить, что один препарат будет высокоэффективен при данной патологии. Безусловно, у ряда пациенток с короткой шейкой матки будет применяться циркляж или пессарий на начальных сроках беременности. Однако в целом укорочение шейки матки мы можем лечить с помощью препарата микронизированного прогестерона, и достаточно успешно. Mетаанализ, проведенный R. Romero et al. [3], показал, что назначение вагинальной формы прогестерона при одноплодной беременности и наличии ультразвуковых характеристик укорочения шейки матки во второй половине беременности снижает риск ПР в сроке менее 33 нед. и улучшает неонатальные исходы без каких-либо явных нарушений и патологий развития плода. Эффект вагинальной формы прогестерона оценивали также в плане неблагоприятных перинатальных и неврологических исходов. Было показано, что терапия вагинальной формой микронизированного прогестерона снижает риск респираторного дистресс-синдрома плода, являющегося основным заболеванием и причиной смертности детей, рожденных с массой от 1500 до 2500 г. Неонатальная смертность составляла 1,4% на фоне применения прогестерона против 3,2% в группе плацебо.
Возвращаясь к сравнительному анализу микронизированного прогестерона с 17-ОПК для внутримышечного введения, авторы исследования отмечают, что еженедельные инъекции 17-ОПК не снижают частоту ПР у женщин с укорочением шейки матки (менее 30 мм) и поэтому не должны быть использованы с этой целью и по этим показаниям.
Эффективность акушерских пессариев при укорочении шейки матки
Группа испанских ученых оценила эффективность акушерских пессариев у женщин с короткой шейкой матки [43]. Акушерский пессарий показал обнадеживающие результаты в отношении профилактики ПР при назначении по результатам ультразвукового скрининга длины шейки матки в середине беременности.
Увы, в дальнейшем исследователи были разочарованы, так как в большей выборке данный эффект повторить не удалось и результаты были противоположными: в группе пациенток с одноплодной беременностью и короткой шейкой матки на 20–24-й неделе установка пессария не снижала частоту ПР и показатели перинатальной заболеваемости и смертности соответственно. Также из неблагоприятных эффектов акушерского пессария было отмечено повышение частоты влагалищных выделений у пациенток основной группы (86,7%) по сравнению с контрольной группой (46%) [44]. (Последние европейские рекомендации по установке акушерского пессария и тактике ведения пациенток с пессарием во время беременности написаны под руководством G.C. Di Renzo [45].)
Обратимся к систематическому обзору (выполнен группой канадских ученых) работ по применению различных форм прогестерона (вагинального, перорального, внутримышечного), использованию пессариев для профилактики ПР в группе риска — у пациенток с одноплодной беременностью [46]. Только вагинальная форма прогестерона показала свою эффективность для профилактики и предотвращения ПР у женщин с одноплодной беременностью, имевших в анамнезе ПР. В целом отмечено снижение рисков ПР у женщин с укорочением шейки матки менее 25 мм и анамнезом ПР при приеме вагинальной формы прогестерона.
А как же женщины с двойней? R. Romero et al. [47] в метаанализе оценивали применение вагинальной формы прогестерона у женщин с двойней. Заключение таково, что назначение вагинальной формы прогестерона при отсутствии клинической симптоматики у женщин с двойней и ультразвуковыми данными укорочения шейки матки в II триместре снижает риски ПР на сроках 30–35 нед. беременности, неонатальную смертность и некоторые показатели неонатальной заболеваемости, а также демонстрирует отсутствие неблагоприятного влияния на показатели здоровья ребенка.
Вопросу установки акушерских пессариев у женщин с двойней и укорочением шейки матки было посвящено мультицентровое исследование, проведенное группой испанских ученых [48]. Показана некоторая эффективность пессария при двойне, но доказательства в целом недостоверны.
В заключение стоит подумать о перспективах и применении на практике вышеизложенной информации. Совместно с русской группой исследователей нами опубликованы результаты комбинированного лечения предлежания плаценты у пациенток с высоким риском преждевременных родов [49]. Рандомизированное контролируемое исследование включало 217 пациенток с предлежанием плаценты, из которых 81 пациентке был назначен прогестерон и установлен пессарий Dr. Arabin, 136 получали только прогестерон. Миграцию плаценты отслеживали по результатам допплеровского исследования на сроках после 24 нед. Получены следующие результаты:
Пациентки с пессарием Dr. Arabin на фоне приема прогестерона имели троекратное снижение частоты кровотечений во время беременности (11,3%) по сравнению с контрольной группой (33,1%).
Миграция плаценты выявлялась в 1,8 раза чаще в группе женщин с пессарием (48,1%), чем в контрольной группе (26,4%).
ПР в сроке до 34 нед. случались в 2,7 раза реже в группе женщин с пессарием, чем у женщин контрольной группы.
Применение пессария Dr. Arabin способствовало открытию угла матки кпереди на 7,4°, что сопровождалось снижением индекса резистентности в дугообразных артериях на сроке 32–33 нед. в сравнении с контрольной группой.
ВыводыНазначение микронизированного прогестерона в лютеиновую фазу менструального цикла женщинам с анамнезом репродуктивных потерь будет благоприятно сказываться на планировании последующей беременности.
Микронизированный прогестерон имеет положительное влияние при угрозе прерывания беременности и анамнезе спонтанного выкидыша.
При выявлении укорочения шейки матки на любом сроке беременности будет правильно назначить микронизированный прогестерон в качестве терапии для снижения риска ПР и улучшения перинатальных исходов.
Пациенткам с анамнезом ПР рекомендуется лекарственная поддержка препаратом микронизированного прогестерона.
Женщинам с двойней и укорочением шейки матки должен быть рекомендован микронизированный прогестерон для снижения риска ПР и улучшения неонатальных исходов.
Остается важный вопрос: в какие сроки должна быть начата терапия микронизированным прогестероном, чтобы получить наиболее благоприятный результат в случае угрожающего выкидыша? Согласно данным крупного исследования PRISM в среднем 6–9 нед. беременности —
оптимальный срок для начала терапии. Это рекомендации для женщин вне зависимости от указания в анамнезе на репродуктивные потери.
Прогестерон в дозе 800 мг/сут в настоящее время рекомендован беременным женщинам с анамнезом репродуктивных потерь в I триместре беременности и с жалобами на кровяные выделения с момента их появления до 16–20 нед.
Кровяные выделения из половых путей в I триместре беременности при наличии в анамнезе двух и более выкидышей считаются фактором риска ПР. При наличии угрозы прерывания беременности разумно продолжить прием вагинальной формы прогестерона в дозе 200 мг/сут до 36 нед.
У пациенток с ПНБ назначение вагинальной формы микронизированного прогестерона рекомендуется на прегравидарном этапе во вторую фазу менструального цикла за 2–3 мес. до оплодотворения с продолжением во время беременности в дозе 800 мг/сут до 16–20 нед. гестации.
При наличии ультразвуковых критериев укорочения шейки матки при одноплодной беременности или у женщин с двойней рекомендуется назначение вагинальной формы прогестерона в дозе 200 мг/сут до 36 нед.
Таким образом, в заключение нужно отметить: никогда не сравнивайте яблоки и груши. Целесообразно применение в клинической практике микронизированного прогестерона, он подтверждает свою эффективность и безопасность с 1990-х годов. И сегодня мы знаем, как помочь разным категориям пациенток с проблемой невынашивания беременности.
Сведения об авторах:
Ди Ренцо Дж.К. — д.м.н., профессор Университета Перуджи; 06123, Италия, Перуджа, Университетская пл., д. 1; ORCID iD 0000-0003-4467-240X.
Доброхотова Юлия Эдуардовна — д.м.н., профессор, заведующая кафедрой акушерства и гинекологии лечебного факультета ФГАОУ ВО РНИМУ им. Н.И. Пирогова Минздрава России; 117997, Россия, г. Москва, ул. Островитянова, д. 1; ORCID iD 0000-0002-7830-2290.
Маркова Элеонора Александровна — к.м.н., ассистент кафедры акушерства и гинекологии лечебного факультета ФГАОУ ВО РНИМУ им. Н.И. Пирогова Минздрава России; 117997, Россия, г. Москва, ул. Островитянова, д. 1; ORCID iD 0000-0002-9491-9303.
Контактная информация: Маркова Элеонора Александровна, e-mail: [email protected]. Прозрачность финансовой деятельности: никто из авторов не имеет финансовой заинтересованности в представленных материалах или методах. Конфликт интересов отсутствует. Статья поступила 20.08.2020, поступила после рецензирования 14.09.2020, принята в печать 07.10.2020.
About the authors:
Gian Carlo Di Renzo — MD, PhD, FRCOG (hon) FACOG (hon) FICOG (hon) Past General Secretary of FIGO University of Perugia; 1, piazza Universitá, Perugia, 06123, Italy; ORCID iD 0000-0003-4467-240X.
Yuliya E. Dobrokhotova — Doct. of Sci. (Med.), Professor, Head of the Department of Obstetrics and Gynecology of Medical Faculty, Pirogov Russian National Research Medical University; 1, Ostrovityanov str., Moscow, 117437, Russian Federation; ORCID iD 0000-0002-7830-2290.
Eleonora A. Markova — Cand. of Sci. (Med.), assistant of the Department of Obstetrics & Gynecology of Medical Faculty, Pirogov Russian National Research Medical University; 1, Ostrovityanov str., Moscow, 117437, Russian Federation; ORCID iD 0000-0002-9491-9303.
Contact information: Eleonora A. Markova, e-mail: [email protected]. Financial Disclosure: no authors have a financial or property interest in any material or method mentioned. There is no conflict of interests. Received 20.08.2020, revised 14.09.2020, accepted 07.10.2020.
.
Иммуномодулирующая роль прогестерона в терапии угрозы прерывания беременности Текст научной статьи по специальности «Фундаментальная медицина»
УДК 618.3-06
© И.В. Сахаутдинова, Л.Р. Ложкина, 2014
И.В. Сахаутдинова, Л.Р. Ложкина ИММУНОМОДУЛИРУЮЩАЯ РОЛЬ ПРОГЕСТЕРОНА В ТЕРАПИИ УГРОЗЫ ПРЕРЫВАНИЯ БЕРЕМЕННОСТИ
ГБОУ ВПО «Башкирский государственный медицинский университет» Минздрава России, г. Уфа
В обзоре представлены данные об основных причинах прерывания беременности и влиянии прогестерона на процесс имплантации и течения беременности. Рассмотрены иммунологические аспекты невынашивания беременности, в частности взаимодействия между уровнем прогестерона, прогестеронпродуцированным блокирующим фактором и балансом ци-токинов. Освещены данные об интерлейкиновом каскаде, смещении соотношения провоспалительных и противовоспалительных цитокинов при физиологической беременности и угрозе прерывания беременности на ранних сроках. Представлены обзорные данные об иммуномодулирующей роли прогестерона в течении беременности, в частности осуществляемой посредством контроля уровня цитокинов. Произведен анализ литературных данных о применении экзогенного прогестерона в лечении невынашивания беременности. Влияние терапии прогестинами при угрозе прерывания беременности на баланс цитокинов.
Ключевые слова: прогестерон, угроза прерывания беременности, цитокины.
I.V. Sakhautdinova, L.R. Lozhkina IMMUNOMODULATORY ROLE OF PROGESTERONE IN THE THERAPY OF THREATENED MISCARRIAGE
The review presents data about the main causes of threatened miscarriage, progesterone influence on the process of implantation and pregnancy. The article looks into the immunological aspects of miscarriage, in particular, the interaction between progesterone level, progesterone-produced blocking factor and cytokine balance. The data about interleukin cascade, displacement ratio of pro-inflammatory and anti-inflammatory cytokines in physiological pregnancy and threatened miscarriage in early pregnancy are provided. The survey data about the immunomodulatory role of progesterone in pregnancy, in particular, carried out by controlling the level of cytokines, are presented.
The analysis of literature data about the use of exogenous progesterone in the treatment of miscarriage and the effect of progestin therapy in threatened miscarriage on the balance of cytokines is performed.
Key words: progesterone, threatened miscarriage, cytokines.
Проблема преждевременного прерывания беременности на ранних сроках остается одной из актуальных и социально значимых. Несмотря на активное внедрение новых препаратов для лечения, частота невынашивания беременности по-прежнему остается высокой и, по данным исследователей разных стран, составляет 15-20% [1]. Наибольшее количество (75-80%) репродуктивных потерь приходится на сроки беременности до 12 недель [2].
Доминирующую роль в генезе невынашивания играют генетические, инфекционные, анатомические, иммунологические и гормональные нарушения. Среди известных причин невынашивания беременности ведущее место занимают эндокринные и иммунологические факторы, доля которых составляет 67% [3].
В последнее время многие исследователи пытаются осмыслить значение иммунной системы в процессах репродукции. Установлено, что до 80 % такого нарушения фертиль-ности, как спонтанные аборты неясного гене-за, обусловлено действием именно иммунологических факторов [4].
По выражению профессора Люненфельда (2012) «плод — это совместный продукт двух гистонесовместимых индивидуумов», который развивается в полости матки, но материнский и плодный организмы не едины [5].
Принципиальную роль в подготовке слизистой оболочки матки к имплантации играет прогестерон. Доказано, что для нормального исхода беременности иммунная система женщины должна распознать беременность. При нормально протекающей беременности в лимфоцитах периферической крови присутствуют рецепторы прогестерона, причем доля клеток, содержащих такие рецепторы, возрастает по мере увеличения срока гестации [6,22].
После того, как была открыта цитоки-новая сеть, появились исследования, направленные на изучение иммунологического «парадокса» беременности [7], роли цитокинов при физиологической и осложненной беременности [8-11, 26, 27].
Именно цитокины обеспечивают взаимодействие эндокринной и иммунной систем, участвуя в высвобождении ряда гормонов [7,12]. Система цитокинов представляет собой полиморфную регуляторную сеть медиаторов, которые играют не только важную роль при воспалении слизистой оболочки матки, но и в регуляции физиологических процессов в эндометрии: пролиферации, имплантации, развитии эмбриона [10].
Т.О. Wegman (1993), являющийся одним из соавторов создания иммунотрофической концепции, доказал, что распознавание эмбрио-
нальных антигенов материнской иммунной системой ведет к активации местных иммуноком-петентных клеток и секреции ими двух видов цитокинов, а также факторов роста, способствующих сохранению беременности [7].
Согласно этой гипотезе во время беременности в иммунной системе происходит переключение иммунного ответа опосредованного Т-хелперами 1-го типа (провоспали-тельные цитокины — ФНО, ИЛ-ф,ИЛ-10) на иммунный ответ, опосредованный Т-хелперами 2-го типа (противовоспалительные цитокины — ИЛ-4,ИЛ-6,ИЛ-2, TGFбетта). Тогда как преобладание провоспалительных цитокинов приводит к потере зародыша. Образование локальной доминанты противовоспалительных цитокинов предупреждает агрессию материнских клеток на бластоцисту и зародыш, несущие антигены отца.2). У женщин со спонтанными выкидышами в анамнезе концентрация воспалительных (ТЫ) цитокинов была значимо выше.
Все большее количество исследований доказывает существенную роль прогестерона в формировании адекватного иммунного ответа на ранних сроках беременности. Именно он руководит иммунными процессами здоровой гестации [5].
Впервые предположение о дефиците прогестерона как о причине спонтанного прерывания беременности было высказано профессором Люненфельдом (1969) [5].
В процессе развития беременности наблюдается период физиологического снижения концентрации прогестерона в сыворотке крови, который совпадает с передачей био-
синтеза гормона от желтого тела к плацентарным структурам (синцитиотрофобласт). Этот период (6 -9-я недели беременности) называют «лютеоплацентарной сменой» и на него приходится основная часть случаев самопроизвольного аборта, что еще раз подтверждает значение прогестерона для успешного развития беременности. Концентрация прогестерона неуклонно повышается во время беременности и составляет 80-140 ммоль/л в I триместре, 1900-8200 и 6500-23 000 ммоль/л — во II и III триместрах.
На уровне эндометрия прогестерон осуществляет секреторную трансформацию, подготавливая слизистую оболочку к имплантации. При недостаточной продукции прогестерона в слизистой оболочке матки наблюдаются недоразвитие желез, стромы, сосудов, недостаточное накопление гликогена, белков, фактора роста и других веществ, необходимых для развития эмбриона. Все это создает неблагоприятные условия для адекватного развития трофобласта и питания зародыша, что обуславливает прерывание беременности в первом триместре [13].
Подготовка репродуктивной системы для инициации поддержания беременности прогестероном заключается в дифференци-ровке стромального компонента эндометрия, стимуляции секреции желез и накоплении в них базальных вакуолей, замене гамма секреции белков эндометрием и обеспечении «покоя» миометрия [5, 7].
Иммунологическое действие прогестерона осуществляется посредством контроля продукции цитокинов [23, 24].
При нормально протекающей беременности желтое тело, а позже плацента вырабатывают достаточное количество прогестерона. В его присутствии активируемые лимфоциты вырабатывают специальный белок -прогестерониндуцированный блокирующий фактор (ПИБФ), который изменяет соотношение Т-хелперов в пользу ТЬ2. Т-хелперы второго типа опосредованно могут прекратить превращение NK-клеток в лимфокин-активированные киллеры, подстегнув производство факторов роста плаценты и естественных иммуносупрессоров [19, 29].
Прогестерониндуцированный блокирующий фактор, усиливающий иммуномодули-рующее и антиабортивное действия прогестерона, предотвращает отторжение наполовину чужеродного плода. Этот протеин обеспечивает цитопротективный характер иммунного ответа, предотвращает воспалительные и тромботические вторичные реакции на тро-фобласт [26].
Таким образом, одним из патогенетических факторов, лежащих в основе формирования невынашивания беременности, является недостаточная продукция прогестерона.
Первые работы о возможности использования прогестинов для восполнения недостатка эндогенного прогестерона в терапии угрозы прерывания беременности появились в 1953 году.
В 2005 году M. EI-Zibden проводилось сравнение применения перорального прогестерона, внутримышечного хорионического гонадотропина человека (ХГЧ) и отсутствие дополнительной терапии. В группе с использованием дидрогестерона частота прерывания беременности была ниже, чем в контрольной (13% против 29%) [20].
В 2012 году опубликованы результаты метанализа индивидуальных данных пациенток с интравагинальным введением прогестерона при укорочении шейки матки и риске прерывания беременности.2 переключение, следствием которого является формирование физиологической цитокин опосредованной иммуносупрессии [25]. Было доказано, что экзогенный прогестерон блокирует ин-терлейкиновый каскад, что снижает активность воспалительного процесса.
В работе Т.М. Соколовой и А.В. Усовой (2010) было убедительно показано, что назначение экзогенного прогестерона при угрозе прерывания беременности во II триместре блокирует интерлейкиновый каскад [21].
Данные Кокрановского обзора (2011) продемонстрировали отсутствие статистической разницы в частоте потери беременности 1-П триместров в группах женщин, получавших гестагены, плацебо и не получавших лечение. Однако у женщин с привычным невынашиванием применение гестагенов приводило к достоверно значимому снижению частоты потери беременности. К сожалению, данный обзор не содержит выводов о различиях по влиянию различных прогестинов на частоту выкидышей ранних сроков [17]. В исследованиях Э.Ю. Доброхотовой и соавт. [2] показано, что дидрогестерон обладает мощным
иммуномодулирующим действием, способствуя снижению иммунной агрессии материнских клеток в отношении развивающегося эмбриона. Доказано, что дидрогестерон приводит к повышению концентрации ПИБФ-позитивных лимфоцитов, что влечет за собой изменения в иммунной системе, направленные на сохранение беременности.
Касаясь вопросов лечения угрозы прерывания беременности, в литературе нет однозначного мнения о целесообразности назначения того или иного препарата, в том числе и экзогенного прогестерона, для пролонгирования беременности [3, 17].
Эффективность применения экзогенного прогестерона при привычном невынашивании беременности не подлежит сомнению, но вопросы, касающиеся обоснованности применения у первобеременных женщин в терапии угрозы прерывания, требуют дальнейшего изучения. Многие исследователи считают, что сохраняющая терапия у данного контингента пациенток является неоправданной [17].
Исследования в небольших группах пациенток показали позитивный эффект применения прогестинов в лечении угрозы прерывания на ранних сроках. Публикации, посвященные использованию прогестинов у первоберемен-ных женщин, единичны, а ведь именно исход первой беременности и первых родов — это показатель репродуктивного здоровья женщины, соматического здоровья и репродуктивного потенциала будущих поколений [18].
На основании анализа литературных данных можно сделать вывод о значимости эндогенного прогестерона на процесс наступления и течения беременности. Применение прогестагенов в терапии угрозы прерывания беременности у женщин с привычным невынашиванием беременности в анамнезе эффективно. Следует отметить тот факт, что, по мнению большинства исследователей, требуется проведение дальнейших исследований применения экзогенного прогестерона в терапии угрозы прерывания беременности у пер-вобеременных женщин, которое должно включать определение групп риска по невынашиванию беременности среди первобере-менных женщин, выявление маркеров невынашивания беременности, определение терапевтических условий применения экзогенного прогестерона у данного контингента женщин.
Сведения об авторах статьи: Сахаутдинова Индира Венеровна — д.м.н., профессор, зав. кафедрой акушерства и гинекологии №3 ГБОУ ВПО БГМУ Минздрава России. Адрес: 450000, г. Уфа, ул. Ленина, 3. Тел./факс: 8(347)232-69-55.
Ложкина Лариса Расилевна — аспирант кафедры акушерства и гинекологии N°3 ГБОУ ВПО БГМУ Минздрава России. Адрес: 450000, г. Уфа, ул. Ленина, 3. E-mail: [email protected].
ЛИТЕРАТУРА
1. Сидельникова, В.М. Эндокринология беременности в норме и патологии / В.М. Сидельникова. — М.: МЕДпрессинформ, 2007. -352 с.
2. Роль прогестеронзависимой иммуномодуляции и рецептивности эндометрия в невынашивании беременности / Ю.Э. Доброхотова [и др.] // Проблемы репродукции. — 2009. — № 5. — С. 59-62.
3. Сидельникова, В.М. Привычная потеря беременности / В.М. Сидельникова. — М.: Триада-Х, 2006. — 304 с.
4. Иммунологические и генетические факторы нарушения репродуктивной функци / В.А. Черешнев [и др.]. — Екатеринбург: УрО РАН, 2005. — 174 с.
5. Маклецова, С.А. Роль прогестерона в имплантации и ранней беременности: от истории вопроса к современным решениям / С.А. Маклецова, И.Д Ипастова // Status Praesens. — 2013. — № 3. — С. 111-116.
6. Сидельникова, В.М. Невынашивание беременности — современный взгляд на проблему / В.М. Сидельникова // Рос. вестн. акушерства и гинекологии. — 2007. — № 2. — С. 62-65.
7. Причины и дифференцированное лечение раннего невынашивания беременности: руководство для врачей /под ред. А.П. Ми-лованова, О.Ф. Серовой. — М.: Студия МДВ, 2011. — 214 с.
8. Тетруашвили, Н.К. Роль иммунных взаимодействий на ранних этапах физиологической беременности и при привычном выкидыше / Н.К. Тетруашвили // Иммунология. — 2008. — № 2. — С. 124-129.
9. Усова, А.В. Содержание про- и провоспалительных цитокинов у женщин с невынашиванием беременности после проведения сохраняющей терапии. / А.В. Усова, Ю.В. Начаров, Т.М. Соколова // Вестн. новых мед. технологий. — 2008. — Т. XV, № 2. — С. 50-52.
10. Цитокиновый профиль женщин с угрозой прерывания беременности и его модуляция препаратом Дюфастон / Н.Ю. Сотникова [и др.] // Журн. акушерства и женских болезней. -2006. — Т. LV, № 2. — C. 42-45.
11. Бапаева, Т.Б. Взаимосвязь между прогестероном и цитокинами при привычном невынашивании беременности / Т.Б. Бапаева, Н.М. Мамедалиева // Проблемы репродукции. — 2005. — № 5. — С. 93-96.
12. Ширшев, С.В. Цитокины плаценты в регуляции иммунноэндокринных процессов при беременности / С.В. Ширшев // Успехи соврем. биологии. — 1994. — № 114. — С. 223-237.
13. Оценка экспрессии м-РНК генов цитокинов в эндометрии при хроническом эндометрите / Н.А. Гомболевская [и др.] // Акушерство и гинекология. — 2013. — № 11. — С.35-40.
14. Межевитинова, Е.А. Возможности применения дидрогестерона у женщин с недостаточностью лютеиновой фазы менструального цикла / Е.А. Межевитинова. Э.Р. Довлетханова // Гинекология. — 2010. — № 3. — С. 5-28.
15. Сидельникова, В.М. Неполноценная лютеиновая фаза — тактика ведения пациенток с привычной потерей беременности / В.М. Сидельникова // Гинекология. — 2002. — № 4. -С. 7-10.
16. Тихомиров, А.Л. Привычное невынашивание беременности: причины, диагностика и современные подходы к терапии / А.Л. Тихомиров, Д.М. Лубнин // Фарматека. — 2004. — Т. 80, № 1. — С. 28-39.
17. Радзинский, В.Е. Акушерская агрессия / В.Е. Радзинский. — М.: Status Praesens, 2011. — 688 с.
18. Ушакова, Г.А. Воспроизводство населения и репродуктивное здоровье женщин Кузбасса / Г.А. Ушакова, Л.Б. Николаева. — М.: ГЭОТАР-Медиа, 2010. — 176 с.
19. Соколов, Д.И. Иммунологический контроль формирования сосудистой сети плаценты / Д.И. Соколов, С.А. Сельков. — СПб.: Издательство Н-Л, 2012. — 206 с.
20. Полухова, Е.В. Сохранение беременности: оценка эффективности применения прогестагенов: реферат / Е.В. Полухова // Consilium Medicum. — 2012. — Т. 14, № 6. — С. 77-80.
21. Усова, А.В. Оценка основных показателей цитокинового профиля у женщин с угрозой прерывания беременности и на фоне ее лечения: дис. … канд. мед. наук. — Омск, 2010 — 129 с.
22. Progesterone inhibits in-vitro embryotoxis Th2 cytokine production to trophoblast in women with recurrent pregnancy loos / B.C Choi [et.al.] // Hum. Reprod. — 2000. — Vol. 15, № 1. — p. 46-59.
23. Progesterone and non-specific immunological mechanisms in pregnancy / J. Szekeres-Bartho [et al] // Am. J. Reprod. Immunal. — 1997. — Vol.38, № 3. — p. 176-182.
24. Szekeres-Bartho, J. / Progesterone receptor-mediated immunomodulation and anti-abortive effects: The role of PIBF / J. Szekeres-Bartho // Ginecol Endocrinon. — 2001. — Vol. 15, № 5. — p. 43-47.
25. Szekeres-Bartho, J. Progesterone-dependent immunomodulatoryprotein alters the Th2/Th3 balance / J. Szekeres-Bartho, T.G. Wegman // Am. J. Reprod. Immunol. — 1996. — Vol. 31. — p. 81-95.
26. Kalinka, J. Влияние дидрогестерона на гормональный профиль и концентрацию прогестерон-индуцированного блокирующего фактора у беременных с угрожающим абортом / J. Kalinka, J. Szekeres-Bartho // Журн. акушерства и женских болезней. — 2005. -Т. LIV, № 1, — С. 96-101.
27. Casart Y., Tarazzi K., Camejio M. Serum levvels of interleukin-6, inerleukin-lbeta and human chorionic gonadotropin in in preeclamptic and normal pregnancy. Gynecol. Endocrinol. 2007; 23(5): 300-20.
28. Salamonsen L.A. Cytokines and cemokines during human embryoimplantation: roles in implantation and early placentation. Semin. Reprod. Med. 2007; 25(6):437-44.
29. Szekeres-Bartho J. Progesteronr receptor-mediated immunonomodulation and anti-abortive effects: The role of PIBF. Ginecol Endo-crinol 2001: 15: 5: 43-47.
30. Romero J., Rebarbeer A., Saltzman D.H., Schwartz R., et al. The prediction of recurent preterm birth in patients on 17-alpha-hydroxyprogesterone ceproate using serial fetal fibronectin and cervical lenght. American Journal of Obstetrics and Gynecology, 2012, 207, 51-55.
Прерывание беременности — Медицинский центр СОЮЗ
Прерывание беременности в Иркутске проводится у женщин с помощью препарата “Мифепристон” без инструментального вмешательства в полость матки, что значительно уменьшает возможность развития осложнений аборта часто приводящего к бесплодию. Это называется медикаментозное (таблетированное) прерывание беременности на ранних сроках.
“Мифепристон” – это антипрогестероновый препарат для медикаментозного прерывания беременности (прерывание беременности таблетками) на ранних сроках. Давно известно, что прерывание беременности представляет собой значительный риск для жизни вообще и, в частности для репродуктивного (репродукция – воспроизводство себе подобных) здоровья женщин.
К сожалению, в г.Иркутске аборт остается одним из способов “планирования семьи”, если нельзя отказаться от искусственного прерывания беременности методом аборта, то нужно свести к минимуму риск осложнений. Поэтому поиски щадящих методов прерывания беременности на ранних сроках, привели к созданию антипрогестероновых препаратов, одним из которых является “Мифепристон”. Мифепристон – таблетированный синтетический стероидный препарат разработан и лицензирован для медикаментозного прерывания беременности на ранних сроках, клинический эффект которого обусловлен действием прогестерона на уровне рецепторов. Препарат был рекомендован в качестве средства терапевтического прерывания беременности при малом сроке и является альтернативой хирургическому методу прерывания беременности.
Этапы проведения медикаментозного аборта
Мифепристон применяется только в медицинских учреждениях.
Медикаментозный аборт 1-ый этап
При первом визите к врачу проводится беседа с пациенткой о целесообразности прерывания беременности именно этим методом и об особенностях действия препарата. Пациентку информируют о порядке прерывания беременности таблетированным методом, сути метода, симптомах, возможных вариантах течения аборта.
Назначается обследование:
мазок на степень чистоты влагалища.
УЗИ органов малого таза для подтверждения маточной беременности.
Медикаментозный аборт 2-ой этап
Пациентка принимает внутрь три таблетки – 600 мг Мифепристон в присутствии врача, и находится под наблюдением врача в течение 1-2 часов, после чего может уйти домой. При этом пациентка получает памятку, в которой указано, куда следует звонить или обращаться в случае необходимости. Спустя 36-48 часов необходимо повторно явиться к врачу.
Медикаментозный аборт 3-ий этап
Повторная явка к врачу через 36-48 часов, пациентка дважды принимает внутрь Мизопростол 400 мг – 2 таблетки. Изгнание плодового яйца происходит либо когда Вы находитесь в медицинском центре, реже в один из последующих дней дома. Кровянистые выделения(скудные) обычно продолжается от 7 до 14 дней. Однако в течение текущего месяца тест на беременность по моче будет положительным, поэтому делать его не следует.
Медикаментозный аборт 4-ий этап
На 10-14 день после 2-го этапа пациентка должна приехать в мед.центр «СОЮЗ» на контрольное УЗИ, для того, чтобы убедиться, полностью ли был изгнан плод.
При проведении таблетированного аборта:
Появляются тянущие боли внизу живота, вовремя экспульсии (выхода) плодного яйца – схваткообразные боли и усиления кровянистых выделений.
Кровянистые выделения из половых путей, которые по количеству соответствующих месячным или немного больше.
Послеабортный период может характеризоваться кровянистыми выделениями из половых путей до 10 дней.
Медикаментозное прерывание беременности на ранних сроках в Нижнем Новгороде в клинике Тонус, сделать медицинский аборт, мини аборт
Раннее прерывание беременности. Медикаментозный аборт
Медикаментозное прерывание беременности – это один из самых безопасных методов и является прекрасной альтернативой хирургическому аборту. Медикаментозный аборт проводится на сроке до 6 недель беременности. При проведении медикаментозного прерывания беременности на ранних сроках используются лекарственные препараты, по своему механизму действия подавляющие синтез прогестерона.
Медикаментозный аборт выполняется только под строгим контролем врача-гинеколога. После медикаментозного прерывания беременности обязательно проведение УЗИ для осмотра полости матки.
Прерывание беременности на ранних сроках методом медикаментозного аборта не нарушает репродуктивную функцию женщины. По данным множества исследований, после проведения медикаментозного прерывания беременности восстановление овуляции происходит в кратчайшие сроки. Дополнительным положительным качеством медикаментозного аборта считается возможность его проведения непосредственно в день обращения.
Прерывание беременности на ранних сроках – мини-аборт
Мини-аборт как метод раннего прерывания беременности можно проводить на сроке с 6 по 12 неделю. Основная методика проведения мини-аборта – это вакуум-аспирация. Плодное яйцо удаляется из полости матки с помощью специального электрического отсоса. Этот вариант раннего прерывания беременности носит более щадящий характер, чем стандартные варианты хирургического аборта.
Нельзя забывать о том, что чем раньше сделать аборт, тем меньше риск возникновения осложнений.
Процедура длится около 5 минут, женщина может пойти домой уже через несколько часов после выполнения манипуляции. Слизистая матки, в отличие от выскабливания, травмируется незначительно. Противопоказанием к проведению прерывания беременности таким способом является наличие инфекции в остром периоде. После проведения мини-аборта выполняется контрольное УЗ-исследование полости матки.
Где сделать аборт?
Многие женщины (особенно юного возраста), чтобы не афишировать беременность начинают искать варианты, где сделать аборт. Нужно запомнить, что правильнее всего сделать аборт, в клинике, под наблюдением специалистов, а не с помощью народных средств.
Прерывание беременности на ранних сроках однократным приемом мифепристона (RU 486), антагониста прогестерона
Eur J Obstet Gynecol Reprod Biol . 1988 июл; 28 (3): 249-55. DOI: 10.1016 / 0028-2243 (88)-4.Принадлежности Расширять
Принадлежность
- 1 Service de Gynécologie-Obstétrique, Centre Hospitalier Intercommunal, Франция.
Элемент в буфере обмена
B Maria et al. Eur J Obstet Gynecol Reprod Biol. 1988 июл.
Показать детали Показать вариантыПоказать варианты
Формат АннотацияPubMedPMID
Eur J Obstet Gynecol Reprod Biol .1988 июл; 28 (3): 249-55. DOI: 10.1016 / 0028-2243 (88)-4.Принадлежность
- 1 Service de Gynécologie-Obstétrique, Centre Hospitalier Intercommunal, Франция.
Элемент в буфере обмена
Полнотекстовые ссылки Опции CiteDisplayПоказать варианты
Формат АннотацияPubMedPMID
Абстрактный
Мифепристон (RU 486) — новый стероид, который является антагонистом прогестерона и способен прерывать беременность на ранних сроках без каких-либо серьезных побочных эффектов.Целью нашего исследования было оценить клинический эффект однократного перорального приема 600 мг препарата на ранних сроках беременности. В исследование были включены 150 здоровых женщин, обращающихся за легальным абортом, с аменореей продолжительностью не более 42 дней. Беременность подтверждена клиническим и ультразвуковым обследованием, оценкой ХГЧ плазмы. Успех предполагался повторением этих экзаменов на восьмой день. У 131 пациентки был полный аборт (87,3%) с очень небольшим количеством побочных эффектов. Только двум пациентам потребовалось выскабливание из-за сильного кровотечения.Мифепристон может прервать беременность на ранних сроках амбулаторно под наблюдением врача.
PIP: Мифепристон, новый антагонист стероидов и прогестерона, был назначен 150 женщинам с аменореей менее 42 дней, которые хотели сделать аборт. Каждой женщине давали однократную дозу 600 мг для приема внутрь дома вечером.Женщинам объяснили, какие клинические события должны произойти, и им дали постоянный номер телефона экстренной помощи. Контрольные визиты были запланированы на 8-й день, когда были выполнены клинические тесты, ультразвуковые исследования и забор крови. Успех предполагался, если вагинальное кровотечение произошло между 3-8 днями, ультразвуковое исследование подтвердило пустоту матки и наблюдалось снижение уровня ХГЧ в плазме. Считается, что в общей сложности 131 из 150 женщин сделали полный аборт. Остальные 19 женщин включали 14 развивающихся беременностей, 2 выскабливания при сильном кровотечении и 1 внематочную беременность.Суточное количество и продолжительность кровотечения сравнивали с обильными менструациями. Только 2 женщины сообщили о сильном кровотечении, которое привело к выскабливанию. Только у 16 женщин уровень гемоглобина был достаточно низким, чтобы оправдать терапию железом. Никому не потребовалось переливание крови. Сообщалось о нескольких других побочных эффектах — сокращения матки и боли в области таза, преходящая астения и легкая тошнота. Все биологические тесты остались в пределах нормы. Показав уровень успеха 87,3% и с легкими побочными эффектами, мифепристон оказался простым и безопасным средством для прерывания беременности на ранних сроках и хорошей альтернативой хирургическому аборту.
Похожие статьи
- Прерывание на очень ранних сроках беременности RU 486 — антипрогестивным препаратом.
Ковач Л., Сас М., Реш Б.А., Угочсай Г., Суан М.Л., Бигдеман М., Роу П.Дж. Ковач Л. и др. Контрацепция. 1984 Май; 29 (5): 399-410. DOI: 10.1016 / 0010-7824 (84)
-3. Контрацепция.1984 г. PMID: 6744860
- Антипрогестероны для прерывания беременности.
Бигдеман М, Ван Лук П.Ф. Bygdeman M, et al. Baillieres Clin Obstet Gynaecol. 1988 сентябрь; 2 (3): 617-29. DOI: 10,1016 / s0950-3552 (88) 80048-8. Baillieres Clin Obstet Gynaecol. 1988 г. PMID: 3069265 Рассмотрение.
- Индукция терапевтического аборта на ранних сроках беременности мифепристоном в сочетании с простагландиновым пессарием.
Роджер М.В., Бэрд Д.Т. Роджер М.В. и др. Ланцет. 19 декабря 1987 г .; 2 (8573): 1415-8. DOI: 10,1016 / s0140-6736 (87)-3. Ланцет. 1987 г. PMID: 2891991
- Прерывание беременности на ранних сроках антагонистом прогестерона RU 486 (мифепристон).
Couzinet B, Le Strat N, Ulmann A, Baulieu EE, Schaison G. Couzinet B, et al. N Engl J Med.1986, 18 декабря; 315 (25): 1565-70. DOI: 10.1056 / NEJM198612183152501. N Engl J Med. 1986 г. PMID: 3785321
- Антигестагены.
Бэрд Д.Т. Бэрд Д.Т. Br Med Bull. 1993 Янв; 49 (1): 73-87. DOI: 10.1093 / oxfordjournals.bmb.a072607. Br Med Bull. 1993 г. PMID: 8324617 Рассмотрение.
Процитировано
5 статей- Ослабленное ограничение и функциональная дивергенция рецептора прогестерона (PGR) в человеческой стволовой линии.
Маринич М., Линч В.Ю. Маринич М. и др. PLoS Genet. 2020 17 апреля; 16 (4): e1008666. DOI: 10.1371 / journal.pgen.1008666. eCollection 2020 Апрель. PLoS Genet. 2020. PMID: 32302297 Бесплатная статья PMC.
- Лизосомные болезни накопления.
Platt FM, d’Azzo A, Davidson BL, Neufeld EF, Tifft CJ. Платт Ф.М. и др. Nat Rev Dis Primers.1 октября 2018 г .; 4 (1): 27. DOI: 10.1038 / s41572-018-0025-4. Nat Rev Dis Primers. 2018. PMID: 30275469 Рассмотрение.
- Дифференциальная экспрессия белков AP-1 миометрия во время беременности и родов.
Надим Л., Фарин Т., Дорогин А., Матысяк-Заблоцкий Е., Шынлова О., Лай С. Надим Л. и др. J Cell Mol Med. 2018 Янв; 22 (1): 452-471. DOI: 10.1111 / jcmm.13335. Epub 2017 25 сентября.J Cell Mol Med. 2018. PMID: 28945005 Бесплатная статья PMC.
- Молекулярные доказательства функциональной отмены прогестерона в миометрии человека.
Надим Л., Шынлова О., Матысяк-Заблоцкий Е., Мезиано С., Донг Х, Лай С. Надим Л. и др. Nat Commun. 2016 25 мая; 7: 11565. DOI: 10,1038 / ncomms11565. Nat Commun. 2016 г. PMID: 27220952 Бесплатная статья PMC.
- Мифепристон.Обзор его фармакодинамических и фармакокинетических свойств и терапевтического потенциала.
Брогден Р.Н., Гоа К.Л., Фолдс Д. Brogden RN, et al. Наркотики. 1993 Март; 45 (3): 384-409. DOI: 10.2165 / 00003495-199345030-00007. Наркотики. 1993 г. PMID: 7682909 Рассмотрение.
Условия MeSH
- Абортивные средства, стероидные *
- Аборт, Легальный / Методы
- Зависимость доза-реакция, лекарство
- Триместр беременности, первый / эффекты лекарств *
- Прогестерон / антагонисты и ингибиторы *
Вещества
- Абортивные средства, стероидные
LinkOut — дополнительные ресурсы
Источники полных текстов
Источники другой литературы
Медицинские
Прогестерон для предотвращения прерывания беременности после начала медикаментозного аборта мифепристоном
Вступление: Решение об аборте часто бывает трудным и болезненным для женщины.Возможно, большее беспокойство возникает, когда женщина делает медикаментозный аборт, но затем передумает и желает сохранить беременность, которой сейчас угрожает опасность. В одной опубликованной серии случаев подробно описан потенциальный метод противодействия абортивному эффекту мифепристона путем парентерального введения прогестерона в таких ситуациях.
Цели: В настоящем отчете подробно описаны случаи, когда женщины в аналогичных обстоятельствах получали прогестерон.Цели состояли в том, чтобы задокументировать случаи, когда женщины изменили свое мнение после начала медикаментозного аборта, а также изучить некоторые противоречия и клинические вопросы, связанные с их обстоятельствами.
Методы: Женщины, которые начали медикаментозный аборт путем приема мифепристона, но не принимали мизопростол, в тот же день самостоятельно обратились в национальную службу поддержки беременных.Пациенты, соответствующие критериям для лечения, получали пессарии с прогестероном во влагалище в течение двух недель.
Полученные результаты: Случаи: 28-летняя женщина, срок беременности 6 недель плюс 1 день; 35-летняя женщина, срок беременности 8 недель плюс 5 дней; и 27-летняя женщина, срок беременности 7 недель плюс 3 дня. Исходы соответственно были: здоровый ребенок мужского пола, родившийся на 39 неделе беременности; рождение здорового ребенка мужского пола в срок; и завершенный медикаментозный аборт.
Выводы: Женщины передумали после медикаментозного аборта. Использование прогестерона на ранних сроках беременности сопряжено с низким риском, и его применение для противодействия действию мифепристона в таких обстоятельствах может быть клинически полезным для сохранения ее беременной, находящейся под угрозой. Однако для получения окончательных доказательств необходимы дальнейшие исследования.
Ключевые слова: Аборт; лица, ищущие аборта; принуждение; информированное согласие; мифепристон; использование не по назначению; прогестерон; репродуктивные права.
Таблетка для аборта | Получите факты о медикаментозном аборте
Что такое таблетка для прерывания беременности?
Медикаментозный аборт — также называемый таблеткой для прерывания беременности — это безопасный и эффективный способ прервать беременность на ранних сроках.
Как действуют таблетки для прерывания беременности?
«Таблетка для прерывания беременности» — это общее название для использования двух разных лекарств для прерывания беременности: мифепристона и мизопростола.
Сначала вы принимаете таблетку мифепристон.Беременности для нормального роста нужен гормон прогестерон. Мифепристон блокирует выработку собственного прогестерона в организме, останавливая рост беременности.
Затем вы принимаете второе лекарство, мизопростол, сразу или в течение 48 часов. Это лекарство вызывает спазмы и кровотечение из матки. Это похоже на действительно тяжелые, спастические периоды, и процесс очень похож на ранний выкидыш. Если в течение 24 часов после приема второго лекарства у вас не будет кровотечения, позвоните медсестре или врачу.
Ваш врач или медсестра передаст вам оба лекарства в поликлинике. Когда и где вы их возьмете, зависит от законов штата и правил вашего медицинского центра. Ваш врач или медсестра дадут вам подробные инструкции о том, где, когда и как принимать лекарства. Вы также можете получить антибиотики, чтобы предотвратить инфекцию.
Насколько эффективны таблетки для прерывания беременности?
Таблетка для прерывания беременности очень эффективна. Эффективность зависит от того, на каком этапе беременности вы принимаете лекарство.
- Для людей, находящихся на 8 неделе беременности или меньше, это работает примерно 94-98 раз из 100.
- Для людей на сроке беременности 8–9 недель он работает примерно в 94–96 случаях из 100.
- Для людей на 9-10 неделе беременности он работает примерно в 91-93 раза из 100. Если вам дадут дополнительную дозу лекарства, оно сработает примерно в 99 случаях из 100.
- Для людей на 10-11 неделе беременности он работает примерно в 87 случаях из 100. Если вам дадут дополнительную дозу лекарства, оно сработает примерно в 98 раз из 100.
Таблетки для прерывания беременности обычно работают, но если они не работают, вы можете принять еще лекарства или сделать аборт в клинике, чтобы завершить аборт.
Когда я могу принимать таблетки для прерывания беременности?
В зависимости от того, где вы живете, вы можете сделать медикаментозный аборт в течение 77 дней (11 недель) после первого дня последней менструации. Если с первого дня последней менструации прошло 78 дней или более, вы можете сделать аборт в клинике, чтобы прервать беременность.
Почему люди выбирают таблетки для прерывания беременности?
Какой вид аборта вы выберете, зависит от ваших личных предпочтений и ситуации.Некоторым людям нравится медикаментозный аборт, что вам не нужно проходить процедуру в кабинете врача. Вы можете сделать медикаментозный аборт дома или в другом удобном месте по вашему выбору. Вы сами решаете, с кем хотите быть во время аборта, или можете сделать это в одиночку. Поскольку медикаментозный аборт похож на выкидыш, многие люди считают его более «естественным» и менее инвазивным.
Ваш врач, медсестра или персонал медицинского центра могут помочь вам решить, какой вид аборта вам лучше всего подходит.
Еще вопросы от пациентов:
Можно ли отменить таблетку для прерывания беременности после того, как вы ее приняли?Вот в чем дело: «Таблетка для прерывания беременности» — это популярное название безопасного и эффективного способа прерывания беременности на ранних сроках с помощью комбинации двух лекарств: мифепристона и мизопростола. Первое лекарство (мифепристон) выдается в поликлинике или в офисе вашего лечащего врача. После приема мифепристона через 6-48 часов вы принимаете второй препарат (мизопростол) дома.Это вызывает спазмы, кровотечение и опорожнение матки.
Заявления о методах лечения, которые обращают вспять эффекты медикаментозного аборта, существуют, и несколько штатов требуют, чтобы врачи и медсестры рассказывали о них своим пациентам, прежде чем они смогут оказать помощь при аборте. Но эти утверждения не были подтверждены надежными медицинскими исследованиями — и не были проверены на безопасность, эффективность или вероятность побочных эффектов — поэтому такие эксперты, как Американский колледж акушеров и гинекологов, отвергают эти непроверенные предполагаемые методы лечения.
Исследования таблеток для прерывания беременности действительно показывают, что если вы примете первое лекарство, а не второе, вероятность того, что таблетка для прерывания беременности не подействует, снизится. Поэтому, если вы начали процесс прерывания беременности с помощью таблеток для прерывания беременности, но у вас возникли сомнения, сразу же обратитесь к врачу или медсестре, с которыми вы обратились для прерывания беременности, чтобы обсудить свои лучшие следующие шаги и чего ожидать.
Что такое таблетка для прерывания беременности RU-486?RU-486 — бывшее название мифепристона — одного из лекарств, которые вы принимаете для медикаментозного аборта.RU-486 теперь называется «таблетка для прерывания беременности» или «Мифепрекс» (торговая марка мифепристона).
РУ-486 был разработан в 1980-х годах. Он безопасно используется в Европе с 1987 года и в США с 2000 года.
RU-486 блокирует гормон, необходимый вашему организму для продолжения беременности. Лучше всего он работает, когда вы используете его с другим лекарством, называемым мизопростолом, которое вызывает кровотечение, опорожняющее вашу матку.
Таблетка для прерывания беременности RU-486 — безопасный и эффективный способ прервать беременность на ранних сроках.
Была ли эта страница полезной?Помогите нам стать лучше — чем эта информация может быть полезнее?
Как эта информация вам помогла?
Ты лучший! Спасибо за ваш отзыв.
Спасибо за ваш отзыв.
Psst! Я Ру.
Есть вопросы? Наш конво частный.
ТЕПЕРЬ ГОВОРИТЕPsst! Я Ру.
Есть вопросы? Наш конво частный.
ТЕПЕРЬ ГОВОРИТЕPsst! Я Ру.
Есть вопросы? Наш конво частный.
ТЕПЕРЬ ГОВОРИТЕНам не удалось получить доступ к вашему местоположению, выполните поиск местоположения.
Пожалуйста, заполните это поле.Услуга Все услуги Аборт Направление к специалистам по прерыванию беременности Контроль рождаемости COVID-19 вакцина ВИЧ услуги ЛГБТК-услуги Уход за мужским здоровьем Душевное здоровье Таблетка Morning-After (Экстренная контрацепция) Тестирование на беременность и услуги Первая помощь Тестирование на ЗППП, лечение и вакцины Уход за женским здоровьем
Фильтровать по Все Телездравоохранение Лично
Поиск
Или позвоните по телефону 1-800-230-7526
Как работают таблетки для прерывания беременности и чего мне ожидать?
Таблетка для прерывания беременности вызывает спазмы и кровотечение, которые могут длиться несколько часов и более.Вы можете быть дома или в любом удобном для вас месте. Постарайтесь расслабиться в течение дня.
Что мне нужно сделать, прежде чем я приму таблетку для прерывания беременности?
Перед тем, как принять таблетку для прерывания беременности, вы встретитесь со своей медсестрой, врачом или персоналом медицинского центра, чтобы обсудить, является ли аборт правильным решением для вас и какие у вас есть варианты аборта. Вы пройдете обследование и сделаете лабораторные анализы, а также сможете пройти УЗИ, чтобы определить, на каком этапе беременности вы находитесь.
Медсестра или врач сообщат вам, если вам нужно что-то еще сделать, чтобы подготовиться к аборту.Они дадут вам письменные инструкции о том, как принимать таблетки. В процессе у вас будет доступ к заботливому профессионалу — вы получите номер, по которому вы сможете звонить круглосуточно и без выходных, если у вас возникнут какие-либо вопросы или проблемы.
После приема второго лекарства у вас будет сильное кровотечение и спазмы, поэтому планируйте это заранее, чтобы сделать процесс более комфортным. Вы можете быть дома или в любом удобном для вас месте. Вы также можете захотеть, чтобы с вами (или рядом) был кто-то, кому вы доверяете, которому вы можете позвонить за поддержкой, если вам что-то понадобится.
Запаситесь подушечками макси, едой, книгами, фильмами или чем угодно, чтобы скоротать время, а также грелкой от судорог. Убедитесь, что у вас есть обезболивающее, но не принимайте аспирин, потому что он может вызвать усиление кровотечения.
Что происходит во время медикаментозного аборта?
Процесс изготовления таблеток для прерывания беременности состоит из нескольких этапов и включает два разных лекарства.
Сначала вы принимаете таблетку мифепристон. Это лекарство останавливает рост беременности. Некоторые люди чувствуют тошноту или кровотечение после приема мифепристона, но это случается нечасто.Ваш врач или медсестра могут также прописать вам антибиотики, чтобы предотвратить инфекцию.
Второе лекарство называется мизопростол. Вы примете мизопростол сразу же или в течение 48 часов после приема первой таблетки — врач или медсестра сообщат вам, как и когда принимать. Это лекарство вызывает спазмы и кровотечение из матки.
У большинства людей спазмы и кровотечение обычно начинаются через 1–4 часа после приема мизопростола. Когда это происходит, можно увидеть большие сгустки крови (размером до лимона) или комки ткани.Это похоже на действительно тяжелые, спастические периоды, и процесс очень похож на ранний выкидыш. (Если у вас не будет кровотечения в течение 24 часов после приема второго лекарства, мизопростола, позвоните медсестре или врачу.)
Спазмы и кровотечение могут длиться несколько часов. Большинство людей заканчивают прохождение ткани беременности через 4-5 часов, но это может занять больше времени. Спазмы и кровотечение замедляются после того, как ткань беременной выходит наружу. Спазмы могут появляться и исчезать еще 1-2 дня.
Вы можете принять обезболивающее, например ибупрофен, примерно за 30 минут до приема второго лекарства, мизопростола, для облегчения судорог. Вы также можете принимать лекарство от тошноты, если его вам пропишет врач или медсестра. Не принимайте аспирин, потому что он может вызвать усиление кровотечения.
Кровотечение и кровянистые выделения в течение нескольких недель после аборта — это нормально. Вы можете использовать прокладки, тампоны или менструальную чашу — все, что вам удобнее. Но медсестра или врач могут порекомендовать вам использовать тампоны в первые несколько дней после аборта, чтобы вы могли отслеживать, сколько у вас кровотечений.
Последний шаг — это обращение к медсестре или врачу. Вы можете вернуться в поликлинику для проведения УЗИ или анализа крови. Или вы сделаете тест на беременность дома, а затем позвоните медсестре или врачу. Эти тесты позволят убедиться, что аборт сработал и вы здоровы.
В том маловероятном случае, если аборт не сработает и вы все еще беременны, ваш врач или медсестра обсудят с вами возможные варианты. Для завершения аборта вам может потребоваться еще одна доза лекарства или пройти процедуру в клинике.
Как вы себя чувствуете после медикаментозного аборта?
Для большинства людей медикаментозный аборт ощущается как преждевременный выкидыш. У вас может быть:
спазмы и боли в животе
очень сильное кровотечение с большими сгустками (если у вас не будет кровотечения в течение 24 часов после приема второго лекарства, мизопростола, позвоните медсестре или врачу)
расстройство желудка и рвота (Ваш врач или медсестра могут дать вам лекарство от тошноты.)
понос
головокружение
усталость
умеренная лихорадка (99-100 ° F) или озноб в день приема мизопростола (если у вас поднялась температура после дня приема таблеток мизопростола, немедленно позвоните своему врачу или в поликлинику).
Чтобы облегчить боль и сделать вас более комфортным, вы можете:
Принимайте обезболивающие, например ибупрофен (Адвил или Мотрин).Не принимайте аспирин, потому что он может усилить кровотечение.
Положите на живот грелку или грелку.
Примите душ.
Сядьте в унитаз.
Попросите кого-нибудь потереть вам спину.
Помогите нам стать лучше — чем эта информация может быть полезнее?
Как эта информация вам помогла?
Ты лучший! Спасибо за ваш отзыв.
Спасибо за ваш отзыв.
Psst! Я Ру.
Есть вопросы? Наш конво частный.
ТЕПЕРЬ ГОВОРИТЕPsst! Я Ру.
Есть вопросы? Наш конво частный.
ТЕПЕРЬ ГОВОРИТЕPsst! Я Ру.
Есть вопросы? Наш конво частный.
ТЕПЕРЬ ГОВОРИТЕНам не удалось получить доступ к вашему местоположению, выполните поиск местоположения.
Пожалуйста, заполните это поле.Услуга Все услуги Аборт Направление к специалистам по прерыванию беременности Контроль рождаемости COVID-19 вакцина ВИЧ услуги ЛГБТК-услуги Уход за мужским здоровьем Душевное здоровье Таблетка Morning-After (Экстренная контрацепция) Тестирование на беременность и услуги Первая помощь Тестирование на ЗППП, лечение и вакцины Уход за женским здоровьем
Фильтровать по Все Телездравоохранение Лично
Поиск
Или позвоните по телефону 1-800-230-7526
Где я могу получить таблетку для прерывания беременности и сколько она будет стоить?
Вы можете получить таблетку для прерывания беременности у врача, медсестры, в поликлинике или в центре планирования семьи.Вы можете получить таблетку для прерывания беременности бесплатно или по низкой цене.
Где я могу получить таблетки для прерывания беременности?
Вы можете сделать медикаментозный аборт (также известный как таблетка для прерывания беременности) во многих медицинских центрах планирования семьи. Наши заботливые врачи и медсестры являются экспертами в области безопасных абортов и беспристрастной поддержки на протяжении всего процесса. Даже если в вашем местном отделении службы планирования семьи не предоставляются таблетки для прерывания беременности, вы можете позвонить, чтобы узнать, где их можно получить в вашем районе.
При поиске места для прерывания беременности остерегайтесь «центров кризисной беременности». Эти поддельные клиники выглядят как медицинские центры, предлагающие аборты или другие варианты беременности, но на самом деле ими управляют люди, которые хотят напугать или пристыдить людей, чтобы они не сделали аборт.
В зависимости от того, где вы живете, могут быть возрастные ограничения или периоды ожидания для прерывания беременности. Вы можете спросить об этом, когда позвоните своему врачу или в медицинский центр.
Телемедицина для таблеток для прерывания беременности
Центры здравоохранения по программе «Планируемое отцовство» предлагают медикаментозный аборт (также известный как «таблетка для прерывания беременности») несколькими способами.В некоторых штатах мы можем предложить медикаментозный аборт с помощью телемедицины (также называемой телемедициной), когда пациент в одном месте встречается с поставщиком медицинских услуг в другом месте через частное и безопасное видеосвязь. Посмотрите это видео для получения дополнительной информации. В зависимости от штата некоторые пациенты могут получить таблетки для медикаментозного аборта, отправленные прямо к вам домой, без посещения медицинского центра.
Сколько стоит таблетка для прерывания беременности?
Стоимость медикаментозного аборта (таблетки для прерывания беременности) может варьироваться в зависимости от штата, в котором вы получаете медицинское обслуживание, и вашей медицинской страховки (частной или государственной).Ваш местный медицинский центр планирования семьи может предоставить вам дополнительную информацию о стоимости страхового покрытия аборта в вашем штате или других фондах, которые могут помочь вам оплатить аборт. Что нужно знать:
Специалисты Planned Parenthood работают, чтобы предоставить вам необходимые услуги, независимо от того, есть ли у вас страховка. Обратитесь в местный медицинский центр для получения дополнительной информации о расходах.
Ваш аборт может быть бесплатным или недорогим при наличии медицинской страховки.Некоторые планы страхования не покрывают аборты. Вы можете напрямую позвонить в свою страховую компанию, чтобы узнать их полисы.
Некоторые государственные планы медицинского страхования (например, Medicaid) в определенных штатах покрывают аборты, а другие — нет. Некоторые планы покрывают аборт только в определенных случаях.
Если вас беспокоит стоимость, позвоните в местный медицинский центр планирования семьи, чтобы узнать, как они могут предоставить вам медицинское обслуживание, которое вы можете себе позволить.
Примите участие в исследовании TelAbortion
Planned Parenthood заключила партнерские отношения с исследовательской организацией Gynuity Health Projects, чтобы изучить влияние TelAbortion.TelAbortion включает в себя все те же шаги и процедуры, что и медикаментозный аборт лично, но вам не нужно ехать в медицинский центр для прерывания беременности. Вместо этого поставщик услуг по прерыванию беременности проводит видео-оценку через частное и безопасное видеосвязь. Таблетки для прерывания беременности будут отправлены вам по почте.
Вы можете претендовать на участие в исследовательском исследовании TelAbortion, если живете в одном из штатов проекта Gynuity (округ Колумбия, Колорадо, Джорджия, Гавайи, Айова, Иллинойс, Орегон, Мэн, Нью-Мексико, Нью-Йорк, Массачусетс, Мэриленд, Миннесота, Монтана, Нью-Джерси, Невада, Вирджиния и Вашингтон), беременны и хотят сделать медикаментозный аборт.
Вам нужно будет пройти все необходимые анализы перед абортом, получить лекарства и принять первую таблетку для прерывания беременности до того, как наступит 70 дней (10 недель) беременности. Для оценки видео вам потребуется доступ к устройству с подключением к Интернету, веб-камерой и микрофоном.
Посетите веб-сайт Gynuity TelAbortion для получения более подробной информации.
Была ли эта страница полезной?Помогите нам стать лучше — чем эта информация может быть полезнее?
Как эта информация вам помогла?
Ты лучший! Спасибо за ваш отзыв.
Спасибо за ваш отзыв.
Psst! Я Ру.
Есть вопросы? Наш конво частный.
ТЕПЕРЬ ГОВОРИТЕPsst! Я Ру.
Есть вопросы? Наш конво частный.
ТЕПЕРЬ ГОВОРИТЕPsst! Я Ру.
Есть вопросы? Наш конво частный.
ТЕПЕРЬ ГОВОРИТЕНам не удалось получить доступ к вашему местоположению, выполните поиск местоположения.
Пожалуйста, заполните это поле.Услуга Все услуги Аборт Направление к специалистам по прерыванию беременности Контроль рождаемости COVID-19 вакцина ВИЧ услуги ЛГБТК-услуги Уход за мужским здоровьем Душевное здоровье Таблетка Morning-After (Экстренная контрацепция) Тестирование на беременность и услуги Первая помощь Тестирование на ЗППП, лечение и вакцины Уход за женским здоровьем
Фильтровать по Все Телездравоохранение Лично
Поиск
Или позвоните по телефону 1-800-230-7526
Безопасны ли таблетки для прерывания беременности?
Медикаментозный аборт очень безопасен.Серьезные проблемы возникают редко, но, как и при любых медицинских процедурах, могут быть некоторые риски.
Каковы возможные риски приема таблеток для прерывания беременности?
Медикаментозный аборт безопасно применяется в США более 20 лет. Серьезные осложнения действительно редки, но могут случиться. К ним относятся:
таблетки для прерывания беременности не работают и беременность не заканчивается
часть беременных тканей остается в матке
сгустков крови в матке
кровотечение слишком сильное или слишком продолжительное
заражение
аллергическая реакция на одно из лекарств
Эти проблемы встречаются нечасто.И если они действительно случаются, их обычно легко лечить с помощью лекарств или других методов лечения.
В очень редких случаях некоторые осложнения могут быть очень серьезными или даже опасными для жизни. Немедленно позвоните своему врачу или в поликлинику, если вы:
нет кровотечения в течение 24 часов после приема второго лекарства (мизопростол)
имеют сильное кровотечение из влагалища, которое пропускает более 2 подушечек макси в час в течение 2 или более часов подряд
проходят через большие сгустки (больше лимона) более 2 часов
испытывают боль в животе или спазмы, которые не проходят при приеме обезболивающих.
имеют лихорадку 100.4 или более через более 24 часов после приема мизопростола
имеют слабость, тошноту, рвоту и / или диарею, которые продолжаются более 24 часов после приема мизопростола
Вы должны почувствовать себя лучше на следующий день после аборта. Чувство тошноты, рвоты, диареи, боли в животе или повышение температуры в течение более 24 часов после приема мизопростола (второй набор таблеток) может быть признаком инфекции. Немедленно позвоните своему врачу или медсестре, если у вас есть какие-либо из этих симптомов.В самых редких случаях серьезные проблемы могут привести к смерти, но аборт, как правило, очень безопасен. На самом деле беременность и роды более опасны, чем большинство абортов.
Если у вас возникли осложнения во время медикаментозного аборта, вам, возможно, придется вернуться к врачу или в поликлинику. В том маловероятном случае, если вы все еще беременны, ваш врач или медсестра обсудят с вами возможные варианты. Возможно, вам понадобится еще одна доза лекарства или сделать аборт в клинике, чтобы прервать беременность.
Как и все лекарства, таблетки для прерывания беременности подходят не всем. Таблетки для прерывания беременности могут не подойти вам, если у вас есть определенные заболевания или вы принимаете определенные лекарства. Ваш врач или медсестра поговорят с вами и помогут решить, подходят ли вам таблетки для прерывания беременности.
Есть ли у таблетки для прерывания беременности долгосрочные побочные эффекты?
Таблетка для прерывания беременности действительно безопасна и эффективна. Это очень распространенный способ сделать аборт, и миллионы людей воспользовались им без всяких опасений.
Если нет редкого и серьезного осложнения, которое не лечится, нет никакого риска для ваших будущих беременностей или для вашего здоровья в целом. Аборт не увеличивает риск рака груди и не влияет на фертильность. Это не вызывает проблем для будущих беременностей, таких как врожденные дефекты, преждевременные роды или низкий вес при рождении, внематочная беременность, выкидыш или младенческая смерть.
Серьезные долговременные эмоциональные проблемы после аборта случаются редко, и примерно так же редко, как и после родов.Они чаще возникают у людей, которым необходимо прервать беременность по состоянию здоровья, у людей, у которых нет поддержки в их решении сделать аборт, или у людей, у которых в анамнезе есть проблемы с психическим здоровьем. Большинство людей чувствуют облегчение после аборта.
Существует множество мифов о последствиях аборта. Ваша медсестра или врач может предоставить вам точную информацию о побочных эффектах таблеток для прерывания беременности или любых других проблемах, которые могут у вас возникнуть.
Была ли эта страница полезной?Помогите нам стать лучше — чем эта информация может быть полезнее?
Как эта информация вам помогла?
Ты лучший! Спасибо за ваш отзыв.
Спасибо за ваш отзыв.
кинетики сывороточного ХГЧ и прогестерона в ответ на пероральное и вагинальное введение мизопростола при медикаментозном прерывании беременности на ранних сроках | Репродукция человека
Абстрактные
СПРАВОЧНАЯ ИНФОРМАЦИЯ: Мизопростол широко используется в сочетании с мифепристоном для прерывания беременности по медицинским показаниям. Мы изучали эндокринные параметры функции трофобластов во время медикаментозного прерывания беременности на ранних сроках с использованием мифепристона в сочетании с пероральным или вагинальным мизопростолом.Также изучался эффект длительного приема мизопростола. Методы. Тридцать четыре женщины с просьбой о прерывании беременности и с аменореей ≤63 дня получали 200 мг мифепристона в день 0 с последующим пероральным ( n = 13) или вагинальным ( n = 21) введением. 0,8 мг мизопростола на 2-й день. В 23 случаях введение мизопростола было продолжено перорально в течение дополнительных 7 дней. Образцы сыворотки, собранные в течение 14 дней после начала лечения, анализировали на ХГЧ, прогестерон и мифепристон.РЕЗУЛЬТАТЫ: концентрации ХГЧ и прогестерона продолжали расти до 2-го дня. После приема мизопростола уровни ХГЧ и прогестерона снизились на 70,5 ± 8,8% и 61,3 ± 16,3% (среднее ± стандартное отклонение) соответственно за 24 часа. Процентное снижение ХГЧ обратно коррелировало ( P <0,05) со временем, необходимым для прерывания беременности. Пиковый уровень мифепристона, измеренный на 2-й день, не коррелировал со снижением сывороточного ХГЧ или прогестерона. Кинетика ХГЧ, прогестерона и мифепристона была сходной в разных группах лечения.ВЫВОДЫ. Способ и продолжительность приема мизопростола не влияют на кинетику сывороточного ХГЧ или прогестерона во время медикаментозного прерывания беременности на ранних сроках.
Введение
Медикаментозное прерывание беременности с использованием комбинации антипрогестинового мифепристона и простагландина E 1 аналог мизопростола является широко используемой альтернативой хирургической эвакуации матки на ранних сроках беременности. Изучены как пероральные, так и вагинальные схемы приема мизопростола.Однако эффективность перорального мизопростола снижается, если срок беременности превышает 7 недель (Всемирная организация здравоохранения, 2000). После предварительной обработки мифепристоном вагинальное введение мизопростола привело к 95% случаев полного аборта, тогда как после перорального приема мизопростола этот показатель составил 87% (El-Refaey et al ., 1995). Абсорбция мизопростола происходит быстрее после перорального приема, однако более устойчивые уровни в сыворотке крови наблюдаются после вагинального введения (Tang et al ., 2002).По сравнению с пероральным приемом мизопростол вагинально обеспечивает более длительную и более регулярную сократительную способность матки (Gemzell-Danielsson et al ., 1999), что может объяснить лучшую клиническую эффективность мизопростола, вводимого вагинально (El-Refaey et al ). ., 1995).
Кинетика гормонов ХГЧ и прогестерона, производных трофобласта, оценивалась ранее, когда мифепристон использовался отдельно для прерывания беременности у человека на ранних сроках (Somell et al ., 1990). Исследования, оценивающие кинетику этих гормонов после комбинации мифепристона и гемепроста, другого аналога простагландина E 1 , показали, что значения ХГЧ остаются высокими до аборта, а уровень прогестерона снижается на 4 часа после приема гемепроста (Howell et al ., 1989; Оладжиде и др. ., 1989). Когда мифепристон использовался отдельно для прерывания беременности, единственным предиктором успеха был низкий уровень ХГЧ в сыворотке до лечения (Birgerson and Odlind, 1988).
Чтобы сравнить эффективность перорального и вагинального введения мизопростола после однократного перорального приема 200 мг мифепристона и выяснить, можно ли повысить эффективность, продолжая пероральный прием мизопростола в течение недели, Всемирная организация здравоохранения (ВОЗ) организовал двойное слепое рандомизированное многоцентровое исследование (Всемирная организация здравоохранения, рукопись представлена). Учитывая различные модели сократительной способности матки после перорального и вагинального приема мизопростола (Gemzell-Danielsson et al ., 1999), мы хотели вместе с исследованием ВОЗ по медикаментозному аборту оценить, связан ли способ введения мизопростола с сывороточной кинетикой гормонов трофобласта, а именно ХГЧ и прогестерона. Кроме того, мы стремились установить взаимосвязь между этими гормонами и уровнями мифепристона.
Материалы и методы
Субъектов
Это исследование было основано на 34 здоровых женщинах, которые обратились с просьбой о медицинском прерывании нежелательной беременности продолжительностью <9 недель (или ≤63 дней аменореи).Женщины приняли участие в многоцентровом исследовании ВОЗ по медицинскому прерыванию беременности (Всемирная организация здравоохранения, рукопись представлена). Используемые критерии отбора были такими же, как использованные и описанные в предыдущем исследовании ВОЗ (World Health Organization, 2000). В исследование были включены только женщины с одиночной внутриутробной беременностью, подтвержденной ультразвуковым исследованием.
Исследование было проведено в отделении акушерства и гинекологии Центральной больницы Хельсинкского университета, Хельсинки, Финляндия, и одобрено местным комитетом по этике.Перед участием в исследовании испытуемые дали свое информированное согласие.
В исследовании эффективности женщины были рандомизированы в одну из трех групп лечения. Схемы лечения представлены в таблице I. Всем женщинам давали перорально 200 мг мифепристона в день 0 исследования. На 2 день исследования (36–48 ч после приема мифепристона) группа А (пероральная группа) получала 0,8 мг мизопростола перорально; группы B (вагинальный плюс постоянный прием мизопростола перорально) и C (группа только вагинальный) получили 0.8 мг мизопростола вагинально. После приема мизопростола женщины наблюдались в течение 3 часов в больнице № . Их попросили отметить время изгнания плодного материала.
Группа A и группа B продолжали принимать 0,4 мг мизопростола перорально два раза в день в течение 7 дней, начиная с 3 дня исследования.
Субъекты вернулись на контрольные визиты через 2 и 6 недель после начала лечения. Окончательная оценка полного аборта проводилась на 6-недельном визите.
Последовательные пробы крови отбирались пять раз; образец I непосредственно перед введением мифепристона, образец II на 2-й день до введения мизопростола, образец III на 2-й день, ~ 3 часа после приема мизопростола, образец IV на 3-й день, перед первым введением мизопростола на дому и образец V на 14 день. Точное время прерывания беременности отмечено у 27 из 34 женщин.
Гормоны
Концентрации ХГЧ и прогестерона в сыворотке измеряли в двух экземплярах с помощью флюороиммуноанализа с временным разрешением, используя коммерческие наборы (DELFIA), производимые Wallac Finland Oy, Турку, Финляндия.По данным производителя, предел обнаружения анализа ХГЧ составил 0,5 МЕ / л, а анализа прогестерона — 0,8 нмоль / л. Расчетный коэффициент вариации (CV) для ХГЧ составил 2,0–4,1%, а для прогестерона — 3,3–7,3%. CV между анализами для ХГЧ и прогестерона составляли 3,2–4,6 и 2,7–10,1% соответственно.
Мифепристон в сыворотке количественно определяли с помощью специального радиоиммуноанализа после хроматографии на колонке Chromosorb (W-NAW-60–80 Mesh; Sigma St. Louis, Миссури, США), как описано ранее (Heikinheimo et al ., 1986). Специфический индикатор, [6,7– 3 H] -RU 486, был предоставлен Исследовательским центром Русселя-Уклафа (Роменвиль, Франция), а моноклональное антитело против мифепристона было подарком доктора Фортуны Кохена (Институт Вейцмана, США). Израиль). Предел количественного определения анализа, 0,36 пмоль / л, представляет собой самую низкую концентрацию на стандартной кривой, которая может быть измерена с приемлемой точностью (т.е. CV внутри анализа ≤ 20%). CV внутри анализа (8,4%) был рассчитан из дублирующих образцов в одном репрезентативном анализе.CV между анализами рассчитывали на основе пулов сыворотки в каждом анализе и варьировали в пределах 10,3–13,6%.
Начальные индивидуальные значения t 1/2 сывороточного ХГЧ были рассчитаны путем оценки данных сывороточной концентрации в зависимости от времени, измеренных на 2 и 3 дни в линейной регрессии и деления натурального логарифма двух на наклон.
Статистические методы
Различия между группами оценивали с помощью дисперсионного анализа. При необходимости использовался тест Краскела-Уоллиса.Дисперсионный анализ для повторных измерений использовался для анализа продольных изменений концентраций. Корреляции между переменными оценивались путем расчета коэффициента корреляции Спирмена. Эти анализы были выполнены с использованием SPSS 8.0 для Windows. Статистическая значимость была определена как P <0,05.
Результаты
Характеристики женщин и время до аборта показаны в Таблице II. Средняя продолжительность беременности варьировала от 7.От 0 до 7,4 недель в группах лечения, разница между группами не была статистически значимой. Кроме того, уровни ХГЧ и прогестерона, измеренные в день 0, статистически не различались в трех группах лечения. Среднее время до аборта после приема мизопростола варьировало от 210 (группа A) до 380 минут (группа C), при этом разница между группами не была значимой.
Выскабливание было выполнено в одном случае в группе А при контрольном визите через 6 недель из-за продолжающегося кровотечения и остатков в матке.Субъект был включен в анализы. Все остальные пациенты сделали полный аборт.
Концентрация ХГЧ продолжала увеличиваться после введения мифепристона до дня 2, до введения мизопростола (рис. 1). После приема мизопростола через 3 часа было отмечено явное снижение уровня ХГЧ на 18,8 ± 2,0% (среднее ± стандартное отклонение) ( P ≤ 0,001). На следующий день уровень ХГЧ упал на 70,5 ± 8,8% ( P ≤ 0,001) от пикового уровня. Тенденция изменения была сходной во всех группах лечения, и не было никакой разницы в процентном снижении уровней ХГЧ при сравнении групп, получавших пероральный и вагинальный мизопростол.Кроме того, процентное снижение уровня ХГЧ в течение первых 3 или 24 часов не коррелировало с пиковым уровнем ХГЧ, измеренным до введения мизопростола. Период полувыведения сывороточного ХГЧ варьировал от 13,8 ± 3,0 до 16,3 ± 6,2 часа (среднее ± стандартное отклонение) в различных группах лечения, при этом среднее значение (± стандартное отклонение) составляло 14,6 (± 4,1) часа.
Корреляция между пиковой концентрацией ХГЧ и временем до аборта (наблюдаемое изгнание материала беременности) была слабой и статистически недостоверной ( r = 0.25, P = 0,22). Однако процентное снижение уровня ХГЧ в сыворотке со 2-го дня (до приема мизопростола) до 3-го дня отрицательно коррелировало со временем, необходимым для прерывания беременности ( r = –0,39, P <0,05).
К 14 дню концентрации ХГЧ в сыворотке снизились на 99,4 ± 1,0% (среднее ± стандартное отклонение). У трех субъектов были концентрации выше 1000 МЕ / л, у одного из них был единственный отказ (ХГЧ 3560 МЕ / л) в нашем исследовании. У одной пациентки было еще более высокое значение ХГЧ, 4210 МЕ / л, но было обнаружено, что к 6-недельному контрольному визиту у нее был полный аборт.
Концентрация прогестерона продолжала увеличиваться после введения мифепристона до 2-го дня (рис. 2). Через три часа после приема мизопростола было отмечено явное снижение уровня прогестерона в сыворотке на 31,8 ± 10,8% (среднее ± стандартное отклонение) ( P <0,001). На следующий день концентрация прогестерона упала на 61,3 ± 16,3% (среднее ± стандартное отклонение) ( P <0,001) от пикового уровня. Тенденция к снижению была одинаковой во всех группах лечения. Процентное снижение концентрации прогестерона в течение первых 3 или 24 часов не коррелировало с пиковыми уровнями прогестерона, измеренными на 2 день.
Снижение уровня прогестерона в сыворотке со 2-го дня (до приема мизопростола) до 3-го дня достоверно коррелировало со снижением сывороточного уровня ХГЧ ( r = 0,34, P <0,05). Не было корреляции между процентным снижением уровня прогестерона в сыворотке со 2-го дня (до приема мизопростола) до 3-го дня и временем, необходимым для прерывания беременности ( r = 0,13, P = 0,52).
Уровни мифепристона в сыворотке снизились на 47,6 ± 20,2% (среднее ± стандартное отклонение) со 2 по 3 день (рис. 3).Слабая отрицательная корреляция, хотя и не статистически значимая, была обнаружена между концентрациями мифепристона в сыворотке, измеренными до введения мизопростола на 2-й день, и временем, необходимым для прерывания беременности ( r = –0,35, P = 0,1).
Точно так же не было выявлено корреляций, когда пиковые уровни мифепристона, измеренные на 2-й день, коррелировали со снижением сывороточного ХГЧ ( r = 0,03, P = 0,89) или прогестерона ( r = 0,09, P ). = 0.61) с 0 по 2 день (значение через 3 ч после введения мизопростола).
Обсуждение
Равная клиническая эффективность мифепристона в дозе 200 мг по сравнению с более высокими дозами была показана в нескольких рандомизированных клинических исследованиях (World Health Organization, 1993, 2000). Однако оптимальная схема приема мизопростола менее ясна, поэтому использовались как пероральные, так и вагинальные схемы (Ashok et al ., 1998, Spitz et al ., 1998).В рандомизированном исследовании (El-Rafaey et al ., 1995) клиническая эффективность мизопростола, вводимого вагинально, была лучше, чем перорального приема.
Есть также предположение, что клиническая эффективность может быть улучшена за счет увеличения продолжительности лечения мизопростолом (Tang et al ., 1998). Учитывая высокую эффективность комбинации мифепристон-мизопростол, очевидно, что возможное улучшение клинической эффективности может быть продемонстрировано только в крупномасштабных рандомизированных клинических испытаниях.Наряду с исследованием ВОЗ, оценивающим клинический эффект способа и продолжительности введения мизопростола (Всемирная организация здравоохранения, рукопись представлена), мы оценивали кинетику ХГЧ и прогестерона в ответ на мифепристон в комбинации с пероральным и вагинальным мизопростолом. Мы предположили, что потенциально разная кинетика гормонов, производных трофобласта, может помочь в оптимизации режимов, используемых при медикаментозном прерывании беременности.
Ашок и др. . обобщили обширный опыт из одного центра, где комбинация 200 мг мифепристона с последующим введением 0.Использовалось 8 мг мизопростола вагинально: в их исследовании средний интервал между индукцией и прерыванием беременности составлял 255 минут (Ashok et al ., 1998). В настоящем исследовании среднее время до аборта варьировалось от 210 до 380 минут в разных группах (таблица II). Таким образом, клинические курсы хорошо соответствовали опыту, о котором сообщалось ранее.
Уровни ХГЧ в сыворотке соответствовали ожиданиям и соответствовали хорошо изученному клиническому течению прерывания беременности по медицинским показаниям (Spitz et al ., 1998). Несмотря на то, что после введения мифепристона, сывороточные концентрации ХГЧ продолжали расти вплоть до 2-го дня (рис. 1), этот результат согласуется с предыдущими исследованиями, в которых использовался мифепристон в комбинации с гемепростом (Olajide et al ., 1989). Однако после введения мизопростола уровни ХГЧ быстро снизились, и через 24 часа было очевидно снижение на 70,5 ± 8,8% (среднее ± стандартное отклонение). Снижение ХГЧ было одинаковым во всех трех группах. Когда группы B и C, которые получали аналогичный вагинальный мизопростол до 3-го дня, были объединены, не было выявлено различий между группами, получавшими мизопростол перорально или вагинально.Таким образом, кажется, что начальная доза мизопростола запускает каскад, ведущий к прогрессивному падению ХГЧ. Уровни ХГЧ снизились на 99,4 ± 1,0% (среднее ± стандартное отклонение) через 14 дней после введения мифепристона. Снижение было одинаковым во всех группах; таким образом, длительное введение мизопростола не принесло пользы, судя по кинетике ХГЧ.
Более ранние данные in vitro (Das et al ., 1987) показали, что трофобласт сам может быть мишенью ингибирующего действия мифепристона на плацентарный ХГЧ и секрецию прогестерона.Однако повышение сывороточных уровней ХГЧ до 2 дней после введения мифепристона предполагает, что трофобласт не является мишенью действия мифепристона in vivo . Хотя нельзя исключить прямое действие мизопростола на функцию трофобласта, похоже, что падение уровня ХГЧ после введения мизопростола, скорее всего, будет вторичным по отношению к отслойке плаценты из-за быстрого усиления сократимости матки (Swahn and Быгдеман, 1988).
После хирургического прерывания беременности начальный период полувыведения ХГЧ составляет ~ 15 часов (Lähteenmäki, 1978).В настоящем исследовании начальное t 1/2 сывороточного ХГЧ было одинаковым в разных группах лечения, среднее значение составляло 14,6 часа. Таким образом, с точки зрения первоначального удаления ХГЧ медикаментозное прерывание беременности не отличается от хирургической эвакуации матки.
Абсолютный уровень ХГЧ все еще превышал 1000 МЕ / л в трех случаях на 14-й день. В двух случаях было установлено, что прерывание беременности было успешным, тогда как в одном из них в конечном итоге удалось справиться хирургическим путем из-за продолжающегося вагинального кровотечения.Снижение уровня ХГЧ в сыворотке недавно было предложено как средство контроля клинического исхода медикаментозного аборта (Walker et al ., 2001). Однако на основе этих трех случаев возможен полный клинический аборт, несмотря на повышенный уровень ХГЧ, наблюдаемый через 2 недели после лечения мифепристоном и мизопростолом.
Кинетика сывороточного прогестерона была аналогична кинетике ХГЧ, а уровни прогестерона сначала снизились после приема мизопростола (рис. 2).Влияние мизопростола на прогестерон сыворотки может быть связано с его действием на функцию трофобласта и / или желтого тела. Лютеолитические эффекты простагландинов хорошо известны (Ottander et al ., 1999). Однако снижение уровня прогестерона в течение первых 3 или 24 часов было одинаковым независимо от пикового уровня прогестерона, измеренного на 2-й день. Кроме того, снижение концентрации прогестерона со 2-го по 3-й день значительно коррелировало со снижением уровня ХГЧ в сыворотке. .Поэтому мы предполагаем, что снижение концентрации прогестерона связано с отслоением плаценты и падением уровня ХГЧ.
Когда мифепристон используется отдельно для прерывания беременности, единственным предиктором успешного результата является низкий уровень сывороточного ХГЧ до лечения (Birgerson and Odlind, 1988). В настоящем исследовании с ограниченным числом субъектов и высокой эффективностью комбинации мифепристон-мизопростол корреляция между уровнем ХГЧ до лечения и конечным результатом не могла быть оценена.Точно так же была обнаружена незначительная корреляция между пиковым уровнем ХГЧ и временем, затраченным на прерывание. Тем не менее, процентное снижение уровня ХГЧ в сыворотке со 2 по 3 день было обратно пропорционально и достоверно ( r = –0,39, P <0,05) коррелировало со временем, необходимым для прерывания беременности. Не было обнаружено корреляции между процентным снижением уровня прогестерона в сыворотке и временем, необходимым для прерывания беременности.
Кинетика сывороточного мифепристона вела себя так, как ожидалось, на основании наших предыдущих исследований (Heikinheimo et al ., 1990). Согласно его t 1/2 , составляющему ~ 25 ч, уровни мифепристона в сыворотке снизились примерно до половины между 2 и 3 днями. Как и ожидалось, уровни мифепристона в сыворотке были одинаковыми в разных группах лечения. Когда пиковый уровень мифепристона, измеренный на 2-й день, коррелировал со временем, необходимым для прерывания беременности, выявлялась только слабая, статистически незначимая корреляция. Когда была предпринята попытка сопоставить пиковые уровни мифепристона, измеренные на 2-й день, со снижением сывороточных концентраций ХГЧ и прогестерона, корреляции не было обнаружено.
В заключение следует отметить, что изгнание плодного материала после введения мизопростола в ходе медицинского прерывания беременности приводит к быстрому снижению сывороточных уровней ХГЧ и прогестерона. Снижение уровня ХГЧ в сыворотке обратно коррелировало со временем, необходимым для прерывания беременности. Снижение концентраций ХГЧ и прогестерона было одинаковым после перорального и вагинального введения мизопростола. Кроме того, длительный пероральный прием мизопростола не усиливал исчезновение ХГЧ или прогестерона.Таким образом, в настоящем исследовании ранее показанное усиление сократительной способности матки (Gemzell-Danielsson et al ., 1999) и клиническая эффективность, связанная с вагинальным введением мизопростола (El-Refaey et al ., 1995), не нашли отражения в результатах исследования. сывороточная кинетика ХГЧ или прогестерона.
| . | Группа А . | Группа B . | Группа C . |
|---|---|---|---|
| День 0 | Мифепристон пероральный 200 мг | Мифепристон пероральный 200 мг | Мифепристон пероральный 200 мг |
| День 2 90bo759 | Мизопростол пероральный 0,8 мг мизопростол 75 место 8 мг и вагинальный | Вагинальный мизопростол 0,8 мг и плацебо перорально | |
| дни 3–9 | Мизопростол перорально 0,4 мг два раза в день | Мизопростол перорально 0,4 мг два раза в день | Плацебо перорально два раза в день |
| . | Группа А . | Группа B . | Группа C . |
|---|---|---|---|
| День 0 | Мифепристон пероральный 200 мг | Мифепристон пероральный 200 мг | Мифепристон пероральный 200 мг |
| День 2 | Мизопростол пероральный 0.8 мг и вагинальное плацебо | Мизопростол вагинальный 0,8 мг и плацебо перорально | Мизопростол вагинальный 0,8 мг и плацебо перорально |
| дни 3–9 | Мизопростол перорально 0,4 мг два раза в день | Мизопростол пероральный два раза в день | Мизопростол перорально 0,4 мг плацебо два раза в день |
| . | Группа А . | Группа B . | Группа C . |
|---|---|---|---|
| День 0 | Мифепристон пероральный 200 мг | Мифепристон пероральный 200 мг | Мифепристон пероральный 200 мг |
| День 2 90bo759 | Мизопростол пероральный 0,8 мг мизопростол 75 место 8 мг и вагинальный | Вагинальный мизопростол 0,8 мг и плацебо перорально | |
| 3–9 дни | Мизопростол перорально 0,4 мг два раза в день | Мизопростол перорально 0,4 мг два раза в день | Плацебо перорально два раза в день |
Характеристика субъектов
| . | Группа А . | Группа B . | Группа C . |
|---|---|---|---|
| . | ( n = 13) . | ( n = 10) . | ( n = 11) . |
| Возраст, лет (среднее ± стандартное отклонение) | 31.5 ± 5,4 | 27,5 ± 6,4 | 31,9 ± 6,7 |
| ИМТ, кг / м 2 (среднее ± стандартное отклонение) | 22,8 ± 3,6 | 23,2 ± 3,0 | 22,5 ± 4,3 |
| Продолжительность беременности, недель, (дни аменореи) | |||
| Количество пациенток | |||
| <7 недель | дней аменореи | 0 | |
| 7 недель (50–56 дней аменореи) | 7 | 4 | 6 |
| 8 недель (57–63 дня аменореи) | 3 | 5 | |
| Время до прерывания, мин [медиана, (среднее ± SEM)] | 210, (280 ± 59) | 218, (304 ± 70) | 380, (971 ± 510) |
| Количество пациентов | 11 | 8 | 8 |
| ХГЧ перед лечением, МЕ / л (среднее ± SEM) | 64975 ± 8747 | 83105 ± 12662 | 67886 ± 8592 |
| Пре-НМ прогестерон (среднее ± стандартная ошибка среднего) | 69.5 ± 4,6 | 71,6 ± 7,3 | 58,9 ± 6,4 |
| . | Группа А . | Группа B . | Группа C . |
|---|---|---|---|
| . | ( n = 13) . | ( n = 10) . | ( n = 11) . |
| Возраст, лет (среднее ± стандартное отклонение) | 31.5 ± 5,4 | 27,5 ± 6,4 | 31,9 ± 6,7 |
| ИМТ, кг / м 2 (среднее ± стандартное отклонение) | 22,8 ± 3,6 | 23,2 ± 3,0 | 22,5 ± 4,3 |
| Продолжительность беременности, недель, (дни аменореи) | |||
| Количество пациенток | |||
| <7 недель | дней аменореи | 0 | |
| 7 недель (50–56 дней аменореи) | 7 | 4 | 6 |
| 8 недель (57–63 дня аменореи) | 3 | 5 | |
| Время до прерывания, мин [медиана, (среднее ± SEM)] | 210, (280 ± 59) | 218, (304 ± 70) | 380, (971 ± 510) |
| Количество пациентов | 11 | 8 | 8 |
| ХГЧ перед лечением, МЕ / л (среднее ± SEM) | 64975 ± 8747 | 83105 ± 12662 | 67886 ± 8592 |
| Пре-НМ прогестерон (среднее ± стандартная ошибка среднего) | 69.5 ± 4,6 | 71,6 ± 7,3 | 58,9 ± 6,4 |
Характеристика субъектов
| . | Группа А . | Группа B . | Группа C . | ||
|---|---|---|---|---|---|
| . | ( n = 13) . | ( n = 10) . | ( n = 11) . | ||
| Возраст, лет (среднее ± стандартное отклонение) | 31,5 ± 5,4 | 27,5 ± 6,4 | 31,9 ± 6,7 | ||
| ИМТ, кг / м 2 (среднее ± стандартное отклонение) | 22,8 ± 3,6 | 23,2 ± 3,0 | 22,5 ± 4,3 | ||
| Срок беременности, нед, (дни аменореи) | |||||
| Количество пациентов | 9075 9075 7 недель (≤49 дней аменореи) | 3 | 1 | 0 | |
| 7 недель (50–56 дней аменореи) | 7 | 4 | 6 | ||
| 6 | (57–63 дня аменореи) | 3 | 5 | 5 | |
| Время прерывания, мин [медиана, (среднее ± SEM)] | 210, (280 ± 59) | 218, (304 ± 70) | 380, (971 ± 510) | ||
| Количество пациентов | 11 | 8 | 8 | ||
| ХГЧ до лечения, МЕ / л (среднее ± SEM) | 64975 ± 8747 | 83105 ± 1266 67886 ± 8592 | |||
| Прогестерон перед лечением, нмоль / л (среднее ± SEM) | 69.5 ± 4,6 | 71,6 ± 7,3 | 58,9 ± 6,4 |
| . | Группа А . | Группа B . | Группа C . |
|---|---|---|---|
| . | ( n = 13) . | ( n = 10) . | ( n = 11) . |
| Возраст, лет (среднее ± стандартное отклонение) | 31.5 ± 5,4 | 27,5 ± 6,4 | 31,9 ± 6,7 |
| ИМТ, кг / м 2 (среднее ± стандартное отклонение) | 22,8 ± 3,6 | 23,2 ± 3,0 | 22,5 ± 4,3 |
| Продолжительность беременности, недель, (дни аменореи) | |||
| Количество пациенток | |||
| <7 недель | дней аменореи | 0 | |
| 7 недель (50–56 дней аменореи) | 7 | 4 | 6 |
| 8 недель (57–63 дня аменореи) | 3 | 5 | |
| Время до прерывания, мин [медиана, (среднее ± SEM)] | 210, (280 ± 59) | 218, (304 ± 70) | 380, (971 ± 510) |
| Количество пациентов | 11 | 8 | 8 |
| ХГЧ перед лечением, МЕ / л (среднее ± SEM) | 64975 ± 8747 | 83105 ± 12662 | 67886 ± 8592 |
| Пре-НМ прогестерон (среднее ± стандартная ошибка среднего) | 69.5 ± 4,6 | 71,6 ± 7,3 | 58,9 ± 6,4 |
Рисунок 1.
Уровни ХГЧ в сыворотке (среднее ± стандартная ошибка среднего) в трех группах лечения. Снижение концентрации ХГЧ в сыворотке крови было одинаковым во всех трех группах лечения, независимо от пути или продолжительности введения мизопростола.
Рис. 1.
Уровни ХГЧ в сыворотке (среднее ± SEM) в трех группах лечения. Снижение концентрации ХГЧ в сыворотке крови было одинаковым во всех трех группах лечения, независимо от пути или продолжительности введения мизопростола.
Рис. 2.
Уровни прогестерона в сыворотке (среднее ± SEM) в трех группах лечения. Как и в случае с ХГЧ, снижение сывороточного прогестерона было одинаковым во всех трех группах лечения, независимо от пути или продолжительности введения мизопростола.
Рис. 2.
Уровни прогестерона в сыворотке (среднее ± SEM) в трех группах лечения. Как и в случае с ХГЧ, снижение сывороточного прогестерона было одинаковым во всех трех группах лечения, независимо от пути или продолжительности введения мизопростола.
Рисунок 3.
Уровни мифепристона в сыворотке крови (среднее ± стандартная ошибка среднего).
Рис. 3.
Уровни мифепристона в сыворотке (среднее ± стандартная ошибка среднего).
Мы хотим поблагодарить г-жу Пиркко Тимонен за ее профессиональное отношение к участникам и г-жу Марьятту Тевилин за ее экспертную лабораторную работу. Благодарим за финансовую поддержку Совета по народонаселению (Нью-Йорк, штат Нью-Йорк, США) и исследовательских фондов Центральной больницы Хельсинкского университета.Д-р Хейкинхеймо является стипендиатом клинической стипендии Финского медицинского фонда. Содержание настоящей рукописи не обязательно отражает политику любого из источников финансирования.
Список литературы
Ашок, П.В., Пенни, Г.К., Флетт, Г.М.М. и Темплтон, А. (
1998
) Эффективный режим для раннего медикаментозного аборта: отчет о 2000 последовательных случаях.Hum. Репродукция.
,13
,2962
–2965.Бирджерсон, Л.и Odlind, V. (
1988
) Антипрогестативный агент RU 486 в качестве абортивного средства на ранних сроках беременности человека: сравнение трех режимов дозирования.Контрацепция
,38
,391
–400.Дас, К. и Кэтт, К.Дж. (
1987
) Эффекты антагониста прогестерона RU 486 на фертильность включают прямое ингибирование секреции плацентарного гормона.Ланцет
,ii
,599
–601.Эль-Рефей, Х., Раджасекар, Д., Абдалла, М., Колдер, Л. и Темплтон, А. (
1995
) Индукция аборта мифепристоном (RU 486) и пероральным или вагинальным мизопростолом.N. Engl. J. Med.
,332
,983
–987.Gemzell-Danielsson, K., Marions, L., Rodriguez, A., Spur, B.W., Wong, K. и Bygdeman, M. (
1999
) Сравнение перорального и вагинального введения мизопростола в отношении сократимости матки.Акушерство. Гинеколь.
,93
,275
–280.Heikinheimo, O., Tevilin, M., Shoupe, D., Croxatto, H. and Lähteenmäki, P. (
1986
) Количественное определение RU 486 в плазме человека с помощью ВЭЖХ и РИА после колоночной хроматографии.Контрацепция
,34
,613
–624.Heikinheimo, O., Ylikorkala, O., Turpeinen, U. and Lähteenmäki, P. (
1990
) Фармакокинетика антипрогестерона RU 486: Нет корреляции с клинической эффективностью RU 486.Acta Endocrinologica
,123
,298
–304.Howell, RJS, Olajide, F., Teisner, B., Grudzinskas, G. и Chard, T. (
1989
) Уровни плацентарного протеина 14 и прогестерона в крови после мифепристона (RU 38486) и гемепроста для прекращения первого триместр беременности.Fertil. Стерил.
,52
,66
–68.Lähteenmäki, P. (
1978
) Исчезновение ХГЧ и восстановление функции гипофиза после аборта.Clin. Эндокринол.
,9
,101
–112.Olajide, F., Howell, R.J.S., Wass, J.A.H., Holly, J.M.P., Bohn, H., Grudzinskas, J.A.H., Chapman, M.G. и Chard, T. (
1989
) Уровни циркуляции плацентарного протеина 12 и хорионического гонадотропина в соответствии с RU 38486 и гемепростом для прерывания беременности в первом триместре.Hum. Репродукция.
,4
,337
–349.Ottander, U., Leung, C.H. и Olofsson, J.I. (
1999
) Функциональные доказательства различных механизмов активации рецепторов лютеотрофных и лютеолитических событий в желтом теле человека.Мол. Гм. Репродукция.
,5
,391
–395.Somell, C., Ölund, A., Carlström, K. и Kindahl, H. (
1990
) Репродуктивные гормоны во время прерывания беременности на ранних сроках с помощью мифепристона.Gynecol. Акушерство. Вкладывать деньги.
,30
,224
–227.Spitz, I.M., Bardin, C.W., Benton, L. и Robbins, A. (
1998
) Прерывание беременности мифепристоном и мизопростолом на ранних сроках в США.Н.Англ. J. Med.
,338
,1241
–1247.Swahn, M.L. и Bygdeman, M. (
1988
). Влияние антипрогестина RU 486 на сократимость матки и чувствительность к простагландину и окситоцину.руб. J. Obstet. Gynaecol.
,95
,126
–134.Тан О.Т., Гао П.П., Ченг Л., Ли С. и Хо П.С. (
1998
) Пилотное исследование по применению двухнедельного курса перорального приема мизопростола у пациенток после прерывания беременности с помощью мифепристона и мизопростола.Контрацепция
,57
,89
–91.Тан, О.Т., Шеер, Х., Сейберт, Х.В., Ли, С.В.Х. и Хо П. (
2002
) Фармакокинетика различных способов введения мизопростола.Hum. Репродукция.
17
,332
–336.Уокер, К., Шафф, Э., Филдинг, С. и Фуллер, Л. (
2001
) Мониторинг уровня хорионического гонадотропина в сыворотке крови после аборта мифепристоном.Контрацепция
,64
,271
–273.Целевая группа Всемирной организации здравоохранения по постовуляторным методам регулирования фертильности (
1993
) Прерывание беременности сниженными дозами мифепристона.руб. Med. J.
,307
,532
–537.Целевая группа Всемирной организации здравоохранения по постовуляторным методам регулирования фертильности (
2000
) Сравнение двух доз мифепристона в комбинации с мизопростолом для раннего медикаментозного аборта: рандомизированное исследование.руб.J. Obstet. Gynaecol.
,107
,524
–530.© Европейское общество репродукции человека и эмбриологии
.


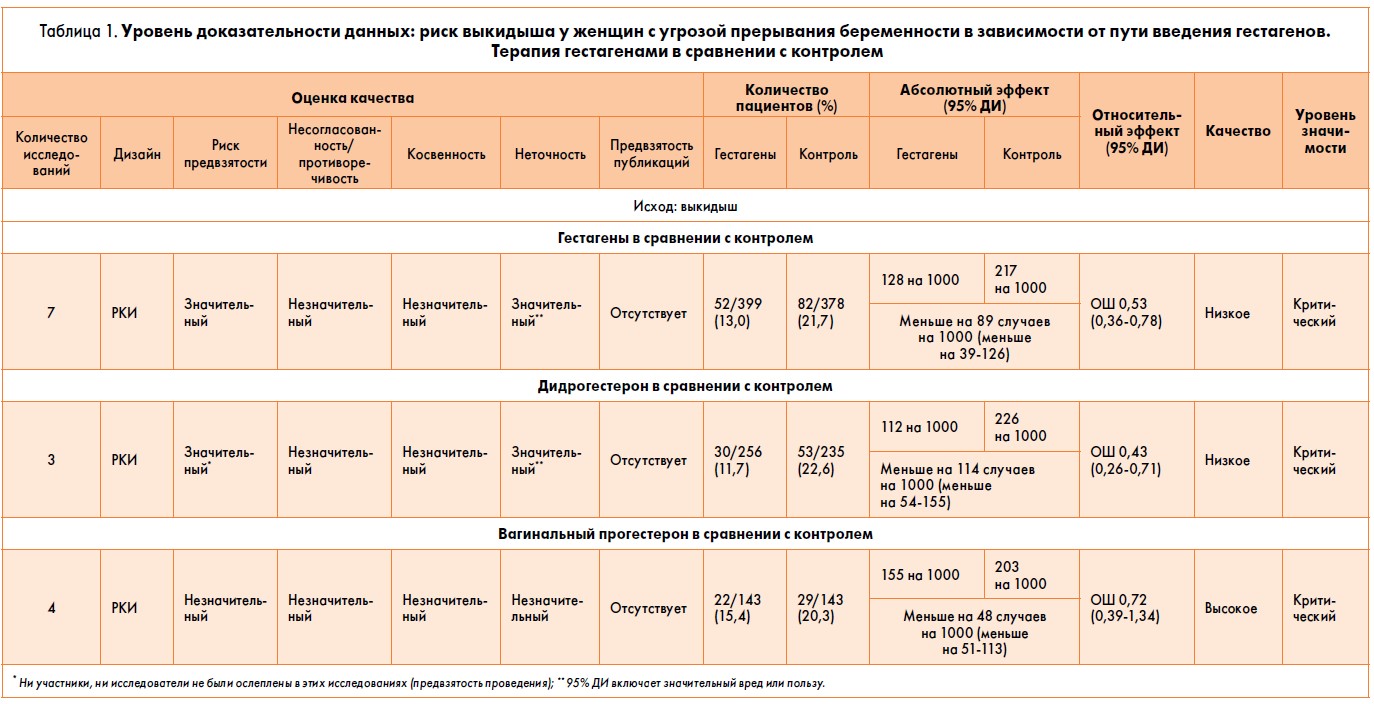
/9/9_4.jpg)
 После перенесенного выкидыша не рекомендуется планировать следующую беременность минимум 3 месяца, оптимальный же срок контрацепции — полгода. При отсутствии противопоказаний лучшим способом контрацепции являются гормональные препараты — помимо высочайшей контрацептивной эффективности они позволяют восстановить нарушенный гормональный фон после прервавшейся беременности.
После перенесенного выкидыша не рекомендуется планировать следующую беременность минимум 3 месяца, оптимальный же срок контрацепции — полгода. При отсутствии противопоказаний лучшим способом контрацепции являются гормональные препараты — помимо высочайшей контрацептивной эффективности они позволяют восстановить нарушенный гормональный фон после прервавшейся беременности.