Перивентрикулярная лейкомаляция — Википедия
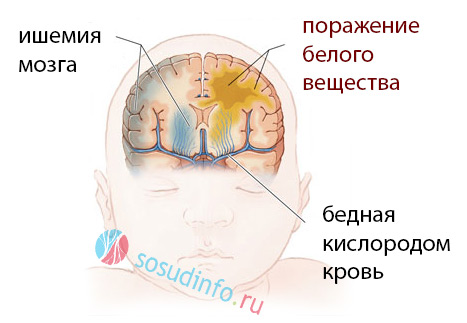
Перивентрикулярная лейкомаляция (ПВЛ) — форма поражения белого вещества полушарий головного мозга у детей, открытая морфологами, одна из причин детского церебрального паралича. ПВЛ характеризуется возникновением очагов некроза, преимущественно коагуляционного, в перивентрикулярных зонах белого вещества полушарий головного мозга у новорождённых детей (редко у мёртворождённых).[3] Она относится к одной из форм так называемой «гипоксически-ишемической энцефалопатии».
Первое микроскопическое описание очага ПВЛ принадлежит J. M. Parrot (1873)[4]. Р. Вирхов[5] лишь макроскопически описал очаги желтоватого цвета в перивентрикулярных зонах боковых желудочков мозга у умерших новорождённых, родившихся от матерей с сифилисом и оспой, относя их к врождённому энцефалиту. Нет достаточных оснований относить данные очаги к ПВЛ. Поражение описывалось под разными названиями («энцефалодистрофия», «ишемический некроз», «перивентрикулярный инфаркт», «коагуляционный некроз», «лейкомаляция», «размягчение мозга», «инфаркт перивентрикулярного белого вещества», «некроз белого вещества», «диффузная симметричная перивентрикулярная лейкоэнцефалопатия»), причём чаще немецкими учеными, но всемирное распространение получил термин «перивентрикулярная лейкомаляция», введённый в 1962 г. B. A. Banker и J. C. Larroche
Наиболее полные в мире исследования ПВЛ на самом большом секционном материале проведены В. В. Власюком (1981)(частота, этиопатогенез, топография, степень поражения различных отделов мозга, стадии развития очагов,нейрогистология, роль микроглии, электроная микроскопия и др.), который впервые выявил высокую частоту поражения зрительной лучистости и доказал, что ПВЛ — это персистирующий процесс, что к старым очагам некрозов могут присоединяться новые, что очаги ПВЛ могут находиться на разных стадиях развития.
По морфологической сути ПВЛ — это мелкоочаговые в основном коагуляционные перивентрикулярные инфаркты белого вещества мозга, чаще двусторонние и относительно симметричные. При ПВЛ очаги некрозов располагаются в перивентрикулярной зоне, но при наличии множества очагов (тяжёлых поражениях) отдельные из них могут распространяться на центральные отделы белого вещества мозга. C наибольшей частотой очаги ПВЛ возникают в перивентрикулярном белом веществе начальных отделов задних рогов боковых желудочков мозга (поражается зрительная лучистость) и центральных отделов желудочков на уровне зрительных бугров (поражается кортико-спинальный тракт). В процессе морфогенеза очаги проходят три стадии: 1) развития некроза, 2) резорбции и 3) формирования глиозного рубца или кисты. Кисты возникают при крупных и сливающихся очагах ПВЛ, при смешанных некрозах (колликвация в центре и коагуляционный ободок по периферии). Вокруг очагов обычно определяется зона других поражений белого вещества мозга — гибель проолигодендроцитов, пролиферация микроглиоцитов и тучных астроцитов, отек, кровоизлияния, гибель капилляров и др. (так называемый «диффузный компонент» ПВЛ). Однако диффузные поражения без некрозов это не ПВЛ. Если произвести 15 фронтальных срезов мозга, то обнаружение очагов ПВЛ в 1-4 срезах свидетельствует о лёгкой степени ПВЛ, в 5-8 срезах — о средней степени ПВЛ и в 9-13 срезах — о тяжёлой степени ПВЛ (2).
Частота ПВЛ по данным разных авторов колеблется от 4,8 % до 88 %, однако часто среди определённой группы детей или по данным нейросонографических исследований, что не вполне объективно. На невыборочном секционном материале частота ПВЛ составляет 12,6 %, причём чаще у мальчиков, а в зависимости от массы при рождении: 1001—1500 г — 13,3 %, 1501—2000 г — 21,5 %, 2001—2500 г — 31,6 %, 2501-3000 г — 14,8 %, более 3000 г — 3,5 %. У недоношенных 1-й и 2-й степеней встречается чаще всего. У умерших в первые сутки после рождения ПВЛ встречается с частотой 1,8 %, а у умерших на 6-й-8-й дни — 59,2 %. В группе родившихся при головном предлежании частота ПВЛ составляет 19,6 %, тазовом предлежании — 17,4 %, при кесаревом сечении — 35,6 %.
Этиологически ПВЛ это гипоксически-ишемическое поражение белого вещества мозга, связанное с артериальной гипотонией, приступами апноэ после рождения, реанимационными мероприятиями, инфекциями и др. Способствует ПВЛ недоношенность, причём небольшой степени (1-2-й). Патогенетические факторы: гипоксия, ацидоз, гипокапния, токсины и др. Очаги некрозов (инфаркты) возникают в пограничной зоне между вентрикулофугальными и вентрикулопетальным артериальными ветвями
Для данной нозологии характерны 2 основных признака:
- 1. локализация в перивентрикулярных зонах белого вещества больших полушарий
- 2. очаги имеют характер преимущественно коагуляционных некрозов.
Вокруг очагов ПВЛ могут определяться другие поражения, так называемый «диффузный компонент».
Время возникновения ПВЛ
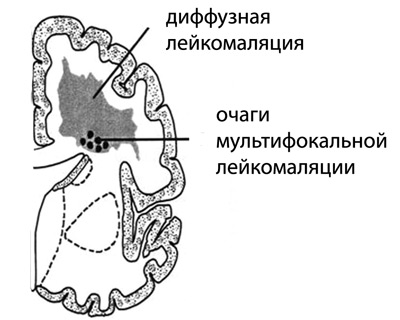
У глубоко недоношенных детей чаще возникают другие поражения белого вещества мозга, отличные от ПВЛ — диффузная лейкомаляция и мультикистозная энцефаломаляция. Ввиду недостаточной изученности последних поражений, их часто стали ошибочно относить к ПВЛ.
ПВЛ надо дифференцировать с со следующими основными поражениями белого вещества больших полушарий мозга:
- отечно-геморрагическая лейкоэнцефалопатия (ОГЛ)
- телэнцефальный глиоз (ТГ)
- диффузная лейкомаляция (ДФЛ)
- субкортикальная лейкомаляция (СЛ)
- перивентрикулярный геморрагический инфаркт (ПГИ)
- внутримозговое кровоизлияние (ВМК)
- мультикистозная энцефаломаляция[11]
- субэпендимальная псевдокиста.
При СЛ очаги некрозов располагаются в субкортикальной области и в отдельных тяжёлых случаях могут распространяться на центральные отделы больших полушарий. При ДФЛ очаги некрозов располагаются диффузно во всех отделах белого вещества мозга, захватывая перивентрикулярную, субкортикальную и центральную области больших полушарий; некрозы колликвационные, ведут к кистообразованию и возникают наиболее часто у глубоко недоношенных детей. При ТГ нет полного некроза мозга и кисты не образуются. ПГИ возникают при тромбозах в системе внутренних мозговых вен или являются осложнением внутрижелудочковых кровоизлияний. Псевдокисты не имеют никакого отношения к некрозам мозга и относятся скорее всего к порокам развития. Патогенез всех перечисленных поражений различен.
В настоящее время имеет место гипердиагностика ПВЛ за счёт переоценки данных нейровизуализационных исследований и недооценки других поражений белого вещества мозга.
- Власюк В. В. Перивентрикулярная лейкомаляция у детей. СПб, «Гликон Плюс», 2009.- 218 с.,ISBN 978-5-93682-540-8.
- Власюк В. В., Туманов В. П. Патоморфология перивентрикулярной лейкомаляци. Новосибирск, «Наука», 1985.- 96 с.
- Власюк В. В., Майер И. О., Охтырская Л. А., Бабуцидзе Т. Я. Перивентрикулярная лейкомаляция у новорождённых и её танатогенетическое значение. Педиатрия, 1981, № 11, с. 32-36.
- Nervivporyadke.ru
- ↑ Disease Ontology release 2019-05-13 — 2019-05-13 — 2019.
- ↑ 1 2 Monarch Disease Ontology release 2018-06-29sonu — 2018-06-29 — 2018.
- ↑ 1. Власюк В. В. Перивентрикулярная лейкомаляция у детей. — СПб.: Гликон Плюс, 2009. — 218 с. ISBN 978-5-93682-540-8.
- ↑ Parrot J. M. Etude sur le ramollissement de l’encephale chez le nouveaune. — Arch. Physiol. Norm. Path., 1873, v. 5, p. 59-79.
- ↑ Virchow R. Zur pathologischen Anatomie des Gehirns: I. Congenitale Encephalitis und Myelitis. — Virchows Arch., 1867, Bd 38, S. 129—138.
- ↑ Banker B. A., Larroche J. C. Periventricular leukomalacia of infancy. A form of neonatal anoxic encephalopathy. — Arch. Neurol., 1962, v. 7, p. 386—410.
- ↑ Власюк В. В., Туманов В. П. Патоморфология перивентрикулярной лейкомаляци. Новосибирск, «Наука», 1985.- 96 с.
- ↑ Власюк В. В., Майер И. О., Охтырская Л. А., Бабуцидзе Т. Я. Перивентрикулярная лейкомаляция у новорождённых и её танатогенетическое значение. Педиатрия, 1981, № 11, с. 32-36.
- ↑ В. В. Власюк Родовая травма и перинатальные нарушения мозгового кровообращения. СПб, «Нестор История», 2009.- 252 С. ISBN 978-5-98187-373-7.
- ↑ De Reuck J., Chattha A. S., Richardson E. P. Pathogenesis and evolution of periventricular leukomalacia in infancy. — Arch. Neurol., 1972, v. 27, p. 229—236.
- ↑ В. В. Власюк, Ю. П. Васильева, А. А. Вильниц, В. Е. Карев. Мультикистозная энцефаломаляция у детей, роль инфекций. Журнал инфектологии, 2010, № 2, с. 45-53. ISSN 2072-6732.
причины, лечение и способы профилактики
В процессе родовой деятельности будущего малыша поджидает множество опасных моментов. Одним из них является перивентрикулярная лейкомаляция – патологический очаг в головном мозге новорожденного, обусловленный недостатком поступления кислорода к его клеткам.
Преимущественное расположение перивентрикулярной зоны поражения – вдоль наружно-верхних отделов боковых желудочков органа. В дальнейшем они могут преобразоваться в кисты или полости, ведущие к тяжелым нарушениям центральной нервной системы малыша. Поэтому профилактике этой патологии уделяется большое внимание врачами во всем мире.
Причины и факторы риска
О важности первых 2–3 месяцев внутриутробного развития ребёнка знают большинство будущим мам. Однако последний триместр беременности также таит в себе множество опасностей для полноценного роста и формирования головного мозга человека.
Специалисты отмечают, что в особой группе риска по формированию перивентрикулярной лейкомаляции – очагам с отмирающими клетками в тканях боковых желудочков, находятся недоношенные дети и те, кто родился ранней весной.
Снижение поступления кислорода к мозговым клеткам обусловлено метеорологическими условиями, провоцирующими спазмы сосудов.

Другие факторы неврологического заболевания:
- эндокринные нарушения у будущей матери – к примеру, диабет;
- анемия беременных;
- авитаминозы;
- внутриутробное инфицирование плода;
- обильные кровотечения в момент родовой деятельности;
- резкие колебания кровяного давления у малыша;
- ранняя острая дыхательная недостаточность у новорожденного.
Тем не менее, главной причиной лейкомаляций головного мозга остается глубокая недоношенность. Поэтому основной упор акушеры-гинекологи делают на своевременную профилактику преждевременных родов и внутриутробной кислородной недостаточности.

Процесс формирования патологии
Для того чтобы понять, что такое ПВЛ и как с нею бороться, необходимо разобраться в механизме ее формирования. На фоне провоцирующих факторов в нервных клетках появляется патологический очаг – из-за кислородного голодания белое вещество органа отмирает. Полноценные нейроциты заменяются иными элементами, которые не способны выполнять те же функции.
Позже – через 7-14 суток на этом участке возникают перивентрикулярные кисты – полые или заполненные особой жидкостью. На завершающем этапе могут появляться рубцы на нервной ткани. Реже в боковых желудочках органа могут наблюдаться вторичные геморрагические инфаркты. В последующем пораженные участки полностью атрофируются.


Как правило, перивентриулярная лейкомаляция развивается в первые часы появления малыша на свет. Однако встречаются случаи, когда перивентрикулярный вариант патологии возникают позднее – до 5-7 суток от момента родов.
Поражение боковых желудочков головного мозга может происходить и внутриутробно – при беременности, сопровождающейся обострением пиелонефрита, гепатита. Для того чтобы этого избежать, женщине необходимо обращаться к наблюдающему за течением беременности врачу при первых же признаках ухудшения самочувствия.
Симптомы и признаки болезни
Заподозрить, что лейкомаляция головного мозга у новорожденных появилась, затруднительно – признаки перивентрикулярной патологии разнообразны и крайне неспецифичны. Тем не менее, недостаток поступления кислорода к нервным клеткам не протекает вовсе бессимптомно. Основные клинические признаки перивентрикулярной лейкомаляции:
- чрезмерная возбудимость новорожденного – крикливость, избыточная хаотичность движений;
- склонность к судорожным состояниям;
- вялость мышечных рефлексов.

У глубоко недоношенных детей симптоматика намного грубее:
- колебание температуры тела;
- вялость;
- повышенная сонливость;
- снижение аппетита;
- нарушение сна;
- парезы/параличи конечностей;
- дыхательные расстройства;
- зрительные нарушения – косоглазие.

Специалисты подчеркивают – проявления перивентрикулярной формы заболевания после острого периода могут стихать. Этот период мнимого благополучия длится до 8-9 месяцев. И только к году лейкомаляция головного мозга дает о себе знать дефицитом нервной деятельности. О течение патологического процесса свидетельствуют:
- недостаточная прибавка в весе;
- медленный рост;
- отставание в освоении навыков;
- несоответствие интеллекта возрасту;
- задержка психоречевого развития;
- выраженная эмоциональная лабильность.
Практически в 90% случаев это заболевание становится причиной развития детского церебрального паралича – тяжелой неврологической патологии, приводящей к инвалидизации.
Прогнозы и степень тяжести ПВЛ
Если женщине не удается доносить малыша до положенного срока – дети появляются на свет недоношенными. Родителям следует заранее подготовиться к правильному уходу за новорожденным.
Относительно благоприятным прогноз будет при легкой степени лейкомаляции головного мозга. В перивентрикулярной клинике преобладает дефицит внимания, а также гиперактивность – хаотичность движений конечностей. Тогда как моторное развитие – своевременность ползанья, ходьбы, переворотов сохраняется.

Специальные коррекционные мероприятия позволяют добиться компенсации расстройства, улучшить физическое и интеллектуальное развитие.
При среднетяжелом и тяжелом характере перивентрикулярной лейкомаляции малыш не будет соответствовать усредненным возрастным нормам – родителям следует быть к этому готовыми. Он позже начнет переворачиваться, присаживаться, ходить.
Затруднено и речевое развитие – слоги появятся позднее, предложения же будут практически недоступны. Иные проявления перивентрикулярной патологии:

- отсутствие естественного детского любопытства;
- болезненность и напряженность мышц конечностей;
- беспокойность, чрезмерная плаксивость;
- нарушение сна – прерывистость, частая путаность дня с ночью;
- грудное вскармливание затруднено – плохо выражен сосательный, а также глотательный рефлекс;
- отклонения в дательной системе – потребность в применении аппарата искусственного дыхания.
Легкая перивентрикулярная лейкомаляция компенсируется к школьному возрасту, при благоприятном течении патологии подросток ничем не отличим от сверстников. Тогда как при тяжелой форме болезни дети становятся инвалидами и требуют постоянного постороннего ухода.
Тактика лечения
Поскольку очаги лейкомаляции подразумевают необратимую гибель нервных клеток, то каких-либо четких схем устранения подобных перивентрикулярных состояний не разработано. Специалисты придерживаются симптоматического подхода – лечение направлено на уменьшение выраженности негативных проявлений.

Перивентрикулярная лейкомаляция у недоношенных детей требует незамедлительного принятия мер по улучшению снабжения клеток кислородом. Для этого следует восстановить полноценный кровоток. Эффективные группы медикаментов:
- ноотропы – усиливают приток крови к нервным клеткам: Пирацетам;
- противосудорожные средства – Карбамазепин;
- витаминные комплексы;
- при высоком внутричерепном давлении – Диакарб;
- при повышенной плаксивости, нарушении сна – успокоительные лекарства на растительной основе, к примеру, Валериана, Мелисса.
Помимо медикаментозной терапии, врачи рекомендуют курсы лечебного массажа и физиотерапии. Обязательно проводятся коррекционные занятия с психологом, педагогами – для стимулирования памяти, мышления, внимания, а также речи.
Родители детей с перивентрикулярной лейкомаляцией должны понимать, что чем больше внимания и труда они вложат в ребенка с первых же дней его жизни, тем лучше он будет развиваться. Поэтому все рекомендации врачей следует выполнять – прием лекарств и массаж, физкультура и правильное питание.
При тяжелой степени перивентрикулярной болезни лечебные мероприятия будут проводиться в стационарных условиях – восстановление дыхательной, сердечнососудистой деятельности, компенсация внутричерепной гипертензии. В этом случае о благоприятном прогнозе речи уже вестись не будет.

Профилактика
Крепкое здоровье детей – это результат усилий их мам с первых дней, когда они узнали о своей беременности. Для того чтобы перивентрикулярная лейкомаляция не возникала, рекомендуется заранее принимать меры профилактики:
- соблюдать принципы здоровой жизни еще на этапе планирования беременности;
- придерживаться сбалансированного питания, с присутствием в рационе различных овощей и фруктов;
- отказаться от всех вредных привычек, особенно употребления табачной и алкогольной продукции;
- заранее пройти консультацию врача, сдать анализы на присутствие в организме скрытых инфекций;
- избегать тяжелых физических, психоэмоциональных нагрузок;
- укреплять защитные барьеры – принимать витаминные комплексы;
- хорошо высыпаться;
- свести к минимуму контакты с людьми, страдающими от заболеваний инфекционного характера.

Узнавшей о своей беременности женщине следует незамедлительно встать на учет к врачу, который будет ее наблюдать на всех этапах внутриутробного развития малыша. Профилактике различных патологий, в том числе и периветрикулярной лейкомаляции у новорожденных, специалистами системы здравоохранения уделяется огромное внимание – разработаны стандарты профилактических исследований у беременных.
Крепкий, здоровый малыш – гордость родителей. Для его полноценного роста и развития – без лейкомаляции, будущая мать должна тесно сотрудничать с врачами и выполнять все их рекомендации.
Перивентрикулярная лейкомаляция (ПВЛ): причины, патогенез
Осложненные роды могут стать причиной травматизма у новорожденных детей. Одной из травм является гипоксико-ишемическое поражение вещества, которое располагается вдоль наружно-верхних отделов боковых желудочков головного мозга. Главным повреждающим фактором является кислородное голодание, хотя в некоторых случаях существуют и другие причины. Таким образом, при наличии мелкоочаговых инфарктов вещества ставится диагноз «перивентрикулярная лейкомаляция» (ПВЛ).
Изменения головного мозга проявляются кистами и полостями, которые формируются в течение примерно одного месяца. Именно поэтому в конце первого месяца жизни для всех новорожденных детей должна быть проведена нейросонография (НСГ).

Поражение носит необратимый характер. Это значит, что лечение, которое применяется после постановки этого диагноза, не может помочь избавиться от патологии.
У недоношенных новорожденных детей часто могут возникать другие поражения головного мозга, которые необходимо дифференцировать от ПВЛ. К некоторым из них относятся церебральная лейкомаляция, телэнцефальный глиоз, псевдокисты, мультикистозная энцефаломаляция, субкортикальная
лейкомаляция и т. д.
Причины и факторы риска
Возможность появления этой патологии повышается у недоношенных детей: при этом чем меньше вес при рождении, тем вероятнее развитие патологического процесса. К другим факторам риска относят пол ребенка: мальчикам диагностируют это заболевание чаще, чем девочкам.
Помимо гипоксии мозга на появление очагов ПВЛ может влиять избыточное количество углекислого газа (гиперкапния) в крови, а также кислородное отравление (гипероксия), которое иногда возникает при искусственной вентиляции легких во время реанимационных мероприятий. Опасной является ситуация резкой смены гипоксии гипероксией, что может случиться без контроля содержания и соотношения кислорода и углекислоты в крови во время ИВЛ. Кроме того, усугублять положение может развившаяся инфекция.
Отмечено также, что риск появления ПВЛ повышается, в зависимости от времени года: чаще всего она диагностируется у тех детей, последние два – три месяца которых приходятся на зиму или раннюю весну. Специалисты связывают это с влиянием метеорологических перепадов, которые влияют на беременность. Также может играть роль гиповитаминоз.
Патогенез
В результате названных причин возникает некроз белого вещества головного мозга, после чего к патологическому процессу добавляется дегенерация астроцитов (звездчатых нейроглиальных клеток с отростками), разрастание микроглии (специфических глиальных клеток ЦНС) и скопление липидосодержащих макрофагов в некротизированных тканях. После этого начинается фагоцитоз поврежденных участков – примерно через 5–7 дней, а через неделю происходит формирование кист (это занимает две недели, а иногда – больше). На завершающих стадиях возникают глиозные рубцы или псевдокисты. В некротизированных областях появляются вторичные геморрагические инфаркты. В течение 2–4 месяцев происходит атрофия ткани.
ПВЛ развивается в первые часы, но также может возникнуть и позднее – вплоть до 10 дней после рождения. Лейкомаляция также может поражать внутриутробно – если течение беременности отличается патологическим характером (гестоз, обострение хронического пиелонефрита, гепатита, фетоплацентарная недостаточность).
Клиническая картина
Уже в роддоме у детей отмечается синдром угнетения центральной нервной системы. Он выражается снижением:
- тонуса мышц;
- специфических рефлексов;
- двигательной активности;
Примерно у четверти новорожденных младенцев присутствует судороги. Почти половина детей страдает от синдрома гипервозбудимости. У некоторых младенцев могут отмечаться стволовые симптомы (нарушения сердечно-сосудистой, дыхательной деятельности). В некоторых случаях какие-либо аномалии в периоде новорожденности могут отсутствовать, а в отдельных вариантах ПВЛ приводит к летальному исходу, независимо от лечения.

Для этого патологического процесса характерно присутствие стадии «мнимого благополучия», которая может длиться 3–9 месяцев, после чего развиваются признаки церебральной недостаточности. Это проявляется нарушением сознания, глотательных рефлексов, дыхания, повышением артериального давления.
Перивентрикулярная лейкомаляция становится почти в 90% случаев причиной детского церебрального паралича (ДЦП), в 60% — сходящегося косоглазия.
Степень тяжести церебральных расстройств зависит от многочисленности и площади лейкомаляционных полостей. Однако в тех случаях, когда очаги распределены тонко вокруг желудочков, прогноз имеет более благоприятный характер.
Процент практически здоровых младенцев с ПВЛ составляет примерно 4%. Последствия поражения для них могут быть незначительны.
Терапевтические мероприятия
Изменения головного мозга носят необратимый характер – по этой причине радикальное лечение, позволяющее избавиться от патологии, не существует. Терапия направлена на устранение негативных симптомов и улучшение мозговых процессов. Стандартно используются ноотропы, корректоры мозгового кровообращения, а также препараты, позволяющие справляться с двигательными нарушениями.
Поскольку ПВЛ в большинстве случаев встречается у недоношенных новорожденных детей, главной мерой профилактики патологии является продление срока беременности, предупреждение преждевременных родов.
Частота осложнений после получения кровоизлияний может снижаться, если адекватно использовать в лечении препараты сурфаканта, уменьшающего проявление дыхательных нарушений. Кроме того, оснащение реанимации новорожденных современной аппаратурой для проведения автономной искусственной вентиляции легких снижает возможность тяжелого последствия для детей.
Поддерживающее лечение ребенка с данным диагнозом должно происходить в течение всего периода детства.
Итак, перивентрикулярная лейкомаляция – это тяжелое поражение головного мозга, которое встречается у новорожденных (преимущественно, недоношенных) детей вследствие тяжелых родов, осложненной беременности. Заболевание следует отличать от других патологий (среди которых псевдокисты, церебральная лейкомаляция, телэнцефальный глиоз и т. д.), по той причине, что лечение этих болезней может отличаться друг от друга.
Оцените эту статью:
Всего голосов: 193
4.37 193
Читайте также
Лейкомаляция (перивентрикулярная) головного мозга детей
© Автор: А. Олеся Валерьевна, к.м.н., практикующий врач, преподаватель медицинского ВУЗа, специально для СосудИнфо.ру (об авторах)
Лейкомаляцию относят к ишемически-гипоксическим повреждениям головного мозга, диагностируемым у новорожденных. Она представляет серьезную проблему неонатологии и неврологии, поскольку отдаленные последствия патологии очень сложно поддаются лечению, приводя к инвалидности.
При лейкомаляции в головном мозге обнаруживают очаги некроза, возникшие после тяжелой гипоксии и нарушения кровотока. Они расположены главным образом вокруг боковых желудочков, поэтому перивентрикулярное поражение – наиболее частый вариант патологии, о котором и пойдет речь ниже.
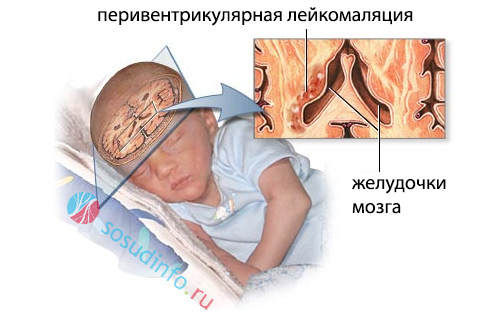
перивентрикулярная (околожелудочковая) лейкомаляция
Перивентрикулярная лейкомаляция (ПЛ) встречается примерно в 12% случаев среди новорожденных, обычно – у недоношенных детей, причем, частота ее зависит от массы, с которой младенец появился на свет. Наибольшее число малышей страдает лейкомаляцией, если масса при рождении была 1500-2500 г. В этом случае патология обнаруживается практически у каждого третьего.
Около 60% новорожденных, проживших до недели, имеют признаки ПЛ. Кесарево сечение значительно повышает ее риск (до 35%) по сравнению с естественными родами, но это касается случаев с уже имеющейся пренатальной патологией. Если малыш внутриутробно рос и развивался нормально, а кесарево сечение проводится в положенный срок, то сама по себе операция не увеличивает риск подобного повреждения головного мозга.
Причины лейкомаляции
Головной мозг недоношенных новорожденных очень чувствителен к недостатку кислорода, так как компенсаторные механизмы еще не развиты, и микроциркуляторное русло не может своевременно обеспечить доставку крови. У доношенных детей с более или менее зрелой нервной системой и кровотоком гипоксия стимулирует кровообращение, поэтому повреждения не будут так выражены.
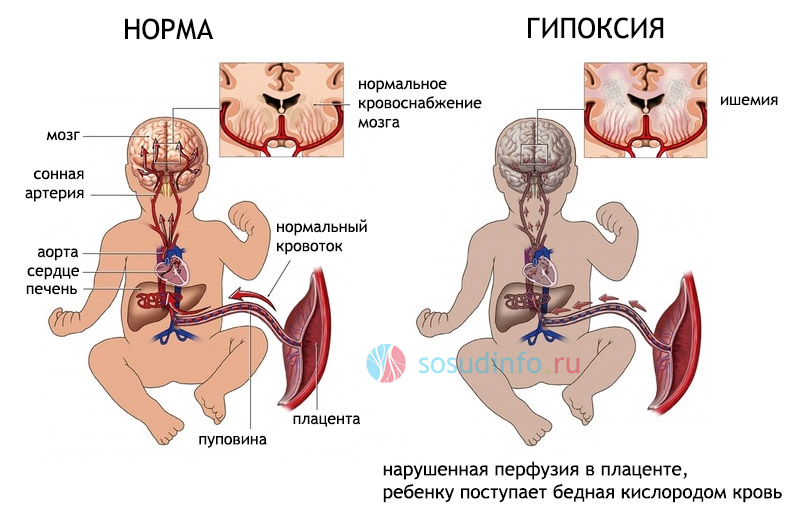
Вариант развития внутриутробной гипоксии (кислородного голодания) из-за недостаточности плацентарного кровотока
Проблема усугубляется еще и тем, что у недоношенных детей нет хорошей связующей сети между артериями мозга, и особенно страдает при этом подкорковый отдел вокруг желудочков, на расстоянии до 1 см от их стенок, больше в теменных зонах. Этим объясняется именно перивентрикулярное (около желудочков) расположение очагов некроза.
Гипоксия вызывает образование свободных радикалов, кислых продуктов обмена, которые не только оказывают непосредственное повреждающее действие на нейроны, но и способствуют нарушению микроциркуляции в виде тромбозов, застоя крови в мелких артериях и венах. Таким образом, гипоксия, сама по себе вызывающая некроз, провоцирует метаболические расстройства и тромбозы, которые еще больше усугубляют ситуацию.
Замечено, что перивентрикулярная энцефалопатия чаще развивается у малышей, находившихся на искусственной вентиляции легких (ИВЛ). Казалось бы, аппарат обеспечивает дыхание и доставку кислорода, поэтому головной мозг страдать не должен. Однако, избыток кислорода, подаваемый через аппарат, провоцирует спазм артериол, который приводит к ишемии.
Частота ПЛ среди новорожденных зависит от времени года. Обычно большее число таких пациентов приходится на зимне-весенний период. Возможной причиной считают недостаток витаминов и влияние неблагоприятных метеоусловий на организм беременной в поздние сроки гестации.
Факторами риска лейкомаляции считают:
- Тяжелые гестозы;
- Хронические инфекции у беременных;
- Внутриутробная гипоксия из-за нарушений в плаценте или кровотоке у плода;
- Аномалии родов – преждевременные роды, преждевременное излитие вод, слабость родовых сил;
- Патология новорожденных – респираторный дистресс-синдром, пневмонии, требующие проведения ИВЛ.
Что происходит в мозге при лейкомаляции?
При лейкомаляции головного мозга в подкорковых структурах появляются очаги некроза, обычно – коагуляционного, гибнут нервные клетки, а дефекты замещаются размножающимися клетками микроглии наподобие того, как образуются рубцы в других органах. Нейроны не могут размножаться, и поля омертвения мозгу нечем заполнить, поэтому следствием их становятся кисты (полости) – кистозная лейкомаляция.
Более половины случаев ПЛ сопровождаются вторичными кровоизлияниями в зоне ишемии и некрозов, возможны кровоизлияния в желудочки мозга. Важно, что кора мозга у таких детей поражается крайне редко в связи с хорошим кровоснабжением.
Лейкомаляция начинается в первые дни и продолжается около недели с момента рождения. Возможно и более позднее ее возникновение, обычно связанное с инфекцией или нарушением дыхания у новорожденного ребенка. В этих случаях на фоне уже имеющихся некрозов могут появляться новые, а состояние ребенка будет прогрессивно ухудшаться.
Очаги мультифокальной лейкомаляции диаметром в 2-3 мм обнаруживают в теменных и лобных долях, симметрично, вокруг стенок боковых желудочков. Реже поражаются височные и затылочные доли мозга. Исходом некроза становится образование множества кист разных размеров, рассеянных по подкорковому слою мозга (кистозная дегенерация), число которых со временем увеличивается. При тяжелой ПЛ они занимают всю перивентрикулярную часть полушарий.
На некроз и образование кист уходит около двух недель, а последующие несколько месяцев в мозге малыша происходит спадение полостей, замещение погибших участков рубцами из нейроглии и необратимая атрофия нервной ткани.
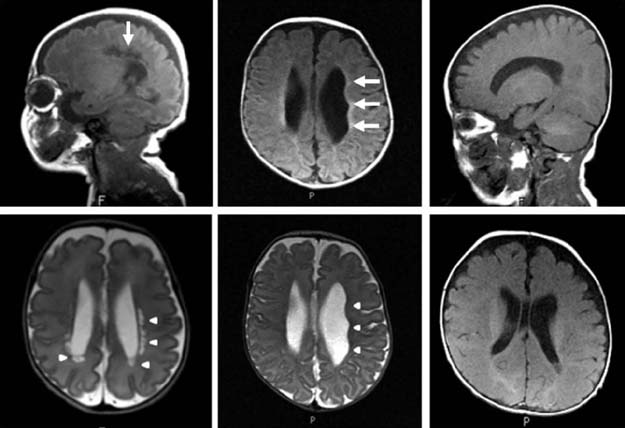
лейкомаляции на снимках МРТ
Проявления лейкомаляции
Признаки лейкомаляции разнообразны и часто неспецифичны, но тяжелое гипоксическое повреждение мозговой ткани не может протекать бессимптомно. Выделяют несколько степеней ПЛ:
- Легкая степень – признаки поражения нервной системы сохраняются до недели от момента рождения;
- Средняя тяжесть – от 7 до 10 дней, возможны судороги, внутричерепная гипертензия, вегетативные нарушения;
- Тяжелая ПЛ – глубокое повреждение с угнетением головного мозга, нередко – кома.
Среди симптомов церебральной лейкомаляции возможны:
- Избыточная нервно-рефлекторная возбудимость или, наоборот, ее угнетение;
- Судорожный синдром;
- Гипотонус мышц;
- Стволовая симптоматика;
- Парезы и параличи;
- Зрительные нарушения в виде косоглазия;
- Задержка психомоторного развития, нарушения интеллекта, гиперактивность, дефицит внимания.
Специалисты особо отмечают, что неврологическая симптоматика в остром периоде и до 3-5 месяцев жизни может быть невыраженной. Примерно у 90% детей после острого периода наступает мнимое благополучие, длящееся до 5 и даже 8-9 месяцев жизни. И только по прошествии такого длительного времени возникают признаки дефицита нервной деятельности на фоне атрофии мозговой ткани.
Вокруг желудочков мозга сконцентрированы проводящие нервные пути, ответственные за двигательную функцию конечностей, поэтому основным признаком церебральной лейкомаляции у детей становится детский церебральный паралич, но степень выраженности его зависит от массивности некроза.
В связи с вовлечением ствола мозга, черепных нервов большая половина малышей страдает косоглазием, чаще – сходящимся, возможны нарушения глотания, дыхательные расстройства. К полугодовалому возрасту проявляется судорожный синдром. Чем больше размер полей некроза и, соответственно, кист, тем больше выражена мозговая недостаточность. Характер симптомов определяется локализацией очагов повреждения (двигательные, зрительные расстройства, судороги, задержка психического развития).
Тяжелое поражение теменных и лобных долей влечет детский церебральный паралич с одновременным нарушением психического развития. Если вовлечены лишь проводящие пути, отвечающие за иннервацию конечностей, то паралич может не сопровождаться нарушением интеллекта и развития ребенка.
Часто у детей, перенесших перинатальную гипоксию, среди симптомов фигурируют дефицит внимания и гиперактивность при сохранном моторном развитии. Это относительно благоприятный вариант патологии, который можно корректировать специальными лечебными мероприятиями.
Ввиду такой непредсказуемости и разнообразия симптомов, маме бывает сложно разобраться, чего ожидать, когда малыш родился раньше срока и в условиях гипоксии. Если поражение носит умеренный или тяжелый характер, то ребенок не будет развиваться соответственно возрасту – не научится вовремя переворачиваться, сидеть и, тем более, ходить. Речевое развитие затормозится, малыш не сможет гулять, не будет следить за игрушками и проявлять такого характерного для своего возраста любопытства.
Особое внимание привлекает гипертонус, который может быть болезненным, поэтому ребенок будет беспокойным, плаксивым, нарушится сон. Грудное вскармливание может стать проблемой из-за плохого сосательного рефлекса, избыточной нервно-мышечной возбудимости или атонии.
Недостаточная прибавка в весе, медленный рост, не соответствующий возрасту, и отсутствие навыков, которыми должен овладевать растущий ребенок – основные симптомы, с которыми приходится иметь дело родителям малыша с умеренной или легкой степенью повреждения подкорковых структур.
Примерно к году становится заметным неврологический дефицит, развивается церебральный паралич, задерживается психомоторное развитие. После года, когда восстановительный период подходит к концу, в клинике преобладают такие последствия, как задержка психоречевого развития, эмоциональная лабильность, проблемы со сном и вниманием, которые могут быть наряду с более тяжелыми моторными расстройствами (детский церебральный паралич).
ПЛ у взрослых может быть причиной церебрального паралича, гипертонуса, нарушений интеллекта, тяжелой олигофрении. При благоприятном течении патологии взрослые люди мало чем отличаются от остальных.
Лечение
Лейкомаляция сопровождается необратимыми изменениями нервной ткани, и какой-либо четкой схемы лечения этого состояния не разработано. Обычно врачи применяют симптоматический подход, в зависимости от конкретных проявлений патологии.
В качестве основного компонента лечения применяют ноотропные средства, помогающие улучшить кровоток и метаболизм в головном мозге (пирацетам, ницерголин, стугерон). Дополнительная терапия направлена на коррекцию двигательных расстройств, нарушений психомоторного развития.
В качестве профилактической меры акушеры-гинекологи предпринимают все возможные попытки пролонгирования беременности до того срока, когда роды станут безопасными для малыша. Если ребенок все же рождается недоношенным, то необходимо сразу же наладить контроль за дыханием и показателями гомеостаза – уровнем кислорода и углекислоты в крови, артериальным давлением, кислотно-щелочным равновесием.
При тяжелой ПЛ дети нуждаются в лечении в условиях реанимации. При необходимости ИВЛ следует четко контролировать газовый состав крови, а при респираторном дистресс-синдроме показаны препараты сурфактанта, позволяющие в части случаев отказаться от искусственной вентиляции.
После года, когда на первый план выходят последствия перенесенной острой ПЛ, лечение большей частью симптоматическое. Повышенная нервно-рефлекторная возбудимость обычно требует наблюдения, а по показаниям могут быть назначены ноотропы, пантогам, фенибут, обладающие некоторым тормозным эффектом. При нарушении сна назначаются успокоительные растительные средства (мелисса, валериана), водные процедуры.
При повышенном внутричерепном давлении и гидроцефалии показан диакарб, возможно применение фуросемида или глицерина одновременно в препаратами калия. При отсутствии эффекта от мочегонных и при нарастании внутричерепной гипертензии проводятся шунтирующие операции для отвода излишков ликвора из головного мозга.
Судорожный синдром лечится с помощью карбамазепина, фенобарбитала. При повышении артериального давления и тахикардии возможно применение бета-адреноблокаторов (анаприлин, обзидан).
При двигательных расстройствах с повышенным тонусом показаны баклофен, мидокалм, реланиум, а при пониженном тонусе – массаж, специальные упражнения, физиотерапевтическое лечение.
Задержка психомоторного развития и речи требует коррекции со стороны педагогов и дефектологов. Помимо ноотропной терапии, витаминов, необходимы постоянные занятия с такими детьми, направленные на развитие внимания, памяти, речи.
Прогноз при церебральной лейкомаляции зависит от масштаба поражения головного мозга. В относительно легких случаях среди последствий преобладают минимальные изменения неврологического статуса, обратимые нарушения интеллекта, а при тяжелых формах поражения мозга возможен детский церебральный паралич, эпилепсия, олигофрения – умственная отсталость.
Рекомендации читателям СосудИнфо дают профессиональные медики с высшим образованием и опытом профильной работы.
На ваш вопрос ответит один из ведущих авторов сайта.
В данный момент на вопросы отвечает: А. Олеся Валерьевна, к.м.н., преподаватель медицинского вуза
Поблагодарить специалиста за помощь или поддержать проект СосудИнфо можно произвольным платежом по ссылке.
Перивентрикулярная лейкомаляция — это… Что такое Перивентрикулярная лейкомаляция?
 | В этой статье не хватает ссылок на источники информации. Информация должна быть проверяема, иначе она может быть поставлена под сомнение и удалена. Вы можете отредактировать эту статью, добавив ссылки на авторитетные источники. Эта отметка установлена 18 июля 2011. |
Перивентрикулярная лейкомаляция (ПВЛ) — форма поражения белого вещества полушарий головного мозга у детей, открытая морфологами, одна из причин детского церебрального паралича. ПВЛ характеризуется возникновением очагов некроза, преимущественно коагуляционного, в перивентрикулярных зонах белого вещества полушарий головного мозга у новорожденных детей (редко у мертворожденных).[1] Она относится к одной из форм так называемой «гипоксически-ишемической энцефалопатии».
История описания
Первое микроскопическое описание очага ПВЛ принадлежит J.M.Parrot (1873)[2]. Р.Вирхов[3] лишь макроскопически описал очаги желтоватого цвета в перивентрикулярных зонах боковых желудочков мозга у умерших новорожденных, родившихся от матерей с сифилисом и оспой, относя их к врожденному энцефалиту. Нет достаточных оснований относить данные очаги к ПВЛ. Поражение описывалось под разными названиями («энцефалодистрофия», «ишемический некроз», «перивентрикулярный инфаркт», «коагуляционный некроз», «лейкомаляция», «размягчение мозга», «инфаркт перивентрикулярного белого вещества», «некроз белого вещества», «диффузная симметричная перивентрикулярная лейкоэнцефалопатия»), причем чаще немецкими учеными, но всемирное распространение получил термин «перивентрикулярная лейкомаляция», введенный в 1962 г. B.A.Banker и J.C.Larroche[4]. Термин недостаточно четкий, так как при ПВЛ возникают не размягчения, а более плотные по сравнению с окружающими участками мозга очаги коагуляционных некрозов. Первая статья в СССР и России, посвященная ПВЛ, написана В. В. Власюком с соавт. (1981), который предложил воспользоваться термином «перивентрикулярная лейкомаляция».
Наиболее полные в мире исследования ПВЛ на самом большом секционном материале проведены В. В. Власюком (1981)(частота, этиопатогенез, топография, степень поражения различных отделов мозга, стадии развития очагов,нейрогистология, роль микроглии, электроная микроскопия и др.), который впервые выявил высокую частоту поражения зрительной лучистости и доказал, что ПВЛ — это персистирующий процесс, что к старым очагам некрозов могут присоединяться новые, что очаги ПВЛ могут находиться на разных стадиях развития.[5][6]
Морфология
По морфологической сути ПВЛ — это мелкоочаговые в основном коагуляционные перивентрикулярные инфаркты белого вещества мозга, чаще двусторонние и относительно симметричные. При ПВЛ очаги некрозов располагаются в перивентрикулярной зоне, но при наличии множества очагов (тяжелых поражениях) отдельные из них могут распространяться на центральные отделы белого вещества мозга. C наибольшей частотой очаги ПВЛ возникают в перивентрикулярном белом веществе начальных отделов задних рогов боковых желудочков мозга (поражается зрительная лучистость) и центральных отделов желудочков на уровне зрительных бугров (поражается кортико-спинальный тракт). В процессе морфогенеза очаги проходят три стадии: 1)развития некроза, 2)резорбции и 3)формирования глиозного рубца или кисты. Кисты возникают при крупных и сливающихся очагах ПВЛ, при смешанных некрозах (колликвация в центре и коагуляционный ободок по периферии). Вокруг очагов обычно определяется зона других поражений белого вещества мозга — гибель проолигодендроцитов, пролиферация микроглиоцитов и тучных астроцитов, отек, кровоизлияния, гибель капилляров и др. (так называемый «диффузный компонент» ПВЛ). Однако диффузные поражения без некрозов это не ПВЛ. Если произвести 15 фронтальных срезов мозга, то обнаружение очагов ПВЛ в 1-4 срезах свидетельствует о легкой степени ПВЛ, в 5-8 срезах — о средней степени ПВЛ и в 9-13 срезах — о тяжелой степени ПВЛ (2).
Частота
Частота ПВЛ по данным разных авторов колеблется от 4,8 % до 88 %, однако часто среди определенной группы детей или по данным нейросонографических исследований, что не вполне объективно. На невыборочном секционном материале частота ПВЛ составляет 12,6 %, причем чаще у мальчиков, а в зависимости от массы при рождении: 1001—1500 г. — 13,3 %, 1501—2000 г. −21,5 %, 2001—2500 г.- 31,6 %, 2501-3000 г.- 14,8 %, более 3000 г. — 3,5 %. У недоношенных 1-й и 2-й степеней встречается чаще всего. У умерших в первые сутки после рождения ПВЛ встречается с частотой 1,8 %, а у умерших на 6-8 дни — 59,2 %. В группе родившихся при головном предлежании частота ПВЛ составляет 19,6 %, тазовом предлежании — 17,4 %, при кесаревом сечении — 35,6 %.[7]
Этиология и патогенез
Этиологически ПВЛ это гипоксически-ишемическое поражение белого вещества мозга, связанное с артериальной гипотонией, приступами апноэ после рождения, реанимационными мероприятиями, инфекциями и др. Способствует ПВЛ недоношенность, причем небольшой степени (1-2-й). Патогенетические факторы: гипоксия, ацидоз, гипокапния, токсины и др. Очаги некрозов (инфаркты) возникают в пограничной зоне между вентрикулофугальными и вентрикулопетальным артериальными ветвями[8], локализующейся в перивентрикулярном белом веществе мозга.
Для данной нозологии характерны 2 основных признака:
- 1. локализация в перивентрикулярных зонах белого вещества больших полушарий
- 2. очаги имеют характер преимущественно коагуляционных некрозов.
Вокруг очагов ПВЛ могут определяться другие поражения, так называемый «диффузный компонент».
Время возникновения ПВЛ — в основном в первые дни после рождения, иногда анте- и интранатально.
Отличия от других поражений
У глубоко недоношенных детей чаще возникают другие поражения белого вещества мозга, отличные от ПВЛ, — диффузная лейкомаляция и мультикистозная энцефаломаляция. Ввиду недостаточной изученности последних поражений, их часто стали ошибочно относить к ПВЛ.
ПВЛ надо дифференцировать с со следующими основными поражениями белого вещества больших полушарий мозга:
- отечно-геморрагическая лейкоэнцефалопатия (ОГЛ)
- телэнцефальный глиоз (ТГ)
- диффузная лейкомаляция (ДФЛ)
- субкортикальная лейкомаляция (СЛ)
- перивентрикулярный геморрагический инфаркт (ПГИ)
- внутримозговое кровоизлияние (ВМК)
- мультикистозная энцефаломаляция[9]
- субэпендимальная псевдокиста.
При СЛ очаги некрозов располагаются в субкортикальной области и в отдельных тяжелых случаях могут распространяться на центральные отделы больших полушарий. При ДФЛ очаги некрозов располагаются диффузно во всех отделах белого вещества мозга, захватывая перивентрикулярную, субкортикальную и центральную области больших полушарий; некрозы колликвационные, ведут к кистообразованию и возникают наиболее часто у глубоко недоношенных детей. При ТГ нет полного некроза мозга и кисты не образуются. ПГИ возникают при тромбозах в системе внутренних мозговых вен или являются осложнением внутрижелудочковых кровоизлияний. Псевдокисты не имеют никакого отношения к некрозам мозга и относятся скорее всего к порокам развития. Патогенез всех перечисленных поражений различен.
В настоящее время имеет место гипердиагностика ПВЛ за счет переоценки данных нейровизуализационных исследований и недооценки других поражений белого вещества мозга.
Литература
- ↑ 1. Власюк В. В. Перивентрикулярная лейкомаляция у детей. — СПб.: Гликон Плюс, 2009. — 218 с. ISBN 978-5-93682-540-8.
- ↑ Parrot J. M. Etude sur le ramollissement de l’encephale chez le nouveaune. — Arch. Physiol. Norm. Path., 1873, v. 5, p. 59-79.
- ↑ Virchow R. Zur pathologischen Anatomie des Gehirns: I. Congenitale Encephalitis und Myelitis. — Virchows Arch., 1867, Bd 38, S. 129—138.
- ↑ Banker B. A., Larroche J. C. Periventricular leukomalacia of infancy. A form of neonatal anoxic encephalopathy. — Arch. Neurol., 1962, v. 7, p. 386—410.
- ↑ Власюк В. В., Туманов В. П. Патоморфология перивентрикулярной лейкомаляци. Новосибирск, «Наука», 1985.- 96 с.
- ↑ Власюк В. В., Майер И. О., Охтырская Л. А., Бабуцидзе Т. Я. Перивентрикулярная лейкомаляция у новорожденных и её танатогенетическое значение. Педиатрия, 1981, № 11, с. 32-36.
- ↑ В. В. Власюк Родовая травма и перинатальные нарушения мозгового кровообращения. СПб, «Нестор История», 2009.- 252 С. ISBN 978-5-98187-373-7.
- ↑ De Reuck J., Chattha A. S., Richardson E. P. Pathogenesis and evolution of periventricular leukomalacia in infancy. — Arch. Neurol., 1972, v. 27, p. 229—236.
- ↑ В. В. Власюк, Ю. П. Васильева, А. А. Вильниц, В. Е. Карев. Мультикистозная энцефаломаляция у детей, роль инфекций. Журнал инфектологии, 2010, № 2, с. 45-53. ISSN 2072-6732.
Перивентрикулярная лейкомаляция головного мозга
Прохождение родовых путей таит для младенца немало опасностей. Одна из них – лейкомаляция головного мозга, формирование патологического очага в перивентрикулярной зоне головного мозга ребенка. Он развивается из-за дефицита кислорода, поступающего к тканям мозга. Располагается очаг поражения в верхних отделах боковых желудочков. Его дальнейшее развитие грозит перерождением в кистообразные новообразования, в образование пустотных полостей. Как результат – тяжелое осложнение в функциях ЦНС у ребенка.
Причины
Гинекологи напоминают будущим мамам, насколько важен период 2-х–3-х месяцев от зачатия ребенка, когда закладывается нервная система будущего человека. Во внутриутробном развитии фактически нет неважных для развития малютки этапов. Последний триместр важен для полноценного формирования мозговых отделов и их функций. Здоровье мамы – залог того, что у ее ребенка не сформируется лейкопатия головного мозга, что он родится доношенным и полноценно развитым.
Статистика показывает, что особую группу риска по образованию лейкомаляции в головном мозге новорожденных составляют дети, родившиеся раньше срока, с фактором недоношенности.
Формированию патологии в перивентрикулярной области мозга подвержены дети, рождающиеся ранней весной.
Перивентрикулярная лейкомаляция представляет собой очаг с некрозом клеток тканей боковых желудочков. Клетки отмирают из-за резкого кислородного голодания, такой же дефицит кислорода ощущает и беременная женщина с повышенной чувствительностью к изменениям метеорологических условий. У будущей мамы болит голова, болезненность спровоцирована спазмами сосудов, как ответ на смену погоды.
Причинами неврологической патологии могут стать:
- диабет у будущей мамы; другие нарушения эндокринной системы;
- анемия и авитаминоз у беременной;
- внутриутробная инфекция во время беременности;
- сильное кровотечение в ходе родов;
- изменение АД новорожденного;
- острый дефицит дыхательной деятельности новорожденного.
И все же главная причина появления лейкомаляций – недоношенность плода. Гинекологи и перинатологи обращают внимание на предупреждение ранних родов, профилактическими мерами пытаются не допустить нарушений внутриутробного кислородного обеспечения.
Механизм развития
Провоцирующие факторы, вызывающие кислородное голодание, приводят к отмиранию белого вещества нервных клеток в первые часы после рождения ребенка. Нейроциты с полноценными функциями перерождаются в патологическую ткань. На 7-14 сутки эти ткани превращаются в кисты перивентрикулярного типа, пустотные или наполненные жидкостью. Завершающий этап формирования патологии – образование рубцовой ткани на нервных волокнах. Пораженная зона атрофируется.

Перивентрикулярная лейкомаляция у недоношенных детей поражает боковые желудочки мозга плода внутриутробно, если беременность осложняется пиелонефритом, гепатитом. Избежать церебрального поражения плода можно, если женщина постоянно наблюдается у врача, при появлении признаков ухудшения своего состояния принимает соответствующие меры для защиты ребенка.
Поражение мозга необратимо, любое лечение этой патологии не избавляет от заболевания, оно остается с человеком на всю его жизнь.
Симптомы
Родителям трудно увидеть симптомы ПВЛ у своего недоношенного ребенка. Патология проявляется разнообразными и невыразительными признаками, которые следует дифференцировать от других нервных заболеваний. Дефицит кислорода для нервных клеток может вызвать и другие болезни.
Для перивентрикулярной лейкомаляции характерна особая клиническая картина, которую видит у грудничка детский врач:
- повышенная возбудимость, выражающаяся в частых криках, лишних движениях;
- появление судорог;
- вялые мышечные рефлексы.
У недоношенных детей ПВЛ проявляется более выраженными симптомами:
- температурными перепадами без видимых причин;
- непреходящей вялостью, сонливостью;
- нарушениями сосательного и глотательного рефлексов;
- расстройствами сна, дыхания;
- парезами конечностей;
- зрительными нарушениями в заметном косоглазии.
Внешние проявления патологии в раннем возрасте сами по себе стихают, взрослым кажется, что лейкомаляция была либо ошибочным диагнозом, либо прошла. Но к году она показывает свои симптомы в явном дефиците ЦНС, видимом отставании в развитии.
МКБ-10 классифицирует несколько видов поражения мозга, которые врачам важно дифференцировать от ПВЛ: церебральная лейкомаляция, глиоз, поликистозная энцефаломаляция, субкортикальная лейкомаляция. Их симптомы схожи, разницу клинической картины показывает своевременно сделанная МРТ.
МРТ детям делают под наркозом, потому что они не в состоянии без движения вылежать необходимое время обследования.
Диагностика
В современных перинатальных центрах детям в первые дни после рождения неонатолог назначает проведение НСГ – нейросонографии, если у врача есть подозрения на развитие патологии в головном мозге. Это обследование показывает сформировавшиеся во внутриутробном развитии кисты и полости, локализующиеся в боковых долях полушарий.
Информативным методом обследования состояния головного мозга является УЗИ, которое специалисты могут сделать ребенку, пока еще не закрыт родничок. Аккуратными движениями врач двигает и поворачивает датчик на месте родничка, просматривая все ткани мозга.
Ранняя диагностика позволяет выявить степени церебрального поражения тканей мозга у новорожденных: легкую, среднюю, тяжелую; повышает вероятность установления правильного диагноза, назначение направленного лечения.

Легкая степень ПВЛ показывает симптомы кислородного голодания в течение 1 недели после рождения малютки. К 7 дням состояние малыша стабилизируется, приходит в соответствие возрастным нормам. При средней степени ПВЛ патогномоничные признаки сохраняются до 2-х недель, могут проявиться судорожные приступы, угасание рефлексов. Такое состояние для малыша опасно дальнейшими последствиями, нарушением вегетатики, нервной проводимости, нарушением речи, поэтому обязательно требуется наблюдение и лечение у детского невропатолога.
Тяжелая степень ПВЛ проявляется в длительном угнетении ЦНС вплоть до комы. Состояние угрожает жизни ребенка, его лечат в условиях реанимации. Если врачам удается вывести малютку из коматозного состояния, то ему на всю жизнь грозит инвалидность.
Лечение
Новорожденным с нарушенными функциями дыхания дают Сурфаксин, Альвеофакт, позволяющие со временем перейти с искусственной вентиляции легких на естественное дыхание. При признаках ослабленного дыхания ребенка возвращают в кювез и вновь дают препараты, поддерживающие дыхательные функции.
В годовалом возрасте лечебные рекомендации направлены на снижение последствий острой ПВЛ, проводится симптоматическая терапия. При среднем и тяжелом течении болезни врачи предупреждают, что от приема лекарства будет только временное улучшение. Киста не рассосется, основные симптомы патологии останутся. Прогноз болезни на тяжелой стадии – только инвалидность человека.

Лечат ПВЛ у детей после года:
- Мексидолом, Мексипримом, Армадином – они улучшают кислородное насыщение крови.
- Актовегином, Церебролизином – это ангиопротекторы, они укрепляют стенки сосудов.
- Нейромультивитом – отлично зарекомендовавшим себя витаминным препаратом.
- Дибазолом, Тропацином – это спазмолитики, они улучшают нервную проводимость.
- Пироцетамом, Ницерголином – ноотропами, улучшающими артериальное кровоснабжение и функции мозга.
- Карбамазепином, Зептолом, Конвулексом – противосудорожными и противоэпилептическими средствами.
- Диакарбом – для снижения внутричерепного давления; с ним вместе обязателен прием кальцийсодержащих препаратов.
- Мелиссой, Валерианой, Пионом – мягкими седативными средствами, допустимыми с раннего возраста.
Разовые и суточные дозы приема препарата рассчитывает невропатолог по возрасту, весу, состоянию ребенка. Родителям запрещается менять или нарушать режим приема препаратов, это влечет необратимые последствия.
Перивентрикулярная лейкомаляция — Periventricular leukomalacia
| Перивентрикулярная лейкомаляция | |
|---|---|
 | |
| Нанесение боковых и третьего желудочков мозга. Перивентрикулярная лейкомаляция включает в себя смерть белой материи вокруг боковых желудочков в плодах и новорожденных. (Изображение из Анатомии Грея , 1918 -е издание) | |
| Специальность | Педиатрия  |
Перивентрикулярная лейкомаляция ( ПВЛ ) является одной из форм черепно — мозговой травмы белого вещества, характеризуется некроза (чаще коагуляции) из белого вещества вблизи боковых желудочков . Это может повлиять на новорожденных и (реже) плодов; недоношенные дети подвергаются наибольшему риску неонатальной энцефалопатии , которые могут привести к этому условию. Затронутые люди обычно имеют проблемы управления двигателем или другие задержки в развитии, и они часто развиваются церебральный паралич или эпилепсии позже в жизни.
Эта патология мозга была описана под разными названиями ( «encephalodystrophy», «ишемический некроз», «перивентрикулярной миокарда», «коагуляционного некроза», «лейкомаляция», «размягчение мозга», «Инфаркт перивентрикулярной белого вещества», «некроз белого вещества»,„диффузный симметричный перивентрикулярные лейкоэнцефалопатия“), а чаще всего немецкими учеными, но распространение во всем мире был термин перивентрикулярная лейкомаляция , введенный в 1962 г. Б. А. Banker и JC Larroche. Этот термин может вводить в заблуждение, так как не существует размягчение ткани в PVL. В. В. Власюк и В. П. Туманов в 1985 году опубликовал первую в мире монографию , посвященную ПВЛ. Власюк (1981) впервые показал высокую частоту оптических лучевых повреждений и продемонстрировал , что ПВЛИ — упорный процесс , который старый некроз может присоединиться к новому, очаги PVL могут находиться на разных стадиях развития.
В процессе морфогенеза фокусирует PVL проходит через три этапа: 1) некроз, 2) резорбция, и 3) образование глиоз рубцы или кисту. Кисты возникают, когда большое и вырожденный фокусируется ПВЛ, со смешанным некрозом (kollikvacia в центре и коагуляции обода на периферии). Вокруг очагов обычно определяется область других поражений головного мозга белого вещества — смерть prooligodendrocytes, mikrogliocytes пролиферации и астроцитов, отек, кровотечение, потеря капилляров и других (так называемый «диффузный компонент ПВЛ»). Тем не менее, диффузные поражения без некроза не ПВЛ.
презентация
Часто бывает невозможно определить PVL на основе физических или поведенческих характеристик пациента. Белое вещество в перивентрикулярных регионах участвуют в большой степени в управлении двигателем, и поэтому люди с ПВЛ часто имеют проблемы двигателя. Однако, так как здоровые новорожденные (особенно недоношенные младенцы) могут выполнять несколько специфических двигательных задач, ранние дефициты очень трудно определить. По мере развития личности, область и масштабы проблем, вызванных PVL могут начать идентифицировать; Однако, эти проблемы обычно обнаруживаются после того, как первоначальный диагноз был сделан.
Степень признаков сильно зависит от степени повреждения белого вещества: незначительное повреждение приводит лишь незначительные дефициты или задержки, в то время как значительное повреждение белого вещества может вызвать серьезные проблемы с двигательной координацией или органом функцией. Некоторые из наиболее часто встречающихся признаков включают развитие отсроченного двигателя, дефицит видения, апноэ , низкие частоты сердечных сокращений , а также судороги .
Развитие Задержка двигателя
Задержка моторного развития детей, пострадавших от ПВЛ была продемонстрирована в нескольких исследованиях. Одна из самых ранних маркеров задержки развития можно увидеть в движениях ног пострадавших детей, уже в возрасте одного месяца. Те, с белой травмы вещества часто демонстрируют «тесной связи» суставов ног (все расширяющих или все сгибая) гораздо дольше, чем у других детей (недоношенных и доношенных). Кроме того, у детей с ПВЛ не может быть в состоянии взять на себя те же позиции для сна, играть и кормить, как преждевременные или доношенных детей того же возраста. Эти задержки развития могут продолжаться в течение младенчества, детства и взрослой жизни.
дефицит видения
У недоношенных детей часто имеют зрительные нарушения и двигательные дефициты контроля глаз сразу же после рождения. Однако коррекция этих дефицитов происходит «в предсказуемом» у здоровых недоношенных детей, и дети имеют видение , сравнимое с доношенными детьми на 36 до 40 недель после зачатия. Дети с ПВЛ часто демонстрируют уменьшились способность поддерживать устойчивый взгляд на неподвижный объект и создавать скоординированные движения глаз. Кроме того, у детей с ПВЛ часто демонстрируют нистагм , косоглазие и рефракции .
Приступы
Появление судорог часто сообщается у детей с ПВЛ. В Израиле на основе изучения детей, рожденных в период между 1995 и 2002 годами, судороги произошли в 102 541, или 18,7%, из ПВЛ пациентов. Приступы, как правило, видели в более тяжелых случаях ПВЛ, воздействуя пациентов с большим количеством повреждений и рожденных при более низких гестационного возраста и веса при рождении.
причины
Предрасполагающие факторы
Те, как правило, считается в наибольшей опасности для ПВЛ преждевременные, младенцы очень низкой массой тела при рождении. Подсчитано, что примерно 3-4% детей, которые весят менее 1500 г (3,3 фунта) имеют PVL, и 4-10% тех, кто родился до 33 недель беременности (но которые выживают более трех дней после родов) имеют расстройство. Гестационный ЦМВ инфекция также производит ПВЛ у новорожденных.
Травма путь
Два основных фактора , по- видимому, участвуют в развитии ПВЛ: (1) снижение артериального или кислородный поток в перивентрикулярной области (белое вещество вблизи желудочков головного мозга) и (2) повреждение глиальных клеток , клетки , которые поддерживают нейроны на протяжении всего нервная система. Эти факторы особенно часто взаимодействуют у недоношенных детей, что приводит к последовательности событий , что приводит к развитию белого вещества поражений .
Исходная гипоксия (снижение расхода кислорода) или ишемии (снижение кровотока) может происходить по ряду причин. Эмбриональные кровеносные сосуды тонкостенные конструкции, и вполне вероятно , что сосуды , обеспечивающие питательные вещества в перивентрикулярной области , не может поддерживать достаточный приток крови во время эпизодов уменьшилась оксигенации в процессе разработки. Кроме того, гипотензии в результате дистресса плода или кесарева сечения родов может привести к снижению крови и потока кислорода в развивающемся головном мозге. Эти гипоксические-ишемические инциденты могут привести к повреждению гематоэнцефалического барьера (ГЭБ), система эндотелиальных клеток и глиальных клеток , которые регулируют поток питательных веществ к мозгу. Поврежденный ВВВ может способствовать еще более высокому уровню гипоксии. Кроме того , повреждение ГЭБ может произойти из — за материнской инфекции во время внутриутробного развития плода инфекций или инфекции вновь поставленного младенца. Потому что их сердечно — сосудистая и иммунная система не в полной мере развита, недоношенные дети особенно подвержены риску этих первоначальных обид.
Ущерб , причиненный ГЭБ при гипоксически-ишемического повреждения или инфекции оттеняет последовательность реакций называется воспалительный ответ . Сразу же после травмы, нервная система генерирует «провоспалительных» цитокинов , которые являются молекулы , используемые для координации ответа на оскорбление. Эти цитокины являются токсичными для развивающегося мозга, и их деятельность в целях реагирования на конкретные области поврежденной ткани , как полагают , чтобы вызвать «ущерб Bystander» в близлежащие районы , которые не были затронуты в первоначальном оскорблении. Дальнейшее повреждение , как полагает, вызвано свободными радикалами , соединений , образующиеся при ишемических эпизодах. Процессы , влияющие на нейроны также вызывают повреждение клеток глии, в результате чего соседних нейронов практически без поддержки системы.
Считается, что другие факторы могут привести к ПВЛ, и исследователи изучают другие потенциальные пути. . В 2007 году в статье Миллер, и др, свидетельствует о том, что повреждение белого вещества не является условие ограничивается недоношенными детьми: доношенные дети с врожденными заболеваниями сердца также демонстрируют «поразительно высокую частоту повреждения белого вещества.» В исследовании, описанное Миллер, 41 доношенных новорожденных с болезнью сердца врожденного, 13 детей (32%) показала белую травму вещества.
диагностика
Как уже отмечалось ранее, часто есть несколько признаков белого вещества травмы у новорожденных. Иногда врачи могут сделать первоначальные наблюдения крайней жесткости или плохой способностью сосать . Предварительный диагноз ПВЛ часто делается с использованием технологий визуализации. В большинстве больниц, недоношенных детей рассматриваются с УЗИ вскоре после рождения , чтобы проверить на наличие повреждений головного мозга. Тяжелые травмы белого вещества могут быть видны головки ультразвука; Однако, низкая чувствительность этой технологии позволяет немного белого повреждения независимо от того , будет хватать. Магнитно — резонансная томография (МРТ) является гораздо более эффективной при определении ПВЛО, но это необычно для недоношенных младенцев , чтобы получить МРТ , если они не были особенно трудный путь развития ( в том числе неоднократного или тяжелая инфекция, или известный гипоксические события во время или сразу же после того, как рождения). Нет учреждения или регулирующие органы не установили протоколы или руководящие принципы для скрининга групп повышенного риска, поэтому каждая больница или врач обычно принимает решения о том, какие пациенты должны быть обследованы с более чувствительным МРТ вместо основного головы ультразвука.
PVL является гипердиагностируемый по нейровизуализации исследования и другие поражения белого вещества мозга занижены. Важно дифференцировать ПВЛ от следующего основных повреждений белого вещества в больших полушарий головного мозга: отечная геморрагическая лейкоэнцефалопатия (OGL), telentsefalny глиоз (TG), диффузная лейкомаляция (DFL), подкорковая лейкомаляция (SL), перивентрикулярные геморрагический инфаркт (PHI), внутримозговое кровоизлияние (ICH), поликистозное размягчение головного мозга (М), субэпендимальный псевдокист. Диффузные поражения белого вещества полушарий головного мозга, сопровождается смягчающими и распространяется на центральные и подкорковые области, более вероятно, DFL, PHI и ME.
профилактика
Предотвращение или задержки преждевременных родов считаются самым важным шагом в снижении риска ПВЛ. Общие методы профилактики преждевременных родов включают методы ухода за собой (диетическое и образом жизни решения), постельный и предписанные анти-усадочного лекарство. Как избежать преждевременных родов позволяет плоду дальнейшее развитие, укрепление систем, пострадавших в ходе развития ПВЛ.
Акцент на пренатального здоровья и регулярные медицинские осмотры матери может также заметно снизить риск ПВЛ. Подскажите диагностика и лечение материнской инфекции во время беременности уменьшает вероятность больших воспалительных реакций. Кроме того, лечение инфекции стероидов (особенно в 24-34 недель беременности) было указано в снижении риска ПВЛ.
Кроме того , были предложено , чтобы избежать материнского кокаина использования и любое материнский плод изменения кровотока может уменьшить риск ПВЛ. Эпизоды гипотензии или уменьшенный поток крови к младенцу могут вызвать повреждение белого вещества.
лечение
Современные методы лечения
В настоящее время нет никаких установленных для ПВЛ лечения. Все процедуры, вводимые в ответ на вторичных патологий, которые развиваются как следствие ПВЛ. Из-за травмы белого вещества в перивентрикулярной области могут привести к различным дефицитам, неврологи должны внимательно следить за детьми с диагнозом ПВЛ, чтобы определить тяжесть и степень их условий.
Пациенты , как правило , обрабатывают индивидуализированного лечения. Это очень важно для врачей , чтобы наблюдать и поддерживать функции органа: висцеральный отказ органа потенциально может возникнуть у нелеченных пациентов. Кроме того, дефицит двигателя и повышенный тонус мышц , часто относятся с индивидуализированными физическими и профессиональными процедурами терапии.
проблемы лечения
Плода и новорожденного мозг быстро меняется, развивается структура. Поскольку нервные структуры все еще развиваются и связи все еще формируются при рождении, многие лекарства, которые являются успешными для лечения и защиты во взрослой центральной нервной системе (ЦНС) неэффективны у детей раннего возраста. Кроме того, некоторые взрослые методы лечения на самом деле было показано, что токсичны для развивающегося мозга.
Будущие процедуры
Хотя никакие процедуры не были одобрены для использования в ПВЛ больных людей, значительное количество исследований , происходит в разработке методов лечения для защиты нервной системы. Исследователи начали изучать потенциал синтетического нейропротекции , чтобы свести к минимуму количество lesioning у пациентов , подвергающихся ишемии.
Прогноз
Прогноз больных с PVL зависит от тяжести и степени повреждения белого вещества. Некоторые дети проявляют относительно небольших дефицитов, в то время как другие имеют значительные дефициты и инвалидность.
повреждение Minor ткани
Незначительные повреждения белого вещества , как правило , проявляется через небольшие задержки в развитии и дефицита осанки, видеосистем и двигательных навыков. Многие пациенты обнаруживают спастическая диплегия , состояние , характеризующееся повышением мышечного тонуса и спастичности в нижней части тела. Походка PVL больных с спастической диплегией имеет необычный характер изгиба при ходьбе.
прогрессия
У пациентов с тяжелой белой травмой вещества обычно имеют более широкие признаки повреждения головного мозга. Младенцы с тяжелыми ПВЛ страдают от чрезвычайно высоких уровней мышечного тонуса и частых приступов. Дети и взрослые могут быть парализованы , показывая потерю функции или паралич всех четырех конечностей.
церебральный паралич
Многие дети с ПВЛ разовьется церебральный паралич . Процент лиц с ПВЛ , которые разрабатывают церебральный паралич , как правило , сообщается со значительной изменчивостью от исследования к исследованию, с оценками в пределах от 20% до более чем 60%. Одной из причин этого несоответствия является большой вариабельностью тяжести церебрального паралича. Этот диапазон соответствует тяжести PVL, который также может быть весьма различны. Более белый ущерб независимо от того , приводит к более тяжелым церебральным параличом; различные подтипы определены и диагноз невропатолога.
Несмотря на различных сортах ПВЛ и церебральным параличом, пострадавших детей, как правило, начинают проявлять признаки церебрального паралича предсказуемым образом. Как правило, некоторые патологические неврологические симптомы (такие, как упоминалось ранее) открыты в третьем триместре беременности (28 до 40 недель после зачатия), а окончательные признаки церебрального паралича видны шесть-девять месяцев.
эпилепсия
Другой распространенный , но исход тяжелой ПВЛ больных является развитие эпилепсии . Связь между этими двумя не совсем понятно; Однако, оказывается , что как генетические , так и ранние факторы окружающей среды вовлечены. Одно исследование показало , что 47% детей с ПВЛ также эпилепсия, с 78% тех пациентов , имеющих форму эпилепсии не легко управляется с помощью лекарств. Многие из этих пострадавших пациентов обнаруживают некоторые судороги, а также спастическая диплегия или более тяжелые формы церебрального паралича, до того, как диагноз эпилепсии производится.
частота
К сожалению, очень мало популяционных исследований по частоте ПВЛ. Как было описано выше, самая высокая частота ПВЛ наблюдается в недоношенных, с очень низкой массой тела при рождении. Эти дети , как правило , проявляется в отделении интенсивной терапии в больнице, с примерно 4-20% пациентов в отделении интенсивной терапии под воздействием ПВЛ. На секционном материале большого без выбора наиболее часто обнаруживаемых PVL у самцов детей с массой тела при рождении было 1500-2500 г., Умирает через 6-8 дней жизни. Диффузное повреждение мозга смягчающей (diffus leucomalacia, DFL) встречается чаще у детей с массой тела менее 1500 г. Однако, ПВЛ не DFL.
Исследование
исследования на животных
Животные модели часто используются для разработки усовершенствованных методов лечения и более полного понимания ПВЛ. Модель крыса, которая имеет повреждения белого вещества и испытывает приступы были разработаны, а также другие грызуны, используемые в исследовании ПВЛ. Эти животные модели могут быть использованы для изучения потенциальной эффективности новых лекарственных препаратов в профилактике и лечении ПВЛ.
Клинические исследования
Текущие клинические исследования в диапазоне от исследований , направленных на понимание прогрессирования и патологии ПВЛ для разработки протоколов для профилактики развития ПВЛ. Многие исследования изучить тенденции в результатах лиц с ПВЛ:. Недавнее исследование , проведенное Hamrick и др рассмотрел роль кистозной перивентрикулярной лейкомаляции (особенно тяжелой формы ПВЛ, включая развитие кист ) в результатах развития младенца.
Другие текущие клинические исследования направлены на профилактику и лечение ПВЛ: клинические испытания испытания нейропротекторов, профилактика преждевременных родов, а также изучения потенциальных лекарственных препаратов для ослабления белого повреждения вещества все время поддерживается NIH финансирования.