Киста селезенки: Причины,Симптомы,Лечение | Doc.ua
Виды заболевания
Среди основных видов кисты селезенки можно выделить такие:
- ложные кисты – развиваются вследствие травм или как осложнение после заболеваний, операций. Причем, 70 % неблагоприятных операций могут дать толчок развитию ложных кист;
- истинные кисты – провоцируются патологическими процессами разного происхождения, часто во время внутриутробного развития;
- паразитные кисты – вызываются микробами или паразитными микроорганизмами. Часто таковым может быть эхинококк, поражающий почки, мозг, печень, селезенку. Личинки эхинококка находятся на поверхности шерсти животных, в водоемах или траве.
Причины
Основная причина кисты селезенки – эмбриогенез, вследствие которого появляются неправильные полости в органе. Также причиной такой патологии могут быть травмы или неправильно проведенные операции, инфекционные или воспалительные проявления в организме. Когда же встречаются серьезные поражения, то это может быть следствием действия паразитов или приобретения абсцесса.
Симптомы
Зачастую симптомы кисты селезенки не проявляют себя, как у ребенка, так и у взрослого. Первые характерные признаки становятся ощутимы уже тогда, когда изменяется размер кисты, то есть она нарастает и воспаляется. Когда встречается киста селезенки у ребенка, то обычно на общее состояние здоровья она не влияет и приступов не вызывает. Но иногда у детей могут наблюдаться приступообразные боли или спазмы в районе левого подреберья, которые сопровождаются тошнотой или рвотой, повышением температуры.
Когда же киста достигает внушительных размеров, то боль начинает отдавать в лопатку и плечо, возникает чувство тяжести, апатия, одышка, небольшой кашель, покалывание в груди. При образовании кисты порядка 20-ти процентов от общего размера селезенки, ощущается слабость и озноб, дисфункция желудка, тошнота.
Диагностика
Чтобы выявить данное заболевание, рационально провести УЗИ, которое является основным способом диагностики этой патологии.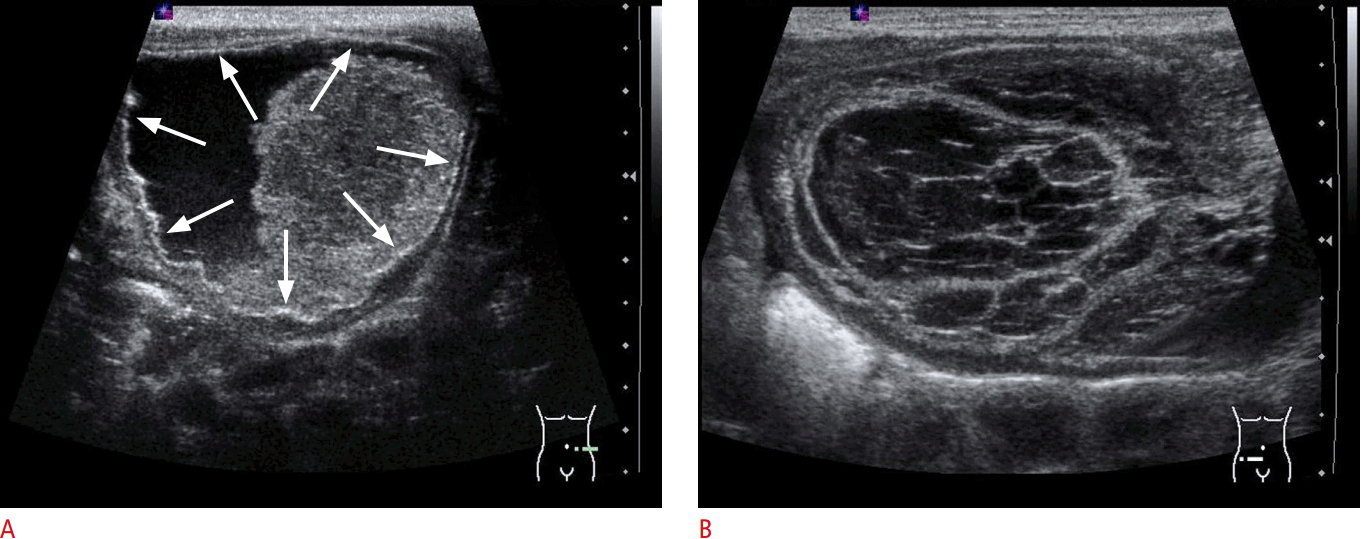 Плюс, необходимо сдать анализ мочи и крови, МРТ. Для контролирования роста кисты периодически проводят УЗИ. Причем, регулярность проведения обследования поможет в дальнейшем выборе лечения, успех которого зависит от уровня диагностики заболевания.
Плюс, необходимо сдать анализ мочи и крови, МРТ. Для контролирования роста кисты периодически проводят УЗИ. Причем, регулярность проведения обследования поможет в дальнейшем выборе лечения, успех которого зависит от уровня диагностики заболевания.
Лечение
Лечение кисты селезенки имеет лишь оперативное вмешательство. Эффективнее и оптимальнее сегодня использовать удаление кисты селезенки с помощью лапароскопии.
- удаление лишь пораженной области селезенки;
- полное удаление селезенки;
- иссечение стенки селезенки;
- удаление патологии на селезенке с оболочкой и ее содержимым внутри;
- вскрытие патологии, обработка полости селезенки и удаление ненужного содержимого.
Лапароскопия в данном случае – не только оптимальный, но и самый альтернативный способ, который позволяет полностью ликвидировать заболевание. Удаление патологических участков кисты проводят при помощи тонких инструментов, которые вводят в специальную камеру. Полная длительность операции составляет порядка 1,5–2 часов. Естественно, после проведения оперативного вмешательства временно больного сопровождает болевой синдром, который исчезает позже за короткое время. То есть реабилитация пациента непродолжительна.

Осложнения
Осложнения данного заболевания могут протекать по-разному, в частности, может появляться:
- нагноение кисты;
- разрыв органа с внутренним кровотечением и вытеканием в брюшную полость;
- раскрытие эхинококковой кисты;
Кистозные образования селезенки у детей Текст научной статьи по специальности «Клиническая медицина»
ХИРУРГИЯ
л
УДК 616.411-006.2-053.2 Авторское мнение
кистозные образования селезенки у детей
Д. А. Морозов — ГБОУ ВПО Саратовский ГМУ им. В. И. Разумовского Минздравсоцразвития России, заведующий кафедрой хирургии детского возраста им. Н. В. Захарова, профессор, доктор медицинских наук; И. В. Горемыкин — ГБОУ ВПО Саратовский ГМУ им. В. И. Разумовского Минздравсоцразвития России, профессор кафедры хирургии детского возраста им. Н. В. Захарова, доктор медицинских наук. В. Б. Турковский — ГБОУ вПо Саратовский ГМУ им. В. И. Разумовского Минздравсоцразвития России, доцент кафедры хирургии детского возраста им. Н. В. Захарова, кандидат медицинских наук; Ф. К. Напольников — Городская клиническая больница им. С. Р. Миротворцева, заведующий детским плановым хирургическим отделением, кандидат медицинских наук; К. Л. Погосян — ГБОУ ВПО Саратовский ГМУ им. В. И. Разумовского Минздравсоцразвития России, аспирант кафедры хирургии детского возраста им. Н. В. Захарова; Е. А. Лукьяненко — ГБОУ ВПО Саратовский ГМУ им. В. И. Разумовского Минздравсоцразвития России, студент 5 курса педиатрического факультета.
D.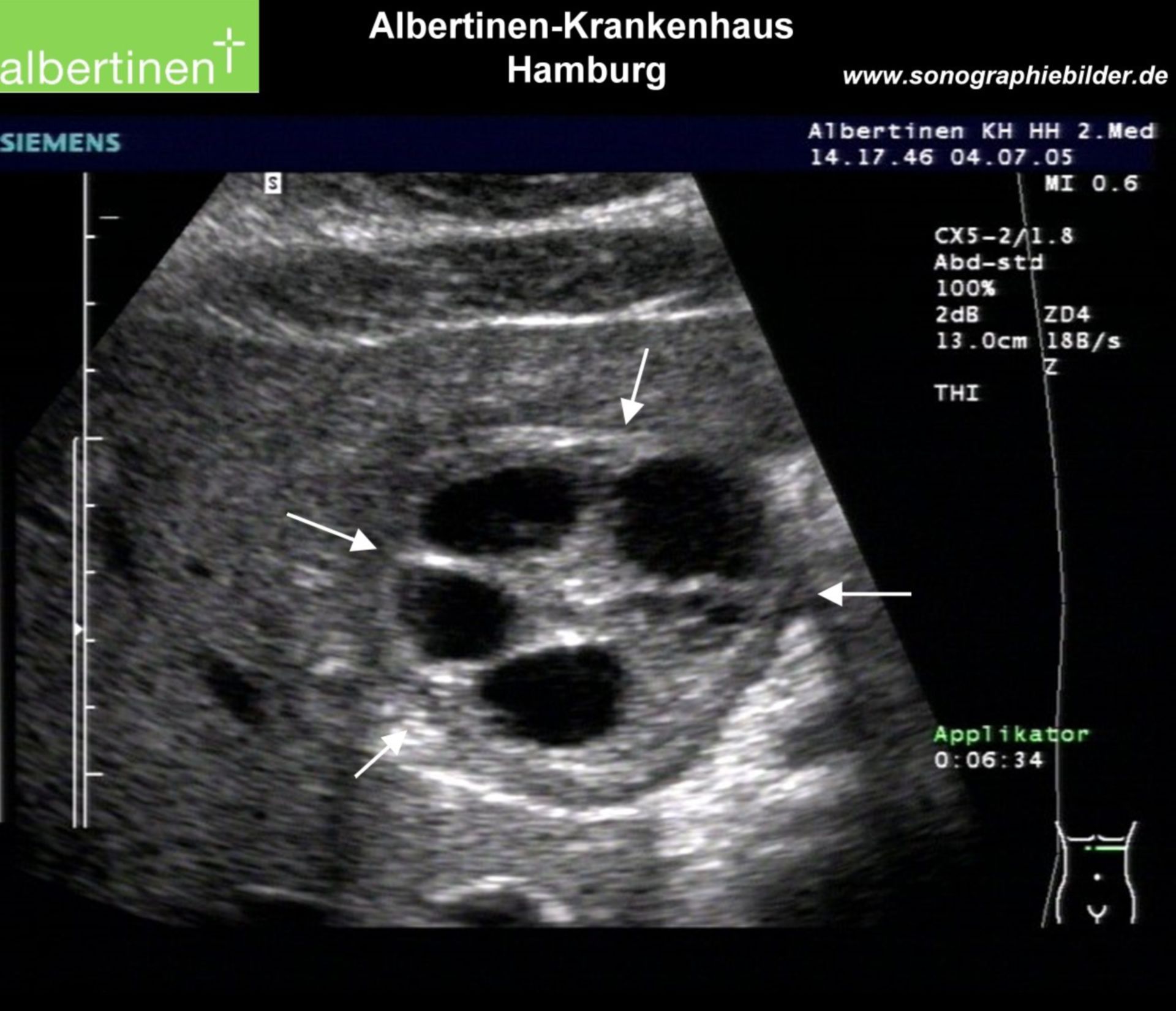 A. Morozov — Saratov State Medical University n.a. V. I. Razumovsky, Head of Department of Pediatric Surgery, Professor, Doctor of Medical Science; I. V. Goremykin — Saratov State Medical University n.a. V. I. Razumovsky, Department of Pediatric Surgery, Professor, Doctor of Medical Science; V. B. Turkovsky — Saratov State Medical University n.a. V. I. Razumovsky, Department of Pediatric Surgery, Assistant Professor, Candidate of Medical Science; F. K. Napolnikov — Saratov Clinical Hospital n.a. S. R. Mirotvortsev, Head of Pediatric Surgery Ward, Candidate of Medical Science; K. L. Pogosyan — Saratov State Medical University n.a. V. I. Razumovsky, Department of Pediatric Surgery, Post-graduate; E. A. Lukyanenko — Saratov State Medical University n.a. V. I. Razumovsky, Pediatric Faculty, Student.
A. Morozov — Saratov State Medical University n.a. V. I. Razumovsky, Head of Department of Pediatric Surgery, Professor, Doctor of Medical Science; I. V. Goremykin — Saratov State Medical University n.a. V. I. Razumovsky, Department of Pediatric Surgery, Professor, Doctor of Medical Science; V. B. Turkovsky — Saratov State Medical University n.a. V. I. Razumovsky, Department of Pediatric Surgery, Assistant Professor, Candidate of Medical Science; F. K. Napolnikov — Saratov Clinical Hospital n.a. S. R. Mirotvortsev, Head of Pediatric Surgery Ward, Candidate of Medical Science; K. L. Pogosyan — Saratov State Medical University n.a. V. I. Razumovsky, Department of Pediatric Surgery, Post-graduate; E. A. Lukyanenko — Saratov State Medical University n.a. V. I. Razumovsky, Pediatric Faculty, Student.
Дата поступления — 12.04.2011 г Дата принятия в печать — 07.09.2011 г
Морозов Д. А., Горемыкин И. В., Турковский В. Б., Напольников Ф. К., Погосян К.Л., Лукьяненко Е. А. Кистозные образования селезенки у детей // Саратовский научно-медицинский журнал. 2011. Т. 7, № 3. С. 724-726.
Сравнивается эффективность методов лечения пациентов с кистозным поражением селезенки. Проанализированы результаты лечения девяти детей с кистами селезенки в возрасте от 9 до 16 лет в период с 1998 по 2009 г Определение диагностической ценности ультрасонографии, компьютерной томографии и магниторезонансного исследования полостных образований селезенки выявило высокую схожесть картины при визуализации лимфангиом, гемангиом, а также истинных кист, поэтому окончательный диагноз ставился после проведения гистологического исследования. Предпочтение отдается малоинвазивным органосохраняющим операциям. Все имеющиеся на сегодня способы сопряжены с возможностью рецидивирования кисты вне зависимости от ее генеза. Перкутанная пункция с дренированием и продленным склерозированием, выполняемая под лапароскопическим контролем, по нашему мнению, является безопасным способом лечения кист селезенки и может выполняться повторно, так как не вызывает спайкообразования в брюшной полости.
Ключевые слова: кисты селезенки, лапароскопия, пункция, дети.
Morozov D.A., Goremykin I. V., Turkovsky V.B., Napolnikov F.K., Pogosyan K.L., Lukyanenko E.A. Cystic growths of spleen in children // Saratov Journal of Medical Scientific Research. 2011. Vol. 7, № 3. P. 724-726.
The effectiveness of different surgical techniques in patients with cystic lesions of spleen is considered in the article. The results of treatment of 9 children aged from 9 to 16 years old during the period from 1998 till 2009 have been analyzed. The examination included ultrasound computerized tomography and MRT Differential diagnosis was made between lymphangiomas, hemangiomas and true cystic growths of spleen. The proper diagnosis was made after histological examination. The invasive procedures preserving spleen were preferred. But despite the surgical technique the possibility of cystic recurrence was remained. Percutaneus puncture with draining and long term sclerotherapy performed by laparoscopy control was considered to be a safe procedure.
Key worlds: splenic cysts, laparoscopy, puncture, children.
Введение. Кисты селезенки у детей встречаются достаточно редко и в большинстве своем являются врожденными кистами, лимфангиомами и гемангио-мами, посттравматическими гематомами, хотя не исключена возможность обнаружения эхинококковой кисты, ангиосаркомы и лимфомы [1-3]. Быстрый рост с нарушением функции органа, а также возможный риск внутрибрюшного кровотечения служат показаниями к оперативному вмешательству [3, 4]. В настоящее время большинство хирургов отказалось от спленэктомии при доброкачественных новообразованиях. В литературе имеются сообщения о применении малоинвазивных методик лечения кист селезенки, таких, как лапароскопические методы [5-7], резекция части селезенки, несущей кисту [8, 9], пер-
Ответственный автор — Игорь Владимирович Горемыкин. Адрес: г. Саратов, ул. Ульяновская,. 42, кв. 85.
Адрес: г. Саратов, ул. Ульяновская,. 42, кв. 85.
Тел.: (сот) 8-927-227-29-38.
E-mail: [email protected]
кутанная аспирация и склерозирование кисты [10]. В работе сравнивается эффективность некоторых диагностических и лечебных методов.
Методы. Проанализированы результаты лечения девяти детей с кистами селезенки в возрасте от 9 до 16 лет, находившихся в клинике детской хирургии Саратовского медицинского университета в период с 1998 по 2009 г. Кистозное поражение селезенки чаще всего протекало бессимптомно и обнаруживалось при УЗИ органов брюшной полости и забрюшинного пространства по поводу других заболеваний. Только у двух детей отмечались ноющие боли в левом подреберье, которые носили приступообразный характер. В анамнезе ни у одного ребенка не было травмы или предшествующего инфекционного заболевания. При пальпации живота только у двух пациентов определялось опухолевидное образование, исходящее из левого подреберья, безболезненное, малоподвижное, плотноэластической консистенции, при этом
объем кист превышал 500 мл с локализацией в нижнем полюсе селезенки. Спленомегалия выявлена у трех больных. Основными методами диагностики были УЗИ, КТ и МРТ селезенки.
В 1990-х годах двум детям была выполнена спле-нэктомия в связи с расположением кист в области ворот селезенки, при этом диагностированы лим-фангиома и гемангиома. Лапаротомия с фенестра-цией кисты была выполнена двум детям. У одного ребенка киста исходила из верхнего полюса по задней поверхности и не визуализировалась при лапароскопическом осмотре, что заставило выполнить конверсию. У другого пациента киста располагалась в области ворот селезенки в глубине паренхимы, размером 14,0×10,0x9,0 см. Гистологически диагностированы лимфангиома и врожденная киста селезенки.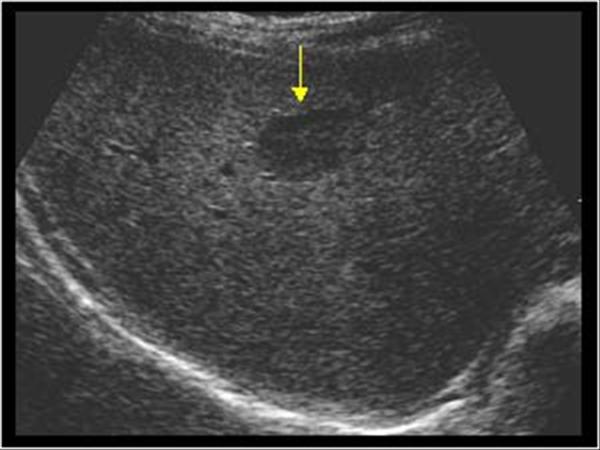
В последнее время отдаем предпочтение малоинвазивным технологиям. Трем детям была выполнена лапароскопическая фенестрация. Кисты располагались в верхнем полюсе селезенки. Их наибольший диаметр составлял от 4 до 6 см. У двоих гистологически диагностирована лимфангиома селезенки, а у одного ребенка врожденная киста. Двум пациентам под лапароскопическим контролем был чрескожно установлен «нефростомический» дренаж в полость кисты с последующей склерозирующей терапией 96% раствором этилового спирта. Гистологическое исследование не проводилось из-за отсутствия материала при пункционном способе лечения.
Приводим описание нескольких клинических случаев.
Больной А., 10 лет, объективно определяется спленомегалия. При УЗИ органов брюшной полости в воротах селезенки обнаружено гипоэхогенное образование 6,0×5,8×5,4 см с четкими ровными контурами. Выполнена спленэктомия. Гистологическое заключение: гемангиома селезенки. Послеоперационный период протекал без осложнений.
Больной П., 16 лет, при УЗИ выявлено гипоэхо-генное образование в верхнем полюсе селезенки округлой формы 10,0×9,5×8,0 см, которое было подтверждено на КТ. Выполнена лапаротомия с широкой фенестрацией кисты. Гемостаз с использованием «Tachocomb». В полости кисты оставлен трубчатый дренаж с активной аспирацией в течение 10 дней. Г и-стологический диагноз: врожденная киста селезенки. Ребенок выписан на 12-е сутки в удовлетворительном состоянии. На контрольном УЗИ через год изменений нет, через 3 года в верхнем полюсе селезенки визуализируются образования в виде трех мелких кист диаметрами от 1 до 2 см.
Больная Л., 15 лет, в течение двух недель беспокоили периодические боли в левом подреберье. УЗИ и КТ выявили образование в верхнем полюсе селезенки размером 7,0×5,7×5,5 см. Выполнена лапароскопическая фенестрация кисты с тампонадой прядью сальника. Гистологический диагноз: лимфангиома селезенки. Послеоперационный период протекал без осложнений.
Выполнена лапароскопическая фенестрация кисты с тампонадой прядью сальника. Гистологический диагноз: лимфангиома селезенки. Послеоперационный период протекал без осложнений.
Больной З., 15 лет, при УЗИ выявлено гипоэхоген-ное образование в верхнем полюсе селезенки округлой формы 6,0×4,0x4,5 см, которое было подтверждено на КТ. Под лапароскопическим контролем был установлен «нефростомический» дренаж в полость кисты, в течение недели проводилась склерозирую-щая терапия 96% раствором этилового спирта с экспозицией 4-5 минут. При УЗИ через 6 месяцев киста не определялась.
Больной М, 13 лет, поступил в клинику с жалобами на наличие безболезненного опухолевидного образо-
вания в левом подреберье. Спленомегалия. Выполнены УЗИ, КТ и МРТ, выявившие полостное образование с капсулой до 5 мм толщиной и внутренней трабекулярностью. Размеры кисты: 12,3×11,2×11,0 см. Под лапароскопическим контролем в полость установлен «нефростомический» дренаж и эвакуировано около 1 литра желтоватого прозрачного содержимого. В течение двух недель проводилась склерозирующая терапия 96% раствором этилового спирта до полного прекращения накопления жидкости в полости кисты. Ребенок выписан на 15-й день после операции и вновь поступил в клинику через две недели с фебрильной температурой и болями в левом подреберье. УЗИ селезенки показало, что полость кисты заполнена жидкостью с взвесью. Под лапароскопическим контролем крыша кисты рассечена и удалено около 700 мл мутного выпота без запаха. В полости оставлен трубчатый дренаж с последующей активной аспирацией в течение двух недель. Экссудация прекратилась на 8-е сутки. Ребенок выписан в удовлетворительном состоянии с остаточной ламинарной полостью в верхнем полюсе селезенки.
Результаты. Обсуждая диагностическую ценность УЗИ, КТ и МРТ полостных образований селезенки, следует отметить высокую схожесть картины при визуализации лимфангиом, гемангиом, а также истинных кист, поэтому окончательный диагноз устанавливается после проведения гистологического исследования..jpg) УЗИ при лимфангиомах и гемангиомах дает хорошо выраженное гипоэхогенное образование с внутренними септами и взвесью повышенной эхоплотности. Содержимое истинных кист, как правило, лишено взвеси и является гомогенным. При этом врожденные кисты обычно одиночные, правильной формы, хотя и могут достигать значительных размеров, в то время как крупные лимфангиомы окружены более мелкими образованиями (рис. 1) и в их содержимом обнаруживается взвесь повышенной плотности (рис. 2).
УЗИ при лимфангиомах и гемангиомах дает хорошо выраженное гипоэхогенное образование с внутренними септами и взвесью повышенной эхоплотности. Содержимое истинных кист, как правило, лишено взвеси и является гомогенным. При этом врожденные кисты обычно одиночные, правильной формы, хотя и могут достигать значительных размеров, в то время как крупные лимфангиомы окружены более мелкими образованиями (рис. 1) и в их содержимом обнаруживается взвесь повышенной плотности (рис. 2).
Отличительными особенностями гемангиом и лимфангиом селезенки от врожденных кист на КТ являются спленомегалия и обнаружение участков линейного и глыбчатого обызвествления (двое детей) (рис. 3 а). Граница с неизмененной паренхимой
Рис. 1. МРТ. Лимфангиома селезенки
Рис. 2. УЗИ. Лимфангиома селезенки: видны септы и неоднородное содержимое кисты
Рис. 3. КТ. Лимфангиома селезенки: а — определяются кальцифицированные участки и септы внутри кисты; б — КТ. Врожденная киста селезенки
обычно четкая как при истинных кистах, так и при лимфангиомах (рис. 3 а, б). При выполнении МРТ отличить сосудистые опухоли от истинных кист селезенки практически невозможно, так как они представлены округлыми образованиями повышенной интенсивности (рис. 1), поэтому МРТ мы использовали в основном для установления топического положения кисты в паренхиме.
Обсуждение. Сравнивая эффективность способов лечения полостных образований селезенки, мы не выявили каких-либо явных преимуществ того или иного способа. Спленэктомия, по нашему мнению, должна применяться только при наличии очаговых или диффузных изменений паренхимы селезенки, характерных для лимфомы, ангиосаркомы и геман-гиоэндотелиомы [3]. Использование лапароскопии для фенестрации кисты или уточнения области пункции для дренирования со склерозированием значительно снижает травматичность вмешательства по сравнения с «открытой» фенестрацией.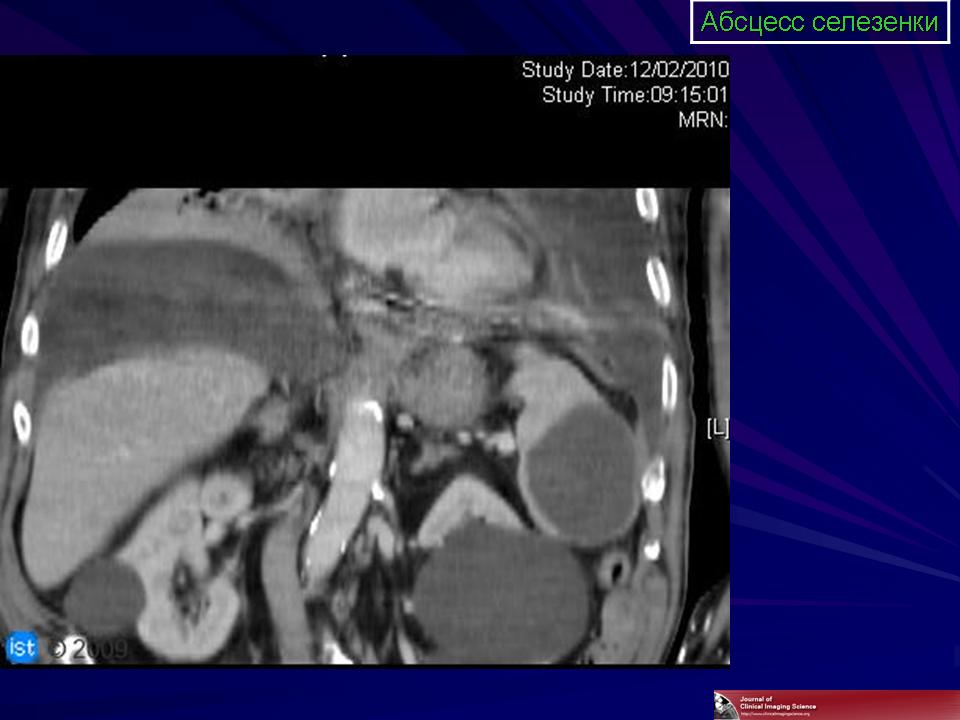 Применение УЗИ для контроля пункции и дренирования является наименее травматичным способом.
Применение УЗИ для контроля пункции и дренирования является наименее травматичным способом.
Наличие гигантской кисты (емкостью свыше 800 мл) диктует необходимость широкой фенестрации с удалением «крыши», так как большая площадь внутренней поверхности кисты обусловливает выраженную экссудацию, препятствующую слипанию стенок. Накопление экссудата, исходя из нашего опыта, может приводить к инфицированию даже на фоне массивной антибиотикотерапии.
Заключение. Доброкачественные полостные образования селезенки являются редкой патологией в
детском возрасте и требуют индивидуального подхода при планировании оперативного лечения. Предпочтение отдается малоинвазивным органосохраняющим операциям. Все имеющиеся на сегодня способы сопряжены с возможностью рецидивирования кисты вне зависимости от ее генеза. Перкутанная пункция с дренированием и продленным склерозированием, выполняемая под лапароскопическим контролем, является безопасным способом лечения кист селезенки и может выполняться повторно.
Библиографический список
1. CT of congenital and acquired abnormalities of the spleen/J. L. Freeman, S. Z. Jafri, J. L. Roberts [et al.] // Radiographics. 1993. № 13. P. 597-610.
2. Cystic Masses of the Spleen: Radiologic-Pathologic Correlation/M. Urrutia, P. Mergo, L. Ros [et al.] // RadioGraphics. 1996. № 16. P. 107-129.
3. Primary Vascular Neoplasms of the Spleen/R. V. Abbott, A. D. Levy, N. S. Aguilera [et al.] // Radiologic-Pathologic Correlation. 2004. № 24. P. 1137-1163.
4. Epithelial splenic cysts in children: surgical treatment by cyst-wall «peeling»/A. Calisti, M. L. Perrotta, Ph. Molle [et al.] // J. Pediatr. 2003. Sur. № 19. P. 300-302.
L. Perrotta, Ph. Molle [et al.] // J. Pediatr. 2003. Sur. № 19. P. 300-302.
5. Дронов А. Ф., Поддубный И. В., Котлобовский В. И., Залихин Д. В. Лапароскопическая хирургия при патологии селезенки у детей // Эндоскопическая хирургия. 1998. № 4. С. 18-22.
6. Лапароскопические вмешательства при кистах печени и селезенки/В. Н. Филижанко, Е. Г. Шеменева, А. М. Фомин [и др] // Эндоскопическая хирургия. 1998. № 1. С. 56-57.
7. Open and laparoscopic treatment of nonparasitic splenic cysts/D. Gianom, A. Wildisen, T. Hotz, [et al.] // Dig. Surg. 2003. № 20. P. 74-78.
8. Partial splenectomy: the preferred alternative for the treatment of splenic cysts/M. F. Brown, A. J. Ross, H. C. Bishop [et al.] // J. Pediatr. Surg. 1989. № 24. P. 694-696.
9. Partial splenectomy for benign cystic lesions of the spleen/A. Khan, A. Bensoussan, A. Ouimet [et al.] // J. Pediatr. Surg. 1986. № 21. Р 749-752.
10. Splenic cysts: aspiration, sclerosis, or resection/C. Moir, F. Guttman, S. Jequier [et al.] // J. Pediatr. Surg. 1989. № 24. P. 646-648.
References
1. CT of congenital and acquired abnormalities of the spleen/J. L. Freeman, S. Z. Jafri, J. L. Roberts [et al.] // Radiographics. 1993. № 13. P. 597-610.
2. Cystic Masses of the Spleen: Radiologic-Pathologic Correlation/M. Urrutia, P. Mergo, L. Ros [et al.] // RadioGraphics. 1996. № 16. P. 107-129.
3. Primary Vascular Neoplasms of the Spleen/R. V. Abbott, A. D. Levy, N. S. Aguilera [et al.] // Radiologic-Pathologic Correlation. 2004. № 24. P. 1137-1163.
2004. № 24. P. 1137-1163.
4. Epithelial splenic cysts in children: surgical treatment by cyst-wall «peeling»/A. Calisti, M. L. Perrotta, Ph. Molle [et al.] // J. Pediatr. 2003. Sur. № 19. P. 300-302.
5. Dronov A. F., Poddubnyj I. V., Kotlobovskij V. I., Zalihin D. V. Laparoskopicheskaja hirurgija pri patologii selezenki u detej // Jendoskopicheskaja hirurgija. 1998. № 4. S. 18-22.
6. Laparoskopicheskie vmeshatel’stva pri kistah pecheni i selezenki/V. N. Filizhanko, E. G. Shemeneva, A. M. Fomin [i dr] // Jendoskopicheskaja hirurgija. 1998. № 1. S. 56-57.
7. Open and laparoscopic treatment of nonparasitic splenic cysts/D. Gianom, A. Wildisen, T. Hotz, [et al.] // Dig. Surg. 2003. № 20. P. 74-78.
8. Partial splenectomy: the preferred alternative for the treatment of splenic cysts/M. F. Brown, A. J. Ross, H. C. Bishop [et al.] // J. Pediatr. Surg. 1989. № 24. P. 694-696.
9. Partial splenectomy for benign cystic lesions of the spleen/A. Khan, A. Bensoussan, A. Ouimet [et al.] // J. Pediatr. Surg. 1986. № 21. Р 749-752.
10. Splenic cysts: aspiration, sclerosis, or resection/C. Moir, F. Guttman, S. Jequier [et al.] // J. Pediatr. Surg. 1989. № 24. P. 646-648.
Кисты и доброкачественные новообразования селезенки — Клиника хирургии «Кураре»
Селезенка — непарный орган, отвечающий в организме человека за кроветворение, иммунитет и кровоснабжение. Строение селезенки: уплощенная овальная форма и в основном состоит из лимфоидной ткани.
Размеры в норме: 16 х 6 х 1.5 — 2.5 см,
Основной процент заболеваний селезенки связан с вторичным процессом, являющиеся следствием заболеваний других органов и систем – болезней крови, иммунных патологий, опухолей, системных заболеваний или повреждений (травм) селезенки. К ним относятся: инфаркт селезенки, перекрут ножки селезенки, абсцесс селезенки, разрыв селезенки, киста селезенки, доброкачественные и злокачественные образования селезенки.
К ним относятся: инфаркт селезенки, перекрут ножки селезенки, абсцесс селезенки, разрыв селезенки, киста селезенки, доброкачественные и злокачественные образования селезенки.
Кисты селезенки
Одной из более частой патологии селезенки являются киста селезенки. Формирование кисты обусловлено многими факторами (причины):
-нарушение эмбрионального развития плода (формирование полостей)
-травма селезенки (закрытая и открытая травма живота, оперативные вмешательства)
-острый воспалительный процесс селезенки (тяжелые инфекционные заболевания)
-инфаркт селезенки
-паразитарные заболевания
Классификация кист селезенки:
-истинные (врожденные)
-ложные (приобретенные)
Клиническая картина: клиническая картина зависит от размеров кисты селезенки. При наличии кисты размерами до 2-3 см характерно бессимптомное течение заболевания. При воспалении кисты селезенки, при резком увеличении в размерах кисты появляется боль в левом подреберье, повышение температуры тела, тошнота, головокружение. При очень больших размерах боль отдает в левую лопатку и плечо, тяжесть в левом подреберье после приема пищи, периодически возникает рвота.
Лечение:
-если киста размерами до 3 см и исключен паразитарный характер кисты, требуется динамическое наблюдение.
-киста более 3 см, имеющая тенденцию к увеличению в размерах, существует опасность перерождения в злокачественную опухоль, опасность разрыва и инфицирования кисты, — является показанием к оперативному лечению.
Объем и метод операций индивидуален как каждого случая, зависит размеров, расположения (центральная, периферическая), характера кисты (паразитарная и непаразитарная), от тяжести состояния пациента, сопутствующей терапевтической патологии.
Виды операций:
-открытая спленэктомия
-лапароскопическаяспленэктомия
-лапароскопическая резекция кисты селезенки
Миниинвазивные манипуляции:
-чрескожная пункция и дренирование кисты , склеротерапия под ультразвуковым наведением
Первичные новообразования селезенки могут быть как доброкачественными, так и злокачественными.
Доброкачественные опухоли селезенки
Из доброкачественных опухолей селезенки встречаются гемангиомы (опухоли сосудистого происхождения), лимфангиомы, лимфомы (опухоли лимфоидной ткани), эндотелиомы, гамартомы, фибромы.
При малых размерах опухолей нет никаких проявлений. При прогрессировании процесса (вплоть до разрыва селезенки) и увеличения в размерах, капсула селезенки растягивается и пациента начинают беспокоить боли постоянного характера.
Лечение: только хирургическое. Объем операции и метод операции зависит от размеров, расположения (центральная, периферическая), от тяжести состояния пациента по сопутствующей терапевтической патологии.
Виды операций:
-открытая спленэктомия
-лапароскопическая спленэктомия
-лапароскопическая резекция селезенки
Злокачественные опухоли селезенки
Злокачественные опухоли селезенки могут быть первичными или вторичными (метастатическими).
К первичным опухолям селезенки относятся саркомы, злокачественная лимфома (первичный очаг только в селезенке).
К вторичным опухолям селезенки относятся метастазы рака другой локализации.
Лечение: комбинированное (хирургическое — удаляют пораженный орган + химиотерапия).
Виды операций:
-открытая спленэктомия
-лапароскопическая спленэктомия
Гигантская киста селезенки у ребенка с хроническим лейкозом
Кисты селезенки у детей наблюдаются сравнительно редко [1–3]. Встречаются как врожденные, так и посттравматические кисты. Как правило, оперативное лечение кист селезенки заканчивается удалением органа. С момента первого сообщения, посвященного постспленэктомическому сепсису у детей, прошло 60 лет (Н. King, Н. Schumacher, 1952). С тех пор отношение хирургов к спленэктомии радикально изменилось в сторону приверженности к органосохраняющей тактике как при травмах, так и при кистах селезенки.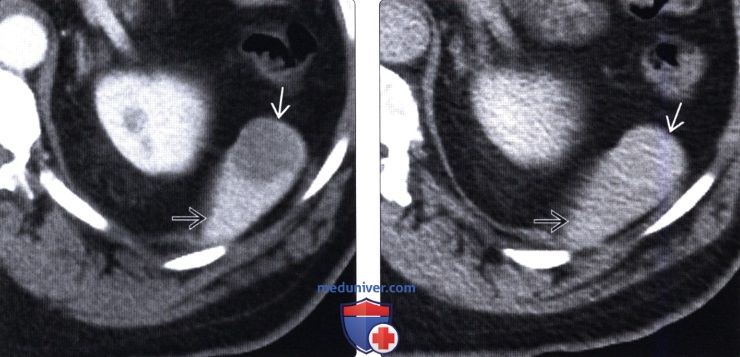 Общепринято считать, что кисты селезенки с диаметром более 4–5 см необходимо удалять оперативным путем, так как высок риск разрыва, нагноения кисты или внутрибрюшного кровотечения [2, 3]. Избежать формирования постспленэктомического синдрома особенно важно при сопутствующих заболеваниях, сопровождающихся развитием иммунодефицитных состояний, в том числе после полихимиотерапии у онкологических больных. В предлагаемом наблюдении удалось осуществить органосохраняющую операцию при наличии гигантской кисты селезенки у ребенка с хроническим лейкозом. Приводим наше наблюдение.
Общепринято считать, что кисты селезенки с диаметром более 4–5 см необходимо удалять оперативным путем, так как высок риск разрыва, нагноения кисты или внутрибрюшного кровотечения [2, 3]. Избежать формирования постспленэктомического синдрома особенно важно при сопутствующих заболеваниях, сопровождающихся развитием иммунодефицитных состояний, в том числе после полихимиотерапии у онкологических больных. В предлагаемом наблюдении удалось осуществить органосохраняющую операцию при наличии гигантской кисты селезенки у ребенка с хроническим лейкозом. Приводим наше наблюдение.
Ребенок Г., 17 лет (история болезни № 8818), поступил в I хирургическое отделение областной детской клинической больницы г. Донецка 03.08.2011 г. с жалобами на периодические боли в животе, подъем температуры тела до 38 °С, увеличение в объеме живота (рис. 1). Из анамнеза известно, что пациент находился на лечении в онкогематологическом центре института неотложной и восстановительной хирургии им. В.К. Гусака по поводу впервые установленного миелоидного лейкоза, Phпозитивного, хронической фазы. Мальчик считает себя больным с 21.06.2011 года, когда появились умеренные боли в левой половине живота, лихорадка. До этого периода рос и развивался соответственно возрасту, травм не было. В отделении получал гливек, аллопуринол, новапим, инфузионную терапию, переливание эритроцитарной массы.
Была выполнена (28.07.11) спиральная компьютерная томография (КТ): селезенка увеличена в размерах до 140 ´ 77 ´ 161 мм, однородной структуры, обычной плотности, без дополнительных образований, контуры ее четкие, ровные. По диафрагмальной поверхности селезенки определяется жидкостное содержимое. В области переднего края селезенки, под передней брюшной стенкой слева, от уровня Th2позвонка, распространяясь каудально до уровня полости таза, определяется кистозное образование размерами 210 ´ 143 ´ 224 мм, жидкостной плотности, с четкими контурами, имеющее интимную связь с селезенкой, оттесняющее петли кишечника вправо.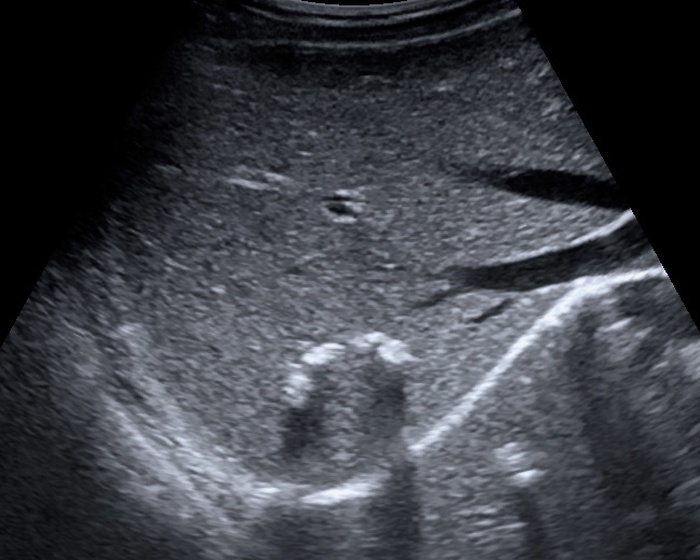 Выводы: киста селезенки, наиболее вероятно обусловленная последствиями разрыва селезенки. После дообследования больной переведен в клинику детской хирургии для оперативного лечения.
Выводы: киста селезенки, наиболее вероятно обусловленная последствиями разрыва селезенки. После дообследования больной переведен в клинику детской хирургии для оперативного лечения.
Общее состояние при поступлении тяжелое по основному заболеванию. Вял, адинамичен. Кожные покровы чистые, бледные. Правильного телосложения, удовлетворительного питания. Периферические лимфоузлы во всех группах не увеличены, в паховой области до 1 см, плотные. В легких жесткое дыхание, тоны сердца ритмичные, систолический шум на верхушке. Живот увеличен в объеме, участвует в акте дыхания. При пальпации мягкий, безболезненный, от левого подреберья до входа в таз пальпируется опухолевидное образование эластической консистенции, умеренно болезненное. Имеется асцит. Печень выступает на 3 см изпод края реберной дуги. Стул и мочеиспускание не нарушены.
В клинике обследован. Ультразвуковое исследование (УЗИ) органов брюшной полости (05.08): печень — размеры увеличены, левая доля 72 мм, правая доля 150 мм, край ниже реберной дуги на 3 см. Паренхима гомогенная, без очаговых изменений. Желчный пузырь, поджелудочная железа — без патологии. Размеры селезенки резко увеличены до 336 ´ 199 мм, тканевая часть 144 ´ 77 мм (рис. 2). Подвижность селезенки резко ограничена. Контуры неровные, четкие. Рисунок структур хорошо дифференцирован. Паренхима неоднородная, у нижнего полюса по медиальной поверхности имеется киста размерами 229 ´ 210 мм с тканевым компонентом. Кровоток в области нижнего полюса селезенки отсутствует. Визуализируемые фрагменты внутрипаренхиматозных сосудов и сосудов ножки селезенки без признаков деформации и дилатации, структура их стенок без особенностей. В брюшной полости по фланкам и в малом тазу свободная жидкость, большое количество неорганизованного жидкого содержимого с мелкодисперсной взвесью. Заключение: эхографические признаки гигантской кисты селезенки. Общий анализ крови: Нb — 114 г/л, Эр. — 3,5 · 1012/л, ЦП — 0,9; Л — 12,5 · 109/л, СОЭ — 34 мм/ч, э — 5, п — 4, с — 83, л — 6, м — 2, тромбоциты — 245 · 109/л (70 : 1000).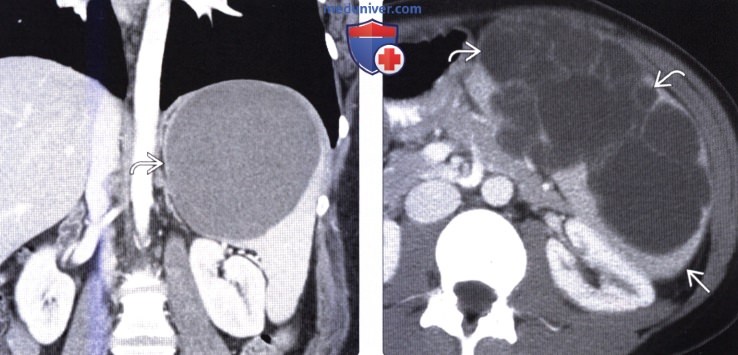 В биохимическом анализе крови и общем анализе мочи без патологии.
В биохимическом анализе крови и общем анализе мочи без патологии.
10.08.2011 г. произведена операция (хирург — к.м.н. К.В. Латышов). Срединная лапаротомия. Выпот серозный, мутный, с фибрином, до 100 мл. При ревизии органов брюшной полости установлено, что всю брюшную полость занимает опухолевидное образование упругоэластической консистенции 30 ´ 25 см, с точечными кровоизлияниями. Киста окутана большим сальником, спаяна с брюшной стенкой и брыжейкой кишечника. Киста уходит в левое подреберье, исходит из нижнего полюса селезенки (рис. 3). Петли кишечника оттеснены книзу и вправо. Тупым и острым путем кистозное образование отделено от передней брюшной стенки и боковых карманов. Вывести кисту в рану не удается. Решено произвести пункцию образования. С помощью атмоса эвакуировано до 5 литров жидкости коричневого цвета с нитями фибрина. Оболочки кисты спаялись, она рассечена. В просвете опухолевидного образования имеется мутное, желеобразное содержимое, оболочки утолщены до 4 мм. Выполнена резекция большого сальника, подпаянного к кисте. Частично острым, частично тупым путем произведена резекция кистозного образования в пределах здоровых тканей до нормальной части селезенки. Демукозация остатков оболочек кисты, прилегающих к паренхиме селезенки (рис. 4). Поэтапно оболочки обработаны раствором бетадина. Произведено подшивание краев оболочек кисты к паренхиме селезенки (рис. 5). Из полости малого таза удалены сгустки фибрина. Дополнительно осушено до 200 мл мутного выпота. Операционная рана послойно ушита наглухо. Макропрепарат: оболочки кисты размером 30 ´ 25 см, утолщены до 4 мм, с обилием кровоизлияний. Диагноз после операции: гигантская киста (дермоидная? посттравматическая? тератодермоидная?) нижнего полюса селезенки с явлениями воспаления. Оментит. Асцит.
Послеоперационный период протекал гладко. Больному проводилась инфузионная терапия, переливание эритроцитарной массы, альбумина, получал фортум, метронидазол, лацидофил, прозерин, анальгин, димедрол..jpg) Перестал лихорадить. Контрольное УЗИ (15.08): селезенка 119 ´ 63 мм. Нижний полюс повышенной эхогенности. От 19.08: у нижнего полюса селезенки визуализируется многокамерное кистозное образование размером 34 ´ 18 ´ 28 мм, нижний контур неровный, бугристый (рис. 6).
Перестал лихорадить. Контрольное УЗИ (15.08): селезенка 119 ´ 63 мм. Нижний полюс повышенной эхогенности. От 19.08: у нижнего полюса селезенки визуализируется многокамерное кистозное образование размером 34 ´ 18 ´ 28 мм, нижний контур неровный, бугристый (рис. 6).
Общий анализ крови (19.08): Нb — 112 г/л, Эр. — 3,5 · 1012/л, ЦП — 0,9; Л — 6,5 · 109/л, СОЭ — 20 мм/ч, э — 5, п — 1, с — 84, л — 7, м — 3, тромбоциты — 245 · 109/л (70 : 1000). Швы сняты, рана зажила первичным натяжением.
Заключение патогистологического исследования (№ 78837909): стенки кисты селезенки представлены плотной волокнистой соединительной тканью без внутренней эпителиальной выстилки. Киста заполнена некротическим детритом, который выявляется и на ее внутренней поверхности (рис. 5а). В толще стенки вокруг многих сосудов располагаются мелкие очаги лимфомакрофагальной инфильтрации, местами — с примесью плазматических клеток и единичных полиморфноядерных лейкоцитов (рис. 5б). Встречаются участки с обильной васкуляризацией, очаговыми, преимущественно периваскулярными кровоизлияниями с образованием гранул гемосидерина и формированием гемосидерофагов (рис. 5в). На многих участках в толще стенки кисты выявляется пролиферация фибробластов и миофибробластов, которые формируют разнонаправленные пучки и участвуют в образовании основного вещества молодой волокнистой соединительной ткани (рис. 5г).
В удовлетворительном состоянии ребенок 22.08.2011 г. выписан домой. Осмотрен через 1 и 2 месяца. Жалоб не предъявляет. Живот при пальпации мягкий, безболезненный. УЗИ (26.09.11): селезенка размером 103 ´ 73 мм, паренхима однородная. У нижнего полюса эхогенное включение 20 ´ 15 мм, неравномерное, овоидной формы. Наблюдается гематологом. Явлений обострения основного заболевания не было.
Выводы: начальные признаки растущей кисты селезенки — боли в брюшной полости и пальпируемое опухолевидное образование. Решающими в диагностике заболевания являются УЗИ и КТ.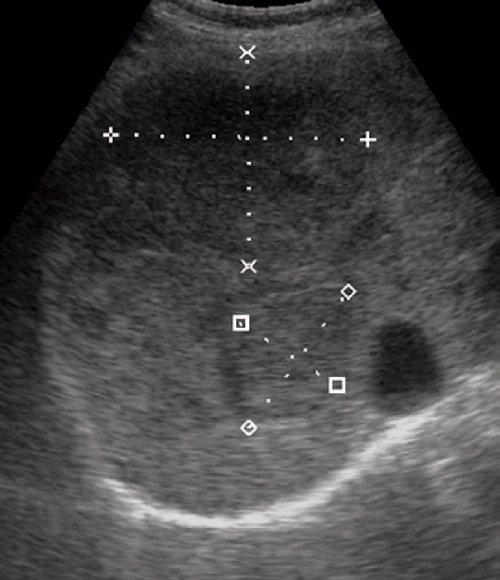 Наиболее целесообразно при гигантских кистах селезенки выполнение органосохраняющих оперативных вмешательств.
Наиболее целесообразно при гигантских кистах селезенки выполнение органосохраняющих оперативных вмешательств.
Страница статьи : Детская хирургия
Higaki K., Jimi A., Watanabe J., Kusaba A., Kojiro M. Epidermoid cust of the spleen with CA 19-9 or carcinoembryonic antigen productions: report of three cases. Am. J. Surg. Pathol. 1998; 22(6): 704-8.
Zvizdić Z., Karavdić K. Spleen-Preserving Surgery in treatment of large mesothelial splenic cyst in children-a case report and review of the literature. Bosn. J. Basic. Med. Sci. 2013; 13(2): 126-8.
Hansen M.B., Moller A.C. Splenic cysts. Surg. Laparosc. Endosc. Percutan. Tech. 2004; 14(6): 316-22.
Kabra N., Bowen J. Congenital splenic cyst: A case report and review of the literature. J. Pediatr. Child. Health. 2001;37(4): 400-2.
Беляева О.А., Кондрашин С.А., Поляев Ю.А., Гарбузов Р.А., Мусаев Г.Х., Бондар З.М. и др. Комбинированные навигационные оперативные вмешательства у детей с солитарными кистами селезёнки. Российский вестник детской хирургии, анестезиологии и реаниматологии 2016; 6(1): 16-23
Hodge M.G., Ricketts R.R., Simoneaux C.R., Abramowsky C.R., Elawabdeh N., Shehata B.M. Splenic cysts in the pediatric population: areport of 21 cases with review of the literature. Fetal and Pediatric Pathology. 2012; 31(2): 54-62.
Rescorla F.J., West K.W., Engum S.A., Grosfeld J.L. Laparoscopic splenic procedures in children. Experience in 231 children. Annals of surgery. 2007; 246(4): 683-7; discussion 687-8.
Рябов А., Морозова О., Рубанский М., Казанцев А., Панферова Т., Волобуев А. и др. Опухоли и кисты селезёнки у детей. Врач. 2010; (11): 40-3.
Karfis E.A., Roustanis E., Tsimoyiannis E.C. Surgical management of nonparasitic splenic cysts. J.S.J.S. 2009; 13(2): 207-12.
Ширяев А.А., Мусаев Г.Х., Харнас С.С, Рябова А.В., Кондрашин С.А., Ахмедова С.Н. и др. Непаразитарные кисты селезенки, методы хирургического лечения. Вестник хирургической гастроэнтелогии. 2013; (4): 26-32.
2013; (4): 26-32.
Sellers G.J., Starker P.M. Laparoscopic treatment of a benigh splenic cyst. Surg. Endosc. 1997; 11(7):766-8.
Mertens J., Penninckx F., DeWever I., Topal B. Long-term outcome after surgical treatment of nonparasitic splenic cysts. Surg. Endosc. 2007; 21(2): 206-8.
Smith S.T., Scott D.J., Burdick J.S., Rege J.S., Jones D.B. Laparoscopic marsupialization and hemisplenectomy for splenic cysts. J. Laparoendosc. Adv Surg. Tech. A. 2001; 11(4): 243-9.
Kaiser M.M., Fischer F. Wessel M.L. The laparoscopic spleen-preserving approach to splenic cysts: advantages and limitations. Zentralbl. Chir. 2008; 133(2): 142-7.
Kaiwa Y., Kurokawa Y., Namiki K., Matsumoto H., Satomi S. Laparoscopic patial splenectomies for true splenic systs. Surg. Endosc. 2000; 14(9): 865.
Cai H., An Y., Wu D., Chen X., Zhang Y., Zhu F. et al. Laparoscopic partial splenectomy: a preferred method for select patients. J. Laparoendosc. Adv. Surg. Tech. A. 2016; 26(12): 1010-4.
Правила подготовки ребенка к УЗИ брюшной полости, подготовка к УЗИ грудничку и детям до года, нормы и расшифровка УЗИ
Оглавление
УЗИ (ультразвуковое исследование) – медицинский осмотр органов человека, который производится при помощи специального датчика. Данный прибор испускает высокочастотные звуковые волны, которые затем отражаются от обследуемых тканей пациента. Результат такого исследования проецируется непосредственно на монитор врача.
Это один из самых современных и безболезненных типов обследования. Он совершенно безопасен для пациентов любого возраста и пола, а также для плода, развивающегося в утробе беременной женщины.
Одновременно это один из наиболее точных анализов, который позволяет рассмотреть структуру внутренних органов, выявить наличие патологий, заболеваний или новообразований.
Какие заболевания выявляются в ходе УЗИ у детей?
Ультразвуковое исследование брюшной полости может быть назначено ребенку как в профилактических целях (в возрасте 1–1,5 месяцев), так и для диагностики заболеваний или отклонений.
Необходимо пройти такой осмотр, если у ребенка:
- Выявлены патологии в развитии
- Есть жалобы на боли в спине, боку или животе
- Зафиксировано пожелтение белков глаз, кожи
- Присутствует чрезмерное газообразование, вздутие живота
- Имеются боли неустановленного характера при пальпации
- У ребенка замечено частое нарушение стула
- Меняется вес
- Проблемы, связанные с тяжестью в животе, тошнотой и горечью в ротовой полости
УЗИ позволяет выявить такие заболевания, как:
- Реактивный панкреатит поджелудочной железы
- Внутреннее кровотечение
- Мононуклеоз — вирусная болезнь, поражающая печень, селезенку и иные органы
- Заболевания крови
- Кисты и другие новообразования
- Абсцесс органов — воспалительный процесс, который сопровождается скоплением гнойных масс
- Заражение паразитами
- Водянка — характеризуется скоплением жидкости в органах
- Мочекаменная болезнь
- Пиелонефрит — воспаление, сосредоточенное в почках
УЗИ брюшной полости грудничку: нужна ли подготовка?
Для проведения УЗИ брюшной полости детям до 1 года требуется несложная подготовка. Она заключается в голодании за некоторое время до процедуры:
- Для новорожденных данный период составляет три часа
- Младенцу на грудном вскармливании также достаточно трех часов
- Малышу на искусственном кормлении нужно 3,5 часа
Лучше всего принести такого младенца на обследование прямо перед следующим приемом пищи. Самым удобным периодом времени для осмотра в данном случае является первая половина дня.
УЗИ брюшной полости ребенку от 1-го года: какая нужна подготовка?
Дети в возрасте от года до трех слишком малы, чтобы спокойно терпеть чувство голода, жажду или позывы к мочеиспусканию. Поэтому для них существуют простые правила:
- Диета
- Последний период питания должен быть за 4–5 часов до обследования
- За час до начала анализа нельзя пить воду (в крайнем случае, малышу можно дать совсем немного жидкости)
Для более взрослого ребенка подготовка усложняется. Она включает в себя:
- Легкую диету
- Опорожнение кишечника и регуляцию пищеварения
- Голодание перед процедурой в течение 6–8 часов
За два-три дня до осмотра необходимо перевести ребенка на облегченную пищу:
- Каши на воде
- Паровую нежирную рыбу и птицу
- Одно вареное яйцо в день
- Сыр
Необходимо исключить такие продукты, как:
- Черный хлеб и иную выпечку
- Молочные продукты
- Овощи
- Бобовые
- Жирные блюда
- Газированные напитки
- Жевательную резинку и конфеты
Накануне процедуры можно сделать клизму, а также принимать регулирующие пищеварение препараты, если у ребенка наблюдаются нарушения стула или повышенный метеоризм.
В случае, если врач ранее прописал ребенку препараты, которые необходимо принимать во время еды, то прием данного лекарства необходимо отложить.
Противопоказания
Ультразвуковое исследование безопасно для детей любого возраста, поэтому противопоказаний к данной процедуре нет.
Затруднение при проведении обследования может возникнуть из-за того, что ребенок окажется в нестандартной для него ситуации. Поэтому перед анализом нужно объяснить малышу, что и зачем будет делать врач.
Проблемы при использовании УЗИ могут возникнуть, если у ребенка повреждена та часть кожи, на которую будет наноситься гель, — имеются рана или болезненные кожные высыпания. Также проведение процедуры будет затруднено в случае, если малышу слишком больно лежать в необходимой для анализа позе.
Норма и расшифровка УЗИ брюшной полости у детей
Если перед проведением УЗИ брюшной полости подготовка к исследованию ребенка прошла правильно, то обследование покажет четкое и контрастное изображение исследуемых органов.
В норме у ребенка не должно быть кист и иных новообразований, все органы должны иметь однородную структуру и четкие границы. Для детей разных возрастов правильные размеры органов отличаются.
По результатам исследования врач оценивает:
- Поджелудочную железу — ее размеры, форму и структуру, а также состояние ее протоков
- Почки — их однородность, наличие или отсутствие конкрементов (камней), толщину стенок, общие размеры
- Печень — ее эхогенность, размеры долей
- Желчный пузырь – форму, правильность развития желчных протоков, размеры и толщину стенок
- Селезенку — ее форму, однородность тканей и размеры
В некоторых случаях УЗИ может показать нестандартную форму одного из органов. Но не всегда это является патологией — данное явление может оказаться индивидуальной особенностью организма, которая не несет никакого вреда.
Преимущества проведения процедуры в МЕДСИ
- В МЕДСИ используется современное ультразвуковое оборудование экспертного класса, которое позволяет поставить диагноз наиболее точно
- Все УЗИ-аппараты подходят как для взрослых, так и для детей
- Врачи-диагносты высоких квалификационных категорий помогут с подготовкой к исследованию, а также обеспечат качественную расшифровку результатов и подберут индивидуальное лечение в случае обнаружения заболевания
- При необходимости может быть проведено экстренное обследование
- Записаться на УЗИ в МЕДСИ просто — нужно позвонить по телефону 8 (495) 7-800-500
Жидкостные образования забрюшинного пространства: диагностика и лечение
© А. В. Антонов
Цель исследования: лекция посвящена диагностике и лечению жидкостных образований органов забрюшинного пространства. Описаны методы дифференциальной диагностики объемных образований почек, печени, поджелудочной железы. Особое внимание уделено кистам почки — наиболее часто встречающимся жидкостным образованиям органов забрюшинного пространства. Подробно описано значение и возможности таких методов диагностики, как УЗИ, КT и MPT. Приведены показания и противопоказания к основным методам лечения кист почек — пункции кисты, склеротерапии, эндовидеохирургическим операциям. Представлен алгоритм диагностики и лечения кистозных образований почки.
Ключевые слова: киста почки; эндовидеохирургия в урологии; жидкостные образования забрюшинного пространства.
С появлением ультразвукового исследования (УЗИ), компьютерной томографии (КТ) и магнитно-резонансной томографии (МРТ) стала реальностью диагностика многих заболеваний на ранних стадиях до появления первых симптомов. Особенно ярко это проявилось у больных с объемными новообразованиями. Органы забрюшинного пространства и верхних отделов брюшной полости тесно связаны между собой не только морфологически, но и функционально. Некоторые из них расположены и в одной, и в другой областях одновременно. Жидкостные образования этих локализаций обладают рядом общих признаков (схожесть с онкологическими заболеваниями, медленный рост, длительное бессимптомное течение, соприкосновение с несколькими органами и др.), затрудняющих дифференциальную диагностику. Несмотря на похожую клиническую картину и морфологическое сходство, принципы лечения кист различных органов разные, поэтому до начала лечения необходимо выяснить происхождение новообразования и его точную органотопию.
Из кист органов забрюшинного пространства и верхних отделов брюшной полости наиболее часто встречаются кисты почек. Они занимают первое место не только по частоте, но и по многообразию форм. Реже встречаются кисты надпочечников, брыжейки, печени, еще реже — селезенки.
Существует несколько классификаций кист, построенных на учете различных признаков. Выделяют кисты паразитарные и непаразитарные, врожденные и приобретенные, истинные и ложные. К истинным кистам относят образования, имеющие эпителиальную выстилку — врожденные, ретенционные, паразитарные, а к ложным — появившиеся после деструкции тканей полости, стенка которых является грануляционной тканью.
Кисты рассматриваемой локализации часто бессимптомны. Среди клинических проявлений кист наиболее характерны боль, пальпируемое образование, реже недостаточность функции исходного или соседнего органа. Боль чаще соответствует проекции органа, носит тупой, ноющий, распирающий характер, усиливается при резких движениях. Пальпируемое образование обычно определяется при кистах большого размера.
Осложнения кист делят на две группы: связанные с патологическим процессом в самой кисте (нагноение, разрыв, кровоизлияние) и со сдавлением окружающих органов (обструкция мочевыводящих путей, кишечная непроходимость, механическая желтуха, эндокринные нарушения). Нагноение кисты сопровождается симптомами острого воспалительного процесса соответствующего органа. Наиболее часто нагнаиваются кисты поджелудочной железы — в 20 % случаев. Что же касается кист почек, то они нагнаиваются относительно редко — только в 2 % случаев. Для кист поджелудочной железы характерны такие грозные осложнения, как кровотечение и перфорация. Чаще всего они перфорируют в брюшную полость с развитием перитонита различной степени тяжести. Разрывы кист почек редки и проявляются резкой острой болью в пояснице и подреберье, иногда гематурией и паранефральной гематомой. Озлокачествление кист обычно не имеет определенных клинических признаков и верифицируется гистологически при биопсии или во время операции.
Кисты непочечного происхождения
Кисты надпочечников — относительно редкая патология. Различают истинные и ложные кисты (псевдокисты). УЗИ играет ведущую роль в диагностике этих кист в связи с доступностью исследования, однако КТ обладает преимуществами в определении плотности содержимого кисты, выявления капсулы, геморрагического содержимого, обнаружении кальцификатов. В кистозном пунктате содержится кортизол или холестерол. После пункции кисты надпочечника высока вероятность ее рецидива, поэтому наличие кисты диаметром более 4 см является показанием к операции.
Кисты печени бывают непаразитарные и паразитарные. В свою очередь, среди непаразитарных кист печени Б. В. Петровский в 1972 г. выделил поликистоз печени с поражением других органов и без такового, истинные кисты (простые, многокамерные, дермоидные, ретенционные), воспалительные (травматические и воспалительные), околопеченочные и кисты связок.
Истинные кисты — результат окклюзии желчных протоков, ложные развиваются после травм печени. Поликистоз печени — это наследственное заболевание, может сочетаться с поликистозом почек и поджелудочной железы. Поликистоз печени не уменьшает продолжительность жизни, при сочетанном поликистозе печени и почек прогноз определяется тяжестью поражения почек.
Паразитарные кисты печени бывают двух видов: гидатидный эхинококкоз и альвеококкоз. Гидатидный эхинококкоз пузырный, однокамерный, составляет, по разным источникам, 53–85 % от всех паразитарных кист печени. Возбудителем эхинококкоза служит личинка Echinococcus granulosis. Возбудителем альвеококкоза является Echinococcus multilocularis. Для альвеококкоза характерно экзогенное размножение пузырьков путем почкования, прорастание в соседние органы, возможность метастазирования в легкие.
Диагностика кист печени базируется на УЗИ, КТ и сканировании печени с изотопами золота и технеция. Кисты печени долгое время остаются бессимптомными и их обнаруживают случайно. При больших размерах кист (более 6 см в диаметре) возможны дискомфорт в правом подреберье, чувство тяжести и тупая, ноющая боль, усиливающаяся при движении, тошнота, отрыжка, изжога.
Жидкостные образования поджелудочной железы. К таковым относят цистаденому и цистаденокарциному, являющихся истинными опухолями, истинную и дисонтогенетическую (аномалия развития) кисты, ретенционную кисту (локальное расширение протока в результате хронического панкреатита), эхинококковую кисту и псевдокисту. В отличие от кист печени, почек, селезенки бессимптомными панкреатические кисты бывают крайне редко.
Клинически наиболее значимой для уролога является псевдокиста, клиническая симптоматика которой схожа с таковой при гнойных процессах в забрюшинном пространстве. Псевдокиста формируется в результате острого панкреатита, реже из-за травмы. Ее стенка не выстилается эпителием, а полость заполнена жидкостью, значительную часть которой составляет сок поджелудочной железы. Объем такой кисты может достигать от 1 до 2 литров. Псевдокисты могут пропотевать через ткани, описаны также случаи их обнаружения в средостении и даже в мошонке. Органоспецифичным признаком для псевдокист поджелудочной железы является наличие в пунктате большого количества амилазы. При УЗИ она представляет собой эхонегативную полость с включениями.
Кисты селезенки чаще бывают эхинококковыми однокамерными, встречается у взрослых в возрасте 20–50 лет, у мужчин в 4 раза реже. Они похожи на типичное полостное образование, трудноотличимое от непаразитарной кисты, достигает размеров до 6–10 литров. Непаразитарные кисты составляют 0,5–2 %.
Кисты брыжейки кишечника являются редкими аномалиями, чаще встречающимися у женщин в возрасте от 20 до 50 лет и локализующимися на участке 1–1,5 м от связки Трейтца, реже в брыжейке толстой кишки. Эти кисты в основном доброкачественные. Ложные кисты могут быть результатом травмы с формированием забрюшинной гематомы. Злокачественные образования возникают вблизи свода брыжейки. Клинические симптомы при кистах брызжейки отсутствуют или незначительны, и чаще всего киста обнаруживается случайно во время различных обследований или операций. Единственным проявлением их наличия может быть выявление безболезненного образования при пальпации.
Кисты почек
Кисты почки — это жидкостные образования, расположенные под собственной капсулой почки. Кисты почек могут быть врожденными и приобретенными. Они занимают первое место среди всех пороков развития почек, обусловленны как генетическими заболеваниями, так и факторами, нарушающими внутриутробное развитие плода в период от 32 до 50 суток после зачатия.
Существует множество различных классификаций кистозных образований почек, которые подробно описаны в литературе, поэтому нет необходимости останавливаться на всех. Единственной классификацией, которую представляется целесообразным упомянуть в данной лекции, является классификация M. A. Bosniak, предложенная в 1986 году. Эта классификация схематична, не учитывает клинических данных, но применяется при описании КТ. Согласно ей кисты делятся на 4 группы: I — типичная однокамерная простая киста почки, II — сложная или осложненная киста (наличие нескольких камер, перегородок), III — обызвествление в стенках, наличие перегородок и более плотных стенок, накопление контрастного вещества в кисте после внутривенного контрастирования более чем на 20 ед.Н по сравнению с негативными сканами, IV — злокачественные образования, интенсивно накапливающие контраст.
Мультикистозная почка формируется при нарушении эмбриогенеза на 4–6-й неделе и характеризуется тотальным замещением почечной паренхимы кистами разных размеров. В клинике мы встречаемся с односторонним пороком развития. Двухстороннее поражение несовместимо с жизнью.
Кортикальный мультикистоз — двухсторонний процесс, характеризующийся образованием в субкортикальной зоне множества мелких кист и уменьшением размеров почек. При возникшей на ранних стадиях эмбриогенеза инфравезикальной обструкции происходит повышение давления в лоханке, приводящее к появлению лоханочно-почечных рефлюксов. В результате происходит повреждение ампул собирательных канальцев и первичных нефронов. Выраженность кистозных повреждений зависит от степени обструкции и срока ее возникновения. При инфравезикальной обструкции на поздних стадиях эмбриогенеза развивается гидронефроз.
Мультилокулярная киста характеризуется замещением тонкостенными, многокамерными кистами участка почки, чаще одного из полюсов. Кистозно-измененный участок отделен от паренхимы собственной капсулой, состоит из мелких камер, заполненных серозной или геморрагической жидкостью. Если повредить капсулу кисты и не удалить ее радикально, неизбежен рецидив с поражением всей почки. Мультилокулярные кисты часто малигнизируются. По некоторым классификациям мультилокулярная киста почки отнесена к нефробластческой опухоли и обозначается термином мультилокулярная кистозная нефрома.
Поликистоз почек представляет собой двухстороннее замещение почечной паренхимы множественными кистами различных размеров и является следствием нарушения эмбриогенеза на стадии слияния экскреторного и секреторного аппаратов почки. Поликистоз бывает тотальный, кортикальный и медуллярный. При тотальном поликистозе различают мелкокистозные и крупнокистозные почки. 95 % детей с мелкокистозной почкой умирают в течение первого года жизни.
При крупнокистозной почке кисты от нескольких миллиметров до нескольких сантиметров, почки увеличены, поверхность бугристая, в 40 % случаев сочетается с поликистозом печени, в 10 % случаев — поджелудочной железы, в 5 % — селезенки. Выраженность процесса в разных органах может быть различной.
Парапельвикальная киста — это множественное кистозное образование, от нескольких миллиметров до 5–6 см, находящееся в синусе почки в тесном соприкосновении с сосудистой ножкой и лоханкой. Парапельвикальные кисты представляют собой резко расширенные лимфатические сосуды. При высоком внутрикистозном давлении киста может сдавливать сосуды и мочеточник, при низком — повторяет форму чашечнолоханочной системы почки и мочеточника. При вскрытии всех парапельвикальных кист рецидивов не встречается. В противном случае оставшиеся кисты быстро растут и занимают место иссеченных.
Не следует путать парапельвикальные кисты с простой кистой почки, расположенной в почечном синусе. Они имеют разное происхождение, разный внешний вид при непосредственной визуализации, хотя очень похожи при УЗИ и КТ. Для ликвидации парапельвикальной кисты достаточно рассечь ее стенку, а для простой кисты почки необходимо широкое иссечение образования, чтобы края оставшейся полости не сомкнулись и не срослись после операции.
Дермоидная киста — очень редкая врожденная аномалия, полость заполняют сальные массы, жир, волосы, иногда зубы.
Лоханочная и чашечковая кисты являются отшнурованной частью полостной системы почки, выстланы уротелием, ее стенкой является атрофированная почечная паренхима.
Губчатая почка представляет собой двустороннее поражение почек и встречается преимущественно у мужчин. Кистами от одного до нескольких миллиметров поражаются почечные пирамиды. В кортикальном слое кисты отсутствуют и снаружи почка имеет нормальный вид. Функция губчатых почек сохраняется.
Простая киста почки диагностируется у 3 % всех взрослых урологических больных, а на вскрытии, по данным разных авторов, они выявляются у 5,8–50 % людей старше 50 лет. Простая киста почки представляет собой одиночное овоидное образование с тонкой стенкой, диаметром от нескольких миллиметров до десятков сантиметров (чаще от 4 до 7 см), выстланное эпителием, с серозным, реже геморрагическим содержимым. Эти образования медленно растут, редко вызывают нарушения урои гемодинамики и чаще обнаруживаются случайно при обследовании больного по поводу другого заболевания.
Простые кисты бывают врожденными или образуются в результате нарушений уродинамики верхних мочевых путей и почечной гемодинамики. Наиболее часто кисты встречаются при ДГПЖ (30,6 %), пиелонефрите (23,4 %), уролитиазе (13,1 %) (в скобках дана частота образования кист). Эмбриональный механизм развития связан с дефектным соединением метанефронов с экскреторной тканью мезонефральных протоков. Органоспецифичным признаком является наличие в простой кисте почки креатинина, мочевины и эритропоэтинов.
Симптоматика и диагностика кист почек
По данным различных авторов, бессимптомное течение кист почек отмечено в 42,4–70 % случаев. Из клинических проявлений встречаются боль, гематурия, пальпация опухоли и артериальная гипертензия.
Боль в проекции почки чаще тупая, усиливается при физической нагрузке, иррадиация, характерная для урологической патологии, однако при сдавлении соседних органов может меняться. Гематурия вызвана разрывом форникальных вен вследствие нарушения венозного оттока или резкого изменения внутрилоханочного давления при кистах, нарушающих отток мочи из почки. Пальпаторно можно определить только крупные кисты и поликистоз почек.
Артериальная гипертензия возникает при сдавлении надпочечника или вследствие активации выработки ренина при натяжении магистральных сосудов почки, если крупная киста своим весом тянет почку вниз (киста 10 см весит около 0,5 кг) или при непосредственном сдавлении сосудов кистой.
Сдавление кистой паренхимы приводит к гипоксии почки и повышению выработки не только ренина, но и эритропоэтина, что объясняет повышение количества эритроцитов и гемоглобина крови. Необходимо помнить, что этот симптом встречается при опухоли почки.
Из осложнений наиболее значимы следующие: нагноение кисты — 2 %, кровоизлияние в кисту — менее 1 % и разрыв кисты — 0,5 % (чаще травматический).
Методы диагностики кист почек
Обзорная и экскреторная урография не являются методами диагностики кист почек, поскольку не позволяют провести дифференциальную диагностику с опухолью и выяснить взаиморасположение кисты с почечными сосудами и элементами полостной системы, что необходимо для планирования операции.
Ультразвуковое исследование (УЗИ) почек — быстрый, экономичный, доступный, неинвазивный метод, позволяющий получить структурную картину почки и находящихся в ней новообразований. УЗИ — основа дифференциальной диагностики кисты с опухолью, оно позволяет определить характер новообразования: жидкостное оно или тканевое, однородное или содержащее включения. Для опухоли характерны пристеночные образования внутри кисты, неровность, нечеткость контура, наличие кровотока внутри новообразования. Неоднородность содержимого бывает при геморрагическом или гнойном характере жидкости, наличии фибрина. Кроме того, ультразвуковая техника позволяет осуществлять контроль над выполнением пункционных вмешательств.
Компьютерная томография (КТ) является высокоинформативным и неинвазивным методом диагностики, позволяющим определить точную локализацию новообразования и его взаимоотношение с соседними органами и крупными сосудами, что очень важно для определения тактики лечения и выбора оперативного доступа. По данным КТ оценивают контур кисты, ее размеры, однородность содержимого, толщину капсулы, наличие нескольких кистозных камер, тканевых включений, а также проводится денситометрия содержимого.
При внутривенном введении контрастного вещества определяется не только функциональное состояние почки, но и степень накопления контраста в кисте, наличие сообщения кисты с полостной системой. КТ с контрастированием позволяет в большинстве случаев дифференцировать кисты от других образований почки. По мнению ряда авторов, КТ является «золотым стандартом» при обследовании больных кистозными образованиями почек. Однако в 8–10 % случаев КТ неэффективна в дифференцировании геморрагических и нагноившихся кист от кистозных опухолей, реже — от абсцессов.
Магнитно-резонансная томография (МРТ) — неинвазивный метод диагностики с высокой разрешающей способностью и возможностью получения изображения в любых проекциях. МРТ позволяет определить малые (менее 1,5 см) опухоли почки, хотя дифференциальная диагностика между доброкачественными и злокачественными образованиями такого размера остае тся весьма сложной. Простые кисты почек менее 2–3 мм выявляются без каких-либо затруднений. Наибольшую помощь МРТ оказывает при кистах с неоднородным содержимым, утолщенными стенками, дополнительными пристеночными образованиями или перегородками.
Характерными признаками малигнизации кисты почки, выявляемыми при УЗИ, КТ и МРТ, являются толщина стенки кисты более 2 мм, неровность или нечеткость ее контура, неоднородность содержимого в полости кисты, наличие в нем тканевых включений, кальцификаты в стенке кисты.
Сравнивая возможности УЗИ, КТ и МРТ в диагностике объемных образований почек, необходимо отметить, что два последних метода являются предпочтительными. Они имеют более высокую чувствительность, большие возможности для оценки взаимосвязи кисты с соседними органами и визуализации сосудистых структур и лимфатических узлов в области ворот почки, их результаты в меньшей степени зависят от человеческого фактора. При этом КТ и МРТ по сравнению с УЗИ дороже и поэтому менее доступны. Недостатком УЗИ и МРТ является невозможность оценки функционального состоянии почки. КТ, в отличие от УЗИ и МРТ, предполагает лучевую нагрузку для пациента.
Сцинтиграфия почек — способ исследования функционального и анатомического состояния органа с помощью радиоактивных изотопов. Лучевая нагрузка на пациента по сравнению с рентгенологическими методами в десятки раз ниже. Статическая сцинтиграфия позволяет определить наличие «холодного» или «горячего» очага в проекции почки, способствуя дифференцировке симптомов опухоли и кисты, выяснить количество функционирующей паренхимы почки, что очень важно при решении вопроса о выполнении нефрэктомии. Динамическая сцинтиграфия позволяет оценить раздельную секреторную и экскреторную функцию почек.
Исследование пунктата кисты. Методы лучевой диагностики дают достаточно много информации относительно локализации и структуры патологического процесса, однако иногда они не в состоянии определить органопринадлежность и доброкачественность жидкостного новообразования. В таком случае показана диагностическая пункция для лабораторного исследования пунк тата. Для выявления малигнизации кисты выполняют цитологическое исследование кистозного содержимого. Для определения органопринадлежности кисты существуют специ фические маркеры, определяемые при биохимическом исследовании. Так, для кисты почки характерными являются наличие эритропоэтина, мочевины и креатинина, для псевдо кист поджелудочной железы — амилазы, а для кист печени — билирубина. С помощью микроскопии можно определить наличие и активность воспалительного процесса в кисте или содержание в ней крови. В качестве окончательного метода диаг ностики, переходящего в оперативное пособие, выступает эндовидеохирургическая (ЭВХ) операция — лапароскопия или люмбоскопия.
Дифференциальная диагностика кист почек
При дифференциальной диагностике в первую очередь необходимо выяснить органопринадлежность кисты, потом дифференцировать ее с опухолью, гнойными процессами, туберкулезом, гидронефрозом и другими заболеваниями. Основные сложности встречаются при больших жидкостных образованиях, особенно если они контактируют с несколькими органами, а также при наличии в них нескольких камер, неоднородности содержимого, тканевых включениях, неровности и нечеткости контура при УЗИ и КТ.
Нередко возникают трудности при дифференциальной диагностике рецидивных простой и чашечковой кист почек. Данная информация весьма важна для планировании оперативного вмешательства: при рецидивной простой кисте достаточно просто иссечь ее стенку, тогда как при чашечковой необходимо ликвидировать сообщение кисты с полостной системой почки. В диагностике определенную помощь может оказать денситометрия содержимого кисты, проводимая после контрастного усиления при КТ.
Трудно дифференцировать жидкостную структуру в области почечного синуса, где может быть парапельвикальная, простая, лоханочная киста и гидронефроз. Во время операции парапельвикальные кисты выглядят как гроздь винограда золотисто-желтого цвета, стенка кисты очень тонкая. Простые кисты имеют стенку толще и синеватую окраску. Лоханочные кисты обычно заключены в непрозрачную капсулу толщиной до 2–3 мм.
Однородные опухоли почки (аденома, липома, саркома) могут иметь сходные с кистой ультразвуковые характеристики. Абсцессы и гематомы в редких случаях могут выглядеть как однородные жидкостные образования, однако чаще в их полости обнаруживаются включения, которые представляют собой сгустки крови различной степени организации или фибринозные массы.
Применение таких современных методов визуализации, как УЗИ и КТ, не всегда позволяют определить органопринадлежность полости и ее распространенность. Диагностическая пункция дает дополнительную возможность установить характер патологического процесса на предоперационном этапе и дренировать полость, что является уже лечебной процедурой. Если это дренирование и не приведет к излечению, то, по крайней мере, даст время на подготовку к полноценной операции.
Лечение кистозных заболеваний почек
Во взрослой урологической практике чаще встречаются простые и парапельвикальные, реже мультилокулярные и чашечковые (изолированный гидрокаликоз) кисты почек, а также поликистоз почек.
При случайном обнаружении кистозного заболевания почки существует несколько вариантов действий. Самый благоприятный вариант — динамическое наблюдение, оно осуществляется в тех случаях, когда лечение кист не показано. Частота осмотров и УЗИ — 1 раз в 6 месяцев.
Наиболее распространенные методы лечения кистозных новообразований почек — пункция кисты со склеротерапией и оперативное вмешательство.
Показанием к лечению кист почек является наличие клинических проявлений заболевания (боль, гематурия, пальпируемое образование и др.) при кистах любых размеров и локализации, а при бессимптомном течении заболевания — размер кисты более 6 см, деформация полостной системы почки, быстрорастущие кисты, нарушение оттока мочи из почки и подозрение на малигнизацию кисты. Принципиальная разница в патогенетическом смысле операции и склеротерапии заключается в том, что во время операции замкнутая полость кисты полностью ликвидируется, а жидкость, которая может секретироваться оставшимся эндотелием, резорбируется забрюшинной клетчаткой. При пункции со склеротерапией стенки кисты спадаются, но замкнутая полость остается. Под действием склерозантов некротизируется эндотелий кисты, жидкость перестает вырабатываться, стенки кисты слипаются, срастаются, полость кисты исчезает.
Общепризнано, что показанием к пункции со склеротерапией являются простые однокамерные кисты почек размером до 6 см с однородным содержимым и толщиной стенки до 1 мм. Предполагаемый пункционный канал до кисты должен проходить экстраренально и экстраперитонеально. Относительным показанием к пункции можно считать особо крупные кисты при поликистозе почек, хотя это заведомо паллиативное вмешательство.
Абсолютным противопоказанием к склеротерапии следует считать подозрение на малигнизацию кисты (наличие тканевых включений, неровность и нечеткость контура, неоднородность содержимого кисты), сообщение кисты с полостной системой, парапельвикальные кисты, многокамерные кисты.
Относительными противопоказаниями к пункции являются размер кисты более 6 см, толщина стенки более 2 мм и наличие 2–3 крупных камер. Кисты в этих случаях часто рецидивируют. Однако сама манипуляция настолько малоинвазивна, что у соматически отягощенных больных оправдано выполнение нескольких пункций для ликвидации крупной кисты.
При всех кистозных заболеваниях почек и других жидкостных новообразованиях забрюшинного пространства и верхних отделов брюшной полости, которые не подлежат пункционному лечению, необходимо выполнять операцию. Она показана и в сомнительных случаях, например, если не установлена органопринадлежность кисты или не исключена онкопатология.
Эндовидеохирургическое (ЭВХ) вмешательство позволяет выполнить полноценное радикальное лечение не только любых кист почек, но и большинства кистозных образований забрюшинного пространства и верхних отделов брюшной полости. Исключением можно считать псевдокисты поджелудочной железы, которые требуют анастомоза полости кисты с просветом кишки; при этом открытая операция предпочтительнее. В остальных случаях открытые операции должны применяться только как исключение, поскольку травма, наносимая больному при открытом доступе, не адекватна цели операции. Другими словами, при открытой операции вред, наносимый больному, превышает пользу от нее.
ЭВХ-операции по поводу почечных кист наиболее просты по сравнению с другими ЭВХоперациями на почках и выполнимы при кистах любой локализации. При адекватном иссечении стенки кисты рецидивирования не наблюдается. Послеоперационный период протекает значительно легче, чем после открытых операций: не требуется применение наркотических анальгетиков, через несколько часов после операции больные самостоятельно встают и способны к свободному передвижению. Восстановление трудоспособности после операций по поводу неосложненной кисты почки наступает через 4–5 дней.
ЭВХ-операция по поводу простых кист почек по своей сути тождественна традиционному открытому вмешательству, отличие составляют только средства достижения цели. После обнаружения кисты ее свободная стенка выделяется и иссекается по возможности до границы с паренхимой почки. Если нет возможности полностью иссечь свободную стенку кисты, необходимо создать максимально широкое сообщение остаточной полости кисты с забрюшинной клетчаткой. При этом необходимо, чтобы свободные стенки кисты не соприкасались и не смогли срастись после операции, что является профилактикой рецидива. Эндотелий оставшейся полости ничем не обрабатывается.
Операции при поликистозе почек являются заведомо паллиативными манипуляциями. Необходимо вскрыть крупные, нагноившиеся и геморрагические кисты с минимальным повреждением паренхимы почки. До операции по данным КТ необходимо определить, какие кисты подлежат вскрытию, и установить их точную локализацию. При поликистозе удобен комбинированный доступ — кисты по передней поверхности вскрываются трансперитонеально, а по задней — ретроперитонеально. Это позволяет уменьшить операционную травму почки и минимизировать повреждение коллатеральных сосудов.
Операции по поводу мультилокулярной кисты заключаются в резекции почки в пределах здоровой ткани, как при опухоли. По нашим наблюдениям, иссечение кистозных полостей в пределах общей капсулы приводит не просто к рецидиву, а к прорастанию кистами всего объема почки, причем происходит это приблизительно за 1 год. Кроме того, в пределах мультилокулярной кисты часто встречается светлоклеточный рак почки.
Операция по поводу чашечковой кисты почки по сути является резекцией почки. При этом иссекается склерозированная и атрофичная паренхима, неизбежно умеренное кровотечение, которое легко останавливается биполярным коагулятором. Часто выявляется связь кисты с полостной системой почки. В этих случаях необходимо устранение этого сообщения, в противном случае гарантирован мочевой затек.
Алгоритм диагностических и лечебных мероприятий при кистозных заболеваниях почек (рис. 1). В случае выявления при УЗИ жидкостного образования, расположенного внутри почки или рядом с ней, которое не является частью полостной системы, размером менее 4 см, без включений, с невидимой при УЗИ капсулой, без клинических и лабораторных проявлений дальнейшие диагностические и лечебные мероприятия не показаны. Необходимо рекомендовать пациенту выполнять контрольное УЗИ 1 раз в 6 месяцев.
Если описанная выше простая киста почки растет или у больного имеются жалобы на боль, гематурию, повышение артериального давления, пальпируемую опухоль — показано лечение кисты. При наличии всех следующих признаков кисты: размер от 5 до 6 см, капсула при УЗИ не видна, однородное содержимое, однокамерная, включений нет, локализация кисты такова, что предполагаемый пункционный канал проходит не трансренально и не трансабдоминально, и киста не парапельвикальная — показана пункция кисты со склеротерапией. Если при пункции кистозная жидкость окрашена кровью — склеротерапия противопоказана, больной подлежит оперативному лечению. Противопоказанием к склеротерапии является также подозрение на сообщение кисты с полостной системой почки. Если киста с перечисленными характеристиками достигла размеров более 6 см, предпочтительнее выполнить эндовидеохирургическое иссечение кисты, поскольку после пункции крупные кисты часто рецидивируют или для их полного излечения необходимо выполнить несколько повторных пункций со склеротерапией.
Если у жидкостного образования размером более 5 см выявлен хотя бы один из следующих признаков: толщина капсулы более 1 мм (видна при УЗИ), неоднородное содержимое, 2–3-камерная, рецидивная, локализация кисты такова, что предполагаемый пункционный канал проходит трансренально или трансабдоминально или киста парапельвикальная — показана ЭВХ-операция (иссечение кисты, резекция почки или нефрэктомия в зависимости от характеристик кисты и функции почки). В случае невозможности провести полноценное оперативное ЭВХ-пособие показана конверсия доступа и выполнение операции традиционным открытым способом. В любом случае, при кистах почек начинать операцию следует эндовидеохирургически. В подавляющем большинстве случаев этот метод позволяет выполнить полноценное оперативное лечение кисты в полном объеме, но с минимальной операционной травмой по сравнению с открытой операцией.
Рис. 1. Алгоритм диагностических и лечебных мероприятий при кистозных заболеваниях почек
* ЧЛС — чашечно-лоханочная система почки;
** «для пункции» — такая локализация кисты, при которой предполагаемый пункционный канал проходит не трансренально и не трансабдоминально и киста не парапельвикальная;
*** случайные находки — нефроптоз, камни лоханки, стриктура лоханочно-мочеточникового соустья и другая патология этой
же почки, требующая оперативного лечения вместе с иссечением кисты;
**** ЛМС — лоханочно-мочеточниковое соустье.
Если выявленное по УЗИ жидкостное образование сопровождается клиникой острого гнойного воспаления (паранефрит, абсцесс или карбункул почки), показано пункционное дренирование полости под контролем УЗИ или ЭВХ-операция в зависимости от состояния больного, размеров, локализации и количества полостей.
Если у жидкостного образования размером более 5 см выявлен хотя бы один из следующих признаков: неоднородное содержимое, тканевые включения, неровный и (или) нечеткий контур, многокамерная, точно не установлена органопринадлежность — больному необходимо выполнить КТ с контрастированием. По результатам этого исследования в подавляющем большинстве случаев появится возможность принять решение о проведении дальнейших диагностических или лечебных мероприятий.
В том случае, если при УЗИ, кроме кисты, выявлено расширение полостной системы почки, конкремент или другая сопутствующая кисте патология этой же или контрлатеральной почки — показано выполнение экскреторной урографии или мультиспиральной компьютерной томографии с контрастным усилением (предпочтительнее). Это необходимо сделать, чтобы, во-первых, выявить сопутствующую патологию, которую можно корректировать одновременно с хирургическим лечением кисты и, во-вторых, выяснить, не является ли выявленная киста причиной вторичных изменений почки. Во втором случае иссечение кисты может привести к нормализации урои гемодинамики и восстановлению нормальной работы почки.
Вышепредставленные ультразвуковые характеристики кист позволяют определить диагностическую и лечебную тактику при кистах почки на первом, начальном, этапе для большинства пациентов. Часть первичных больных подлежит диспансерному наблюдению, часть ЭВХ или пункционному лечению. Остальные больные нуждаются в дальнейшем обследовании и переходят на следующий диагностический этап предложенного алгоритма.
Если в результате проведенной КТ или МРТ установлена внепочечная органопринадлежность жидкостного образования, больной передается для дальнейшего лечения хирургу. Если в результате проведенной КТ или МРТ органопринадлежность жидкостного образования не установлена, показана диагностическая пункция с биохимическим исследованием содержимого жидкостного образования. Это позволяет установить точный диагноз простой кисты почки по наличию в пунк тате мочевины, креатинина и эритропоэтина, кисту печени — при обнаружении билирубина и псевдокисту поджелудочной железы — при наличии амилазы. Последнее обстоятельство очень важно, так как при псевдокистах поджелудочной железы операция принципиально отличается от операций при кистах другой органопринадлежности, а попадание содержимого такой кисты в окружающие ткани крайне опасно из-за риска их ферментативного расплавления. Если в результате пункции доказана внепочечная органопринадлежность жидкостного образования, больной передается для дальнейшего лечения хирургу.
Если в результате пункции установлено почечное происхождение кисты, больному показана пункция со склеротерапией или ЭВХ-операция. Выбор метода лечения в зависимости от характеристик кисты обсуждался выше.
Если в результате пункции не удалось установить органопринадлежность кисты (это возможно при кистах надпочечников, брыжейки, селезенки), а также, если после проведения КТ или МРТ остаются сомнения по поводу наличия онкопатологии, органопринадлежности образования, то последним этапом диагностики является диагностическая лапароскопия или люмбоскопия, которая после установления окончательного диагноза переходит в лечебный этап вмешательства.
В случае выявления кист, расположенных в области ворот почки, при наличии сообщения кисты с полостной системой, при мультилокулярной и множественных кистах показано выполнение ЭВХ-операции (иссечение кисты, резекция почки или нефрэктомия в зависимости от характеристик кисты и функции почки). В случае невозможности проведения полноценного оперативного ЭВХпособия показана конверсия доступа и выполнение операции традиционным способом.
КТ и МРТ одному больному делать не следует, поскольку эти методы при жидкостных новообразованиях по своим диагностическим возможностям схожи. Если один из них не позволил установить точный диагноз, с большой вероятностью и другой не даст дополнительной информации. При наличии кист почки и сопутствующей патологии возможно выполнение сочетанной ЭВХ-операции для одновременной ликвидации кисты и выявленного заболевания. Такими заболеваниями могут быть камни почки или мочеточника, нефроптоз, нарушение проходимости пиелоуретерального сегмента.
Liquid tumors of the retroperitoneum: diagnosis and treatment
Antonov A. V.
Summary. The lecture is about diagnosis and treatment of liquid tumors of retroperitoneal organs. Here are described the methods of differential diagnosis of kidney, liver and pancreas neoplasms. Particular attention is given to kidney cysts the most common liquid tumor of retroperitoneum. In details are described the importance and capability of ultrasound, computer tomography and magnetic resonance imaging. Here reports about indications and contraindications for the main treatment methods of kidney cyst — cyst puncture, sclerotherapy, endovideosurgery. The algorithm of the diagnosis and treatment of kidney cysts is presented.
Key words: kidney cyst; urologic endovideosurgery; liquid tumors of the retroperitoneum.
Консервативное лечение в трех случаях пренатально распознанной кисты селезенки с использованием 2D, 3D, многослойной и допплеровской ультрасонографии
Abstract
Обсуждаются этиология, дифференциальная диагностика и стратегии лечения селезенки плода, пораженной кистозным поражением. В современной литературе очень мало сообщений о кисте селезенки, диагностированной антенатально. В нашем исследовании представлены 3 клинических случая, которые были впервые заподозрены из-за анизоэхогенных структур, обнаруженных во время обычного ультразвукового исследования на 27, 31 и 34 неделе беременности.Все 3 случая дополнительно характеризовались отсутствием патологических результатов допплерографии внутри и вокруг поражений и были морфологически уточнены с помощью пренатальной трехмерной ультразвуковой визуализации. Все результаты были подтверждены послеродовым путем. Никаких осложнений, таких как расширение кисты, субкапсулярное кровотечение или острый живот, не развилось, и все 3 кистозных поражения спонтанно регрессировали после рождения.
Ключевые слова: Пренатальная диагностика, Киста селезенки, УЗИ
Введение
У плодов человека селезенка начинает развиваться на 6-7 неделе беременности.Он образуется в результате агрегации ретикулярных мезенхимальных клеток в задней брыжейке желудка. Он участвует в производстве мегакариоцитов и тромбопоэзе [1], но не в эритропоэзе [2]. Селезенку можно определить при ультразвуковом исследовании примерно на 20 неделе беременности (Н 20) [3]. Врожденная киста селезенки обычно диагностируется в более позднем детстве, когда она может вызывать различные трудности (расширение, кровотечение или разрыв капсулы, внезапные абдоминальные нарушения) [4]. В нашем исследовании сообщается о 3 случаях врожденной кисты селезенки, диагностированной ретроспективно.После первого диагностического подозрения во время планового ультразвукового исследования (УЗИ) на 27, 31 и 34 неделях беременности, во всех случаях в диагностические алгоритмы были включены 3D-МРТ-подобные и допплеровские ультразвуковые исследования. Кисты были подтверждены постнатально во всех 3 случаях.
Методы
В период с августа 1999 г. по июль 2007 г. (8-летний период) в нашем отделении пренатального УЗИ было обследовано 7 897 беременностей. Критерии отбора не применялись, и все беременные женщины, направлявшиеся в наше отделение, регулярно проходили скрининг на наличие каких-либо аномалий плода.Ультразвуковое исследование беременностей, описанных в отчетах о случаях, проводилось на Accuvix QX, поставляемом Medison, с использованием абдоминального зонда 2D / 3D / 4D (включая МРТ-подобное 3D XI ™ eXtended Imaging и Multi-Slice View) и / или на Voluson 730 Pro, поставляемый General Electric, с использованием абдоминального зонда 2D / 3D / 4D. Ультразвуковое исследование Power Doppler (PD-US) было выполнено для оценки возможных параметров кровотока в предполагаемых поражениях.
История болезни 1
Матери 30 лет, tercipara, она была направлена на суперконсилиарное УЗИ на 27 + 4 неделе беременности из-за кистозного тела у плода, расположенного в верхнем левом квадранте брюшной полости.Предыдущее УЗИ, проведенное в первом триместре, было отрицательным, как и тройной тест. Во время нашего УЗИ-исследования в селезенке было обнаружено кистозное тело диаметром 25,5 мм (рис.). С помощью МРТ-подобного 3D XI и Multi-Slice View было определено, что это киста селезенки (рис.). Исследование PD-US не выявило никакого потока внутри полости, а характеристики кровотока вокруг поражения не отличались от остальной ткани селезенки. Все остальные сонографические данные были нормальными. Во время следующего обследования на УЗИ на 31-й неделе беременности никаких изменений в размере и характере кисты не наблюдалось.Ребенок родился на 40 неделе беременности (3650 г / 51 см). Ультразвуковое исследование новорожденного подтвердило наличие кисты селезенки диаметром 26 мм. Контрольное ультразвуковое исследование через 3 месяца показало спонтанное уменьшение размера кисты на 10 мм, а через 6 месяцев после родов киста полностью регрессировала.
Киста селезенки на 28 неделе беременности диаметром 25,5 мм.
Трехмерная МРТ-визуализация случая 1. На основе трехмерного сканирования была сделана серия срезов толщиной 5 мм, которые подтвердили расположение кистозного тела в селезенке.
История болезни 2
Матери 39 лет, первородящая, она была госпитализирована на плановый скрининг УЗИ на 31-й неделе беременности. Тройной тест на 16 неделе беременности оказался отрицательным. Предыдущие ультразвуковые исследования патологии не выявили. При нашем осмотре между желудком и селезенкой обнаружено кистозное тело диаметром 9,1 мм (рис.). 3D-исследование подтвердило кисту селезенки. Исследование PD-US не выявило никакого потока внутри полости, а характеристики кровотока вокруг поражения не отличались от остальной ткани селезенки.При контрольном обследовании УЗИ на 38 неделе беременности киста имела идентичный размер и характеристики потока. Ребенок (3880 г / 50 см) родился на 40-й неделе беременности путем кесарева сечения из-за отсутствия прогресса в родах. Ультразвуковое исследование новорожденного подтвердило кисту селезенки. Нормальная структура селезенки без кистозных изменений была обнаружена через 6 месяцев во время ультразвукового обследования.
Киста селезенки на 30 + 5 неделе беременности, расположенная в воротах. Диаметр 9.1 мм. C = киста; S = селезенка.
История болезни 3
Матери 25 лет, первородящая, ее отправили на суперконсилиарное УЗИ из-за положительного тройного теста. Риск синдрома Дауна составлял 1 из 240. УЗИ на 19 неделе беременности не протекало без заметных признаков. При УЗИ на 34 неделе беременности в брюшной полости в районе селезенки обнаружена кистозная структура размером 2,02 × 0,91 см (рис.). Киста селезенки была подтверждена с помощью трехмерной МРТ-визуализации и трехмерного поверхностного режима.Исследование PD-US не выявило никакого потока внутри полости, а характеристики потока вокруг поражения не отличались от остальной ткани селезенки. УЗИ новорожденного подтвердило кисту селезенки. Контрольное УЗИ через 6 месяцев показало нормальную структуру селезенки без кистозных изменений.
Киста селезенки размером 2,02 × 0,91 см, обнаружена на 34 + 0 неделе беременности.
Обсуждение
В трех наших случаях кисты селезенки плода ни в анамнезе, ни при клиническом обследовании не было обнаружено никаких травм, травм или паразитарных заболеваний.Во всех 3 случаях имелась гладкостенная анизоэхогенная киста неизвестного этиопатогенеза.
Литературные записи о пренатальной кисте селезенки
В 1988 году Личман и Миллер стали первыми авторами, которые сообщили о пренатальной УЗИ-диагностированной кисте селезенки [5]. Большинство описанных в литературе кист селезенки были диагностированы между 25 и 35 неделями беременности [6,7]. Селезенку можно обнаружить у плода только после 20-й недели беременности, определяемой по последней менструации [8].УЗИ (с высокочастотными датчиками и высокой разрешающей способностью) значительно расширило возможности пренатальной диагностики. Сегодня у плода можно обнаружить кисты размером в несколько миллиметров, которые раньше было невозможно идентифицировать. Kabra и Bowen [9] сообщают об обнаружении врожденной кисты селезенки диаметром 6 мм, а Lopes et al. [10] диагностировали кисту 10 мм.
Этиопатогенез и классификация кист селезенки
Кисты селезенки можно разделить на 2 типа в зависимости от их эпителия: первичные кисты и вторичные кисты (или псевдоцисты).Капсула первичной кисты образована из клеточного слоя, а вторичные кисты имеют фиброзную капсулу. Первичные кисты включают серозные, сосудистые, мезотелиальные, инфекционные и опухолевые (эпидермальные, дермоидные, гемангиомы и лимфоангиомы) кисты. Вторичные кисты могут быть посттравматического, воспалительного или дегенеративного происхождения. Врожденные кисты составляют 25% всех кист селезенки.
В большинстве случаев этиология кист селезенки неизвестна. С точки зрения развития образование кисты селезенки может происходить по следующим механизмам:
(1)
Инвазия и метаплазия плюрипотентных клеток различного происхождения в паренхиму селезенки во время внутриутробного развития плода.
(2)
Включение клеточного мезотелия в селезенку во время органогенеза.
(3)
Инвагинация эндотелиальных клеток брюшины в развивающуюся селезенку.
(4)
Расширение лимфатических участков.
Типичное УЗИ-изображение врожденной кисты селезенки включает анизоэхогенное образование с гладкой стенкой, расположенное в верхнем левом квадранте брюшной полости.Эпидермоидные кисты отличаются неправильной структурой и утолщенной задней стенкой. Вторичные кисты также могут иметь анизоэхогенную природу, но чаще имеют кальцификаты. Кровотечения или гематомы характеризуются гипоэхогенной структурой.
Дифференциальная диагностика
Дифференциальная диагностика необходима для любой кисты, расположенной в левом верхнем квадранте брюшной полости. Это может быть врожденная киста почки, гидронефроз, кистозная дисплазия почек, непроходимость или удвоение мочевыводящих путей, адреналинные кисты, кисты печени, кисты и псевдокисты поджелудочной железы, кольцевидная поджелудочная железа, мезентериальные кисты, кисты сальника, врожденное удвоение желудка. , атрезия двенадцатиперстной кишки, кисты яичников у женщин и очень редко гидросальпинкс.Кисты в почках могут быть исключены после обнаружения и визуализации почек. Опухоли надпочечников обычно неоднородны. Кисты в желудочно-кишечном тракте чаще располагаются в передней правой части брюшной полости. В настоящее время неизвестно, могут ли конкретные индексы потока, аналогичные допплеровскому исследованию (например, при опухолях яичников у взрослых и некоторых пренатальных аномалиях), надежно и рутинно применяться в пренатальных случаях кистозных поражений, но всегда рекомендуется проводить скрининг на признаки злокачественного характера ( признаки ангионогенеза, нерегулярный кровоток, искривленная форма сосудов, анархическая архитектура сосудов, нерегулярное ветвление, изменения калибра сосудов и / или сопротивления, микроаневризмы, сосудистые озера, артериовенозное шунтирование и т. д.), и необходимы дальнейшие исследования в этой области [11,12,13].
Клиническое лечение
При обнаружении кист селезенки необходимо исследовать другие органы тела (печень, почки, легкие и поджелудочную железу) на наличие кист, чтобы исключить врожденный поликистоз. Впоследствии необходимо наблюдать за пациентом внутриутробно, а за новорожденным — постнатально. Важно наблюдать любые изменения кисты, ее прогрессирование или регресс вплоть до исчезновения.Большинство врожденных кист селезенки протекают бессимптомно с хорошим прогнозом. Обычно кисты регрессируют. В 1995 г. Garel и Hassan [14] первыми описали спонтанный регресс врожденных кист селезенки. Лишь в нескольких тематических исследованиях сообщается о росте кисты и его осложнениях. Растущая киста вызывает сдавление других органов брюшной полости, она может самопроизвольно лопнуть, демонстрировать кровотечение и вызывать внезапные боли в животе. Это причина, по которой пренатально выявленную кисту селезенки необходимо контролировать до ее полного исчезновения.Стратегия ведения рекомендует консервативный подход, а инвазивное решение рекомендуется только в случаях, когда возникают осложнения. В зависимости от серьезности ситуации могут быть выполнены аспирация кист тонкой иглой под контролем УЗИ, лапароскопическая пункция и цистэктомия. В экстренных случаях проводится частичная или полная спленэктомия [9]. Любые инвазивные методы следует применять только в тех случаях, когда киста становится симптоматической.
Выводы
Спонтанная и бессимптомная регрессия доброкачественных кист селезенки — обычная судьба этого порока развития.Однако во всех случаях необходимо проводить тщательный мониторинг из-за редких случаев опасных для жизни осложнений, таких как разрыв кисты и кровотечение.
Консервативное лечение в трех случаях пренатально распознанной кисты селезенки с использованием 2D, 3D, многосрезового и допплеровского ультразвукового исследования
Abstract
Обсуждаются этиология, дифференциальная диагностика и стратегии лечения селезенки плода, пораженной кистозным поражением. В современной литературе очень мало сообщений о кисте селезенки, диагностированной антенатально.В нашем исследовании представлены 3 клинических случая, которые были впервые заподозрены из-за анизоэхогенных структур, обнаруженных во время обычного ультразвукового исследования на 27, 31 и 34 неделе беременности. Все 3 случая дополнительно характеризовались отсутствием патологических результатов допплерографии внутри и вокруг поражений и были морфологически уточнены с помощью пренатальной трехмерной ультразвуковой визуализации. Все результаты были подтверждены послеродовым путем. Никаких осложнений, таких как расширение кисты, субкапсулярное кровотечение или острый живот, не развилось, и все 3 кистозных поражения спонтанно регрессировали после рождения.
Ключевые слова: Пренатальная диагностика, Киста селезенки, УЗИ
Введение
У плодов человека селезенка начинает развиваться на 6-7 неделе беременности. Он образуется в результате агрегации ретикулярных мезенхимальных клеток в задней брыжейке желудка. Он участвует в производстве мегакариоцитов и тромбопоэзе [1], но не в эритропоэзе [2]. Селезенку можно определить при ультразвуковом исследовании примерно на 20 неделе беременности (Н 20) [3].Врожденная киста селезенки обычно диагностируется в более позднем детстве, когда она может вызывать различные трудности (расширение, кровотечение или разрыв капсулы, внезапные абдоминальные нарушения) [4]. В нашем исследовании сообщается о 3 случаях врожденной кисты селезенки, диагностированной ретроспективно. После первого диагностического подозрения во время планового ультразвукового исследования (УЗИ) на 27, 31 и 34 неделях беременности, во всех случаях в диагностические алгоритмы были включены 3D-МРТ-подобные и допплеровские ультразвуковые исследования. Кисты были подтверждены постнатально во всех 3 случаях.
Методы
В период с августа 1999 г. по июль 2007 г. (8-летний период) в нашем отделении пренатального УЗИ было обследовано 7 897 беременностей. Критерии отбора не применялись, и все беременные женщины, направлявшиеся в наше отделение, регулярно проходили скрининг на наличие каких-либо аномалий плода. Ультразвуковое исследование беременностей, описанных в отчетах о случаях, проводилось на Accuvix QX, поставляемом Medison, с использованием абдоминального зонда 2D / 3D / 4D (включая МРТ-подобное 3D XI ™ eXtended Imaging и Multi-Slice View) и / или на Voluson 730 Pro, поставляемый General Electric, с использованием абдоминального зонда 2D / 3D / 4D.Ультразвуковое исследование Power Doppler (PD-US) было выполнено для оценки возможных параметров кровотока в предполагаемых поражениях.
История болезни 1
Матери 30 лет, tercipara, она была направлена на суперконсилиарное УЗИ на 27 + 4 неделе беременности из-за кистозного тела у плода, расположенного в верхнем левом квадранте брюшной полости. Предыдущее УЗИ, проведенное в первом триместре, было отрицательным, как и тройной тест. Во время нашего УЗИ-обследования в селезенке было обнаружено кистозное тело диаметром 25.5 мм (рис.). С помощью МРТ-подобного 3D XI и Multi-Slice View было определено, что это киста селезенки (рис.). Исследование PD-US не выявило никакого потока внутри полости, а характеристики кровотока вокруг поражения не отличались от остальной ткани селезенки. Все остальные сонографические данные были нормальными. Во время следующего обследования на УЗИ на 31-й неделе беременности никаких изменений в размере и характере кисты не наблюдалось. Ребенок родился на 40 неделе беременности (3650 г / 51 см). Ультразвуковое исследование новорожденного подтвердило наличие кисты селезенки диаметром 26 мм.Контрольное ультразвуковое исследование через 3 месяца показало спонтанное уменьшение размера кисты на 10 мм, а через 6 месяцев после родов киста полностью регрессировала.
Киста селезенки на 28 неделе беременности диаметром 25,5 мм.
Трехмерная МРТ-визуализация случая 1. На основе трехмерного сканирования была сделана серия срезов толщиной 5 мм, которые подтвердили расположение кистозного тела в селезенке.
История болезни 2
Матери 39 лет, первородящая, она была госпитализирована на плановый скрининг УЗИ на 31-й неделе беременности.Тройной тест на 16 неделе беременности оказался отрицательным. Предыдущие ультразвуковые исследования патологии не выявили. При нашем осмотре между желудком и селезенкой обнаружено кистозное тело диаметром 9,1 мм (рис.). 3D-исследование подтвердило кисту селезенки. Исследование PD-US не выявило никакого потока внутри полости, а характеристики кровотока вокруг поражения не отличались от остальной ткани селезенки. При контрольном обследовании УЗИ на 38 неделе беременности киста имела идентичный размер и характеристики потока.Ребенок (3880 г / 50 см) родился на 40-й неделе беременности путем кесарева сечения из-за отсутствия прогресса в родах. Ультразвуковое исследование новорожденного подтвердило кисту селезенки. Нормальная структура селезенки без кистозных изменений была обнаружена через 6 месяцев во время ультразвукового обследования.
Киста селезенки на 30 + 5 неделе беременности, расположенная в воротах. Диаметр 9,1 мм. C = киста; S = селезенка.
История болезни 3
Матери 25 лет, первородящая, ее отправили на суперконсилиарное УЗИ из-за положительного тройного теста.Риск синдрома Дауна составлял 1 из 240. УЗИ на 19 неделе беременности не протекало без заметных признаков. При УЗИ на 34 неделе беременности в брюшной полости в районе селезенки обнаружена кистозная структура размером 2,02 × 0,91 см (рис.). Киста селезенки была подтверждена с помощью трехмерной МРТ-визуализации и трехмерного поверхностного режима. Исследование PD-US не выявило никакого потока внутри полости, а характеристики потока вокруг поражения не отличались от остальной ткани селезенки. УЗИ новорожденного подтвердило кисту селезенки.Контрольное УЗИ через 6 месяцев показало нормальную структуру селезенки без кистозных изменений.
Киста селезенки размером 2,02 × 0,91 см, обнаружена на 34 + 0 неделе беременности.
Обсуждение
В трех наших случаях кисты селезенки плода ни в анамнезе, ни при клиническом обследовании не было обнаружено никаких травм, травм или паразитарных заболеваний. Во всех 3 случаях имелась гладкостенная анизоэхогенная киста неизвестного этиопатогенеза.
Литературные записи о пренатальной кисте селезенки
В 1988 году Личман и Миллер стали первыми авторами, которые сообщили о пренатальной УЗИ-диагностированной кисте селезенки [5].Большинство описанных в литературе кист селезенки были диагностированы между 25 и 35 неделями беременности [6,7]. Селезенку можно обнаружить у плода только после 20-й недели беременности, определяемой по последней менструации [8]. УЗИ (с высокочастотными датчиками и высокой разрешающей способностью) значительно расширило возможности пренатальной диагностики. Сегодня у плода можно обнаружить кисты размером в несколько миллиметров, которые раньше было невозможно идентифицировать.Kabra и Bowen [9] сообщают об обнаружении врожденной кисты селезенки диаметром 6 мм, а Lopes et al. [10] диагностировали кисту 10 мм.
Этиопатогенез и классификация кист селезенки
Кисты селезенки можно разделить на 2 типа в зависимости от их эпителия: первичные кисты и вторичные кисты (или псевдоцисты). Капсула первичной кисты образована из клеточного слоя, а вторичные кисты имеют фиброзную капсулу. Первичные кисты включают серозные, сосудистые, мезотелиальные, инфекционные и опухолевые (эпидермальные, дермоидные, гемангиомы и лимфоангиомы) кисты.Вторичные кисты могут быть посттравматического, воспалительного или дегенеративного происхождения. Врожденные кисты составляют 25% всех кист селезенки.
В большинстве случаев этиология кист селезенки неизвестна. С точки зрения развития образование кисты селезенки может происходить по следующим механизмам:
(1)
Инвазия и метаплазия плюрипотентных клеток различного происхождения в паренхиму селезенки во время внутриутробного развития плода.
(2)
Включение клеточного мезотелия в селезенку во время органогенеза.
(3)
Инвагинация эндотелиальных клеток брюшины в развивающуюся селезенку.
(4)
Расширение лимфатических участков.
Типичное УЗИ-изображение врожденной кисты селезенки включает анизоэхогенное образование с гладкой стенкой, расположенное в верхнем левом квадранте брюшной полости. Эпидермоидные кисты отличаются неправильной структурой и утолщенной задней стенкой. Вторичные кисты также могут иметь анизоэхогенную природу, но чаще имеют кальцификаты.Кровотечения или гематомы характеризуются гипоэхогенной структурой.
Дифференциальная диагностика
Дифференциальная диагностика необходима для любой кисты, расположенной в левом верхнем квадранте брюшной полости. Это может быть врожденная киста почки, гидронефроз, кистозная дисплазия почек, непроходимость или удвоение мочевыводящих путей, адреналинные кисты, кисты печени, кисты и псевдокисты поджелудочной железы, кольцевидная поджелудочная железа, мезентериальные кисты, кисты сальника, врожденное удвоение желудка. , атрезия двенадцатиперстной кишки, кисты яичников у женщин и очень редко гидросальпинкс.Кисты в почках могут быть исключены после обнаружения и визуализации почек. Опухоли надпочечников обычно неоднородны. Кисты в желудочно-кишечном тракте чаще располагаются в передней правой части брюшной полости. В настоящее время неизвестно, могут ли конкретные индексы потока, аналогичные допплеровскому исследованию (например, при опухолях яичников у взрослых и некоторых пренатальных аномалиях), надежно и рутинно применяться в пренатальных случаях кистозных поражений, но всегда рекомендуется проводить скрининг на признаки злокачественного характера ( признаки ангионогенеза, нерегулярный кровоток, искривленная форма сосудов, анархическая архитектура сосудов, нерегулярное ветвление, изменения калибра сосудов и / или сопротивления, микроаневризмы, сосудистые озера, артериовенозное шунтирование и т. д.), и необходимы дальнейшие исследования в этой области [11,12,13].
Клиническое лечение
При обнаружении кист селезенки необходимо исследовать другие органы тела (печень, почки, легкие и поджелудочную железу) на наличие кист, чтобы исключить врожденный поликистоз. Впоследствии необходимо наблюдать за пациентом внутриутробно, а за новорожденным — постнатально. Важно наблюдать любые изменения кисты, ее прогрессирование или регресс вплоть до исчезновения.Большинство врожденных кист селезенки протекают бессимптомно с хорошим прогнозом. Обычно кисты регрессируют. В 1995 г. Garel и Hassan [14] первыми описали спонтанный регресс врожденных кист селезенки. Лишь в нескольких тематических исследованиях сообщается о росте кисты и его осложнениях. Растущая киста вызывает сдавление других органов брюшной полости, она может самопроизвольно лопнуть, демонстрировать кровотечение и вызывать внезапные боли в животе. Это причина, по которой пренатально выявленную кисту селезенки необходимо контролировать до ее полного исчезновения.Стратегия ведения рекомендует консервативный подход, а инвазивное решение рекомендуется только в случаях, когда возникают осложнения. В зависимости от серьезности ситуации могут быть выполнены аспирация кист тонкой иглой под контролем УЗИ, лапароскопическая пункция и цистэктомия. В экстренных случаях проводится частичная или полная спленэктомия [9]. Любые инвазивные методы следует применять только в тех случаях, когда киста становится симптоматической.
Выводы
Спонтанная и бессимптомная регрессия доброкачественных кист селезенки — обычная судьба этого порока развития.Однако во всех случаях необходимо проводить тщательный мониторинг из-за редких случаев опасных для жизни осложнений, таких как разрыв кисты и кровотечение.
Произошла ошибка при настройке вашего пользовательского файла cookie
Произошла ошибка при настройке вашего пользовательского файла cookieЭтот сайт использует файлы cookie для повышения производительности. Если ваш браузер не принимает файлы cookie, вы не можете просматривать этот сайт.
Настройка вашего браузера для приема файлов cookie
Существует множество причин, по которым cookie не может быть установлен правильно.Ниже приведены наиболее частые причины:
- В вашем браузере отключены файлы cookie. Вам необходимо сбросить настройки своего браузера, чтобы он принимал файлы cookie, или чтобы спросить вас, хотите ли вы принимать файлы cookie.
- Ваш браузер спрашивает вас, хотите ли вы принимать файлы cookie, и вы отказались. Чтобы принять файлы cookie с этого сайта, нажмите кнопку «Назад» и примите файлы cookie.
- Ваш браузер не поддерживает файлы cookie. Если вы подозреваете это, попробуйте другой браузер.
- Дата на вашем компьютере в прошлом. Если часы вашего компьютера показывают дату до 1 января 1970 г., браузер автоматически забудет файл cookie. Чтобы исправить это, установите правильное время и дату на своем компьютере.
- Вы установили приложение, которое отслеживает или блокирует установку файлов cookie. Вы должны отключить приложение при входе в систему или проконсультироваться с системным администратором.
Почему этому сайту требуются файлы cookie?
Этот сайт использует файлы cookie для повышения производительности, запоминая, что вы вошли в систему, когда переходите со страницы на страницу.Чтобы предоставить доступ без файлов cookie потребует, чтобы сайт создавал новый сеанс для каждой посещаемой страницы, что замедляет работу системы до неприемлемого уровня.
Что сохраняется в файле cookie?
Этот сайт не хранит ничего, кроме автоматически сгенерированного идентификатора сеанса в cookie; никакая другая информация не фиксируется.
Как правило, в файлах cookie может храниться только информация, которую вы предоставляете, или выбор, который вы делаете при посещении веб-сайта.Например, сайт не может определить ваше имя электронной почты, пока вы не введете его. Разрешение веб-сайту создавать файлы cookie не дает этому или любому другому сайту доступа к остальной части вашего компьютера, и только сайт, который создал файл cookie, может его прочитать.
Фетальные и неонатальные кистообразные поражения селезенки
Solbiati L, Bossi MC, Bellotti E, Ravetto C, Montali G (1983) Очаговые поражения в селезенке: сонографические модели и управляемая биопсия.AJR 140: 59–65
PubMed Google Scholar
Manor A, Starinsky R, Garfinkel D, Yona E, Modai D (1984) Ультразвуковые характеристики симптоматической гемангиомы селезенки. J Clin Ultrasound 12: 95–97
PubMed Google Scholar
Combe J, Lorthioir JM, Muenier CH, Pageaut G, Dreyfus A, Millon G, Milleret P (1980) Lymphangiome kystique de la rate. Дж. Шир (Париж) 117: 547–550
Google Scholar
Enzinger FM, Weiss SW (1988) Опухоли лимфатических сосудов. В: Enzinger FM (ред.) Опухоли мягких тканей. Мосби, Сент-Луис, стр. 624
Google Scholar
Blank E, Campbell JR (1973) Эпидермоидные кисты селезенки. Педиатрия 51: 75
PubMed Google Scholar
Todde G, Bagolan P, Fariello G, Malena S, Ferro F, Mosiello G, Alessandri A (1989) Kyste épidermoïde de la rate chez un nouveau-né.Чир Педиатр 30: 172–174
PubMed Google Scholar
Thorne Griscom N, Hargreaves HK, Marshall Z, Schwartz MZ, Reddish JM, Colodny AH (1977). Огромная киста селезенки у новорожденного: сравнение с 10 случаями в более позднем детстве и подростковом возрасте. AJR 129: 889–891
PubMed Google Scholar
Lichman JP, Miller EI (1988) Пренатальная ультразвуковая диагностика кисты селезенки.J Ultrasound Med 7: 637–638
PubMed Google Scholar
Daneman A, Martin DJ (1982) Врожденные эпителиальные кисты селезенки у детей. Педиатр Радиол 12: 119–125
PubMed Google Scholar
Dachman AH, Ros PR, Murari PJ, Olmsted WW, Lichtenstein JE (1986) Непаразитарные кисты селезенки: отчет о 52 случаях с радиолого-патологической корреляцией.AJR 147: 537–542
PubMed Google Scholar
Goldfinger M, Cohen MM, Steinhardt MI, Rothberg R, Rother I (1986) Сонография и чрескожная аспирация эпидермоидной кисты селезенки. J Clin Ultrasound 14: 147–149
PubMed Google Scholar
Salky B, Zimmerman M, Bauer J, Gelernt I, Kreel I (1985) Лапароскопия для окончательного лечения кисты селезенки.Гастроинтест Endosc 31: 213–215
PubMed Google Scholar
Массивная киста селезенки при беременности: клинический случай | BMC Беременность и роды
Кисты селезенки встречаются редко; зарегистрированный уровень заболеваемости составляет 0,07% согласно большой серии случаев из 42 327 аутопсий за 25-летний период [14]. Фаулер [15] и Мартин [16] классифицируют кисты селезенки как кисты типа 1, которые являются первичными (истинными) кистами с эндоцистозным эпителиальным покровом, тогда как кисты типа II являются вторичными (ложными) кистами без эпителиальной выстилки.Истинные кисты можно разделить на паразитарные (обычно Echinococcus granulosus ) и непаразитарные. Morgenstern [17] подразделяет непаразитарные кисты селезенки (NPSC) на неопластические (гемангиома, лимфангиома) и врожденные (эпидермоид, дермоид, энтодермоид). Псевдокисты типа II составляют 80% всех кист селезенки и обычно возникают в результате травмы, кровотечения, абсцесса, дегенерации, воспаления и инфаркта [18,19,20]. Гормональные изменения во время беременности также могут способствовать развитию инфарктов селезенки [1].
С точки зрения демографии преобладают женщины [21]; две трети всех пациентов с кистами селезенки моложе 40 лет [19]. Большинство пациентов либо бессимптомны, либо испытывают незначительные неспецифические симптомы, связанные с массовым воздействием кисты, такие как боль в левой верхней части живота, раннее насыщение, тошнота и рвота [22]. В нашем случае пациентка соответствует типичной демографической группе, и ее позднее проявление длительного вздутия живота с сопутствующим дискомфортом еще раз подчеркивает ее стоический характер и культурное происхождение, поскольку откладывание медицинской помощи не является редкостью для коренного населения Австралии.
Диагностика кист селезенки часто возникает случайно во время УЗИ брюшной полости и может быть дополнительно определена с помощью компьютерной томографии или МРТ в отношении состава кистозной жидкости, морфологии кисты, включая перегородки или кальцификаты, и окружающей ткани [23, 24]. На УЗИ первичные кисты селезенки представляют собой гладкие, четко очерченные и тонкостенные кистозные поражения без внутреннего усиления, тогда как вторичные кисты селезенки проявляются с более толстыми волокнистыми стенками и кальцификациями, подобными яичной скорлупе, с внутренними эхосигналами, связанными с мусором [23].Однако внутренние перегородки и кальцификаты могут также существовать при первичных эпидермоидных кистах селезенки [25]. На МРТ кисты селезенки демонстрируют интенсивность сигнала, равную воде для обоих модальностей T1 и T2 [26]. Таким образом, первичные кисты и псевдокисты селезенки нельзя надежно отличить только на основании рентгенологических данных; гистологическое исследование остается золотым стандартом для установления их этиологии. У беременных женщин, которым требуется обследование органов брюшно-тазовой области, в первую очередь рекомендуются ультразвуковое исследование и МРТ (без контраста); однако КТ можно зарезервировать в качестве альтернативы, поскольку связанное с этим воздействие ионизирующего излучения может быть снижено до уровня (<50 мГр), при котором воздействие на плод, вероятно, будет незначительным при любой беременности [27,28,29].
Кроме того, есть разумная полезность в исследовании опухолевых маркеров до и после операции, так как выстилка эпителия некоторых первичных кист селезенки может продуцировать CA 19.9, CA 125 и CEA [30]. Эта взаимосвязь повышенных онкомаркеров была отмечена в нашем случае с повышенным CA 19,9 и аналогичным образом продемонстрирована в предыдущих случаях в литературе [31,32,33]. Хотя авторы признают хорошо известные ограничения повышенных онкомаркеров во время беременности, определение этих значений в рамках исследовательской работы в этом случае предоставило значимую информацию для общей клинической картины, особенно с учетом того, что команда гинекологов-онкологов была вовлечены в настройку большой недифференцированной массы живота с неясным злокачественным потенциалом.
Описан широкий спектр подходов к лечению кист селезенки у небеременных пациенток, часто в зависимости от возраста пациента, симптомов, характеристик и размера кисты. При бессимптомных небольших кистах (<5 см) рекомендуются неоперационные меры, такие как наблюдение и регулярная серийная визуализация [34]. Однако при кистах селезенки размером более 5 см или симптоматических кистах необходимо хирургическое лечение; испытания других консервативных методов, таких как чрескожная аспирация или склероз (с использованием этанола или тетрациклина), хотя и экономически эффективны с меньшим временем восстановления, часто приводят к рецидиву заболевания и могут осложнять последующие хирургические процедуры [30, 35, 36].
Традиционно золотым стандартом хирургического лечения кист селезенки была открытая полная спленэктомия. Тем не менее, благодаря растущему пониманию гематологических и иммунологических функций селезенки, с тех пор были разработаны методы спасения органов для снижения опасного для жизни риска обширной постспленэктомической инфекции (OPSI) [37, 38]. Следовательно, предоперационная вакцинация против Streptococcus pneumonia , Neisseria meningitides и Haemophilus influenza имеет решающее значение, а также строгий послеоперационный охват антибиотиками при тотальной спленэктомии.Сегодня оптимальные варианты лечения варьируются от фенестрации кисты, марсупиализации и частичной цистэктомии до тотальной цистэктомии с частичной спленэктомией [39,40,41].
Во время беременности в большинстве ранних случаев кисты селезенки выполнялась спленэктомия либо открытая, либо лапароскопическая [1,2,3,4,5]. В более поздние годы в двух отчетах о случаях была предпринята попытка чрескожной аспирации [7, 8]; хотя в обоих случаях роды произошли через естественные родовые пути, оба также привели к повторному скоплению кистозной жидкости и потребовали дальнейшего вмешательства.Rotas et al. [7] выполнили аспирацию у пациента, у которого в первом триместре была диагностирована симптоматическая киста селезенки 17 см, с последующим двухнедельным ультразвуковым сканированием до второго триместра. Вторая кистозная аспирация осложнилась сепсисом и, как следствие, потребовала лапароскопической фенестрации и оментопексии. Аналогичным образом, после консервативного подхода, включающего добавку железа, анальгезию и антибиотики, Mahran et al. [8] выполнили чрескожную аспирацию кисты селезенки 20 см во втором триместре.Однако были осложнения сепсиса и анемии, потребовавшие переливания крови. Повторное скопление кисты было отмечено в третьем триместре, но повторная аспирация не проводилась до шести недель после родов.
С тех пор было зарегистрировано еще пять случаев кисты селезенки во время беременности, из которых четыре с успехом вернулись к традиционным методам тотальной спленэктомии во втором триместре. Dabrowski et al. [9] и Forouzesh et al. [11] описывают удаление кист селезенки размером 10 см и 14 см соответственно с помощью открытой спленэктомии, сообщая о благоприятных неонатальных исходах, отсутствии послеоперационных осложнений и полном исчезновении симптомов пациента (боли, анорексии, лихорадки и полноты).Более того, Majesky et al. [10] и Варбан и др. [12] оба лечили кисты селезенки с помощью лапароскопической спленэктомии, что также привело к отсутствию послеоперационных осложнений и рождению здоровых новорожденных в срок. Последний отчет о клиническом случае, опубликованный Kapp et al. [13] успешно выполнили малоинвазивную органосохраняющую процедуру лапароскопической цистэктомии по поводу первичной эпителиальной кисты селезенки 15 см во время беременности.
В свете этих сообщений о случаях, похоже, не существует четкого консенсуса или каких-либо рекомендаций по лечению кист селезенки во время беременности, поскольку остается баланс между минимально инвазивными подходами к аспирации с риском повторного накопления хирургия по сравнению с органосохраняющими подходами цистэктомии по сравнению с окончательным подходом к тотальной спленэктомии с большим операционным риском и OPSI.Поэтому при консультировании акушерских пациентов по поводу вариантов лечения, помимо общих соображений, касающихся симптомов, размера кисты, интраоперационных и послеоперационных рисков, рекомендуется дополнительное внимание к их беременности, благополучию плода и предпочтение родов через естественные родовые пути или кесарева сечения.
В нашем случае, учитывая, что пациентка находилась во втором триместре на момент обращения, временные меры, такие как серийные асцитические дренажи, обеспечили симптоматическое облегчение, поскольку мы стремились продлить беременность до адекватного срока.Точная этиология повторяющегося накопления асцитической жидкости остается неясной, однако авторы постулируют ее происхождение от кисты селезенки и / или окклюзии печеночной вены из-за скрытого полного тромбоза воротной вены из-за комбинированного компрессионного воздействия кисты селезенки и ее увеличения. беременная матка. Из-за размера опухоли и ее сдавливающего воздействия на окружающие органы ее происхождение оставалось неясным, несмотря на использование нескольких методов визуализации на протяжении всей беременности.Это создало серьезную диагностическую дилемму, которая значительно повлияла на способ и время родов, а также на тип общей хирургической процедуры. В конечном счете, образование селезенки такого размера потребовало открытой тотальной спленэктомии.
Сильные стороны и ограничения
Одним из основных достоинств данного случая является ретроспективный анализ нашего клинического подхода к диагностике и лечению необычно больших образований в брюшной полости во время беременности. Диагноз кисты селезенки оказался очень уникальным и неожиданным открытием для всех вовлеченных врачей, поэтому этот случай служит своего рода напоминанием для акушеров и гинекологов о необходимости рассматривать диагнозы за пределами тазовой области для женщин с необычным вздутием живота.Эта презентация случая не только дополняет ограниченный объем литературы о кистах селезенки во время беременности, но также дает представление об интересном комбинированном случае акушеров и хирургов, в котором хорошо рассмотрены все варианты лечения матери и плода. Авторы советуют с осторожностью обобщать этот редкий отчет о других более распространенных новообразованиях в брюшной полости во время беременности и признают преимущество лечения таких сложных случаев в больнице третичного уровня, где легко доступны различные специальности, диагностические тесты и варианты лечения.
В заключение, хотя эпителиальные кисты селезенки встречаются редко, их следует рассматривать как часть дифференциального диагноза у молодых людей с вздутием живота. Мы ввели в литературу понятие серийных асцитических дренажей для облегчения симптомов у пациенток и продления беременности. Этот случай подчеркивает необходимость визуализации для диагностики кист селезенки и серийного наблюдения за состоянием плода. Кроме того, этот случай подчеркивает важность оказания помощи на третичном уровне и реализации мультидисциплинарного подхода к сложным клиническим случаям, поощряя хорошее общение между пациентом, акушерами и хирургами при изучении всех вариантов лечения и оптимизации исходов для матери и плода.
Доброкачественные и злокачественные поражения селезенки
Инфекция селезенки и воспалительное заболевание
Воспаление и инфекция селезенки проявляются в трех различных формах: генерализованная спленомегалия без различимых очаговых поражений; солитарные поражения; и диффузный, милиарный или макронодулярный узор со спленомегалией или без нее. Генерализованная спленомегалия — это неспецифическая находка, и ее можно обнаружить при различных заболеваниях, включая инфекции и воспалительные заболевания (вставка 105-3).Множественные узелковые поражения селезенки, обычно менее 2 см в диаметре, обычно связаны с небактериальными инфекциями, такими как грибковые и гранулематозные инфекции. Абсцесс может проявляться одиночным поражением. Присутствие газа в очаге поражения, хотя и редко, является патогномоничным для гнойной инфекции.
Box 105-3
Распространенные причины диффузной спленомегалии
Застойная спленомегалия
Портальная гипертензия
-
Инфекционно-воспалительные заболевания
Острые инфекции (например,g., инфекционный мононуклеоз)
Хронические инфекции (например, милиарный туберкулез, малярия)
Саркоидоз
Системная красная волчанка
гипертрофияГемолитические анемии (например, малярия, истинная полицитемия)
Инфильтративная спленомегалия
Лимфомы, лейкемии
9003 932533333Болезни накопления (e.g., болезнь Гоше, амилоидоз)
Новообразования селезенки
Лимфангиоматоз
Гемангиоматоз
Гемангиоматоз
05
Множественные небольшие узелковые поражения селезенки встречаются при самых разных заболеваниях (вставка 105-4). К ним относятся бактериальные, грибковые и протозойные инфекции; гранулематозные заболевания, включая микобактериальные инфекции; и саркоидоз и злокачественные новообразования, такие как лимфома и метастазы.Многие пациенты с множественными узелками селезенки имеют установленный диагноз, например лимфома, метастазы или туберкулез. В этих случаях предполагается, что узелки представляют одно и то же заболевание, и патологическое подтверждение обычно не требуется. Типично поражение нескольких органов, аналогичные изменения наблюдаются в печени и других органах.
Box 105-4
Причины узловых поражений селезенки *
Грибковые микроабсцессы
Бактериальные микроабсцессы
- 84
- 84 Протозойные инфекции
- 8ber Mycobacterium avium Комплексная инфекция
Pneumocystis jiroveci пневмония
Болезнь кошачьих царапин
Саркоидоз
-
Gamph3
Неходжкинская лимфома
Метастазы
Если диагноз не установлен и узелки селезенки являются изолированными, диагноз редко можно поставить только на основании результатов визуализации.Различные причины часто проявляются сходным клиническим образом, как правило, в виде спленомегалии и лихорадки. Анамнез и клинические проявления могут сузить дифференциальный диагноз. Могут быть показаны дополнительные исследования, такие как лабораторные тесты (включая онкомаркеры), тестирование на туберкулез и биопсию костного мозга. При успешном лечении основного заболевания узелки обычно рассасываются или становятся кальцинированными гранулемами.
Характеристики изображения различных узловых состояний неспецифичны и похожи.Узелки часто бывают многочисленными, от нескольких миллиметров до 2 см в диаметре. На УЗИ они гипоэхогенны, на КТ — понижены. Поражения выглядят гипоинтенсивными на T1-взвешенных последовательностях и варьируются от гипоинтенсивных до гиперинтенсивных на T2-взвешенных последовательностях. Узелки обычно не увеличиваются или могут показывать усиление кольца после внутривенного введения контрастного вещества. Зажившие гранулемы выглядят как рассеянные, дискретные, небольшие кальцификаты в нормальной селезенке.
Грибковые абсцессы и микроабсцессы
Грибковые инфекции селезенки обычно возникают у пациентов с ослабленным иммунитетом и нейтропенией.Синдром приобретенного иммунодефицита (СПИД), химиотерапия, иммунодепрессанты и лимфопролиферативные нарушения являются наиболее распространенными факторами риска. Грибковая инфекция печени и селезенки обнаруживается примерно у 7% пациентов с острым лейкозом, и у этих пациентов плохой прогноз. Наиболее часто встречающимся грибковым организмом является Candida , за ним следуют Aspergillus , Cryptococcus и Histoplasma .
Когда реакция хозяина улучшается, очаг кандидоза инкапсулируется и отгораживается нейтрофилами и воспалительными клетками.В результате результаты диагностической визуализации у пациентов с хроническим диссеминированным кандидозом часто бывают нормальными, поскольку характерные изменения становятся видимыми только после восстановления количества нейтрофилов. В аналогичном случае явление исчезновения очаговых поражений печени и селезенки на изображениях во время нейтропении было описано Песталоцци.
Ни один метод визуализации не оказался специфичным и чувствительным у пациентов с подозреваемыми или доказанными грибковыми инфекциями, и только серийная визуализация может выявить поражение гепатоспленки.Независимо от результатов визуализации, для установления окончательного диагноза может потребоваться биопсия, поскольку посев крови часто бывает ложноотрицательным, особенно при инфекциях Candida .
Патология
При гистологическом исследовании эти поражения плохо ограничены и содержат псевдогифы и дрожжевые формы. При микроскопическом исследовании поражения многослойные, состоящие из внешнего кольца фиброза, средней зоны воспалительных клеток и центральной зоны некроза.
Клинические результаты
Наиболее частым проявлением системного кандидоза является стойкая лихорадка, не поддающаяся лечению обычными антибиотиками. Клинический диагноз грибковой инфекции часто затруднен, поскольку имеющиеся симптомы могут быть аналогичны симптомам основного заболевания пациента: лихорадке и спленомегалии. Необъяснимое клиническое ухудшение состояния пациента с ослабленным иммунитетом должно вызвать подозрение на диссеминированную грибковую инфекцию.
Результаты рентгенологического исследования
Ограничением всех методов визуализации при диагностике гепатоспленочной грибковой болезни является невозможность визуализировать грибковые поражения во время нейтропенической фазы.Важно рассмотреть возможность повторения исследований после восстановления числа нейтрофилов, особенно если клиническое подозрение велико и пациент не отвечает на традиционную антибактериальную терапию.
Описаны различные сонографические модели кандидоза печени и селезенки. Множественные маленькие гипоэхогенные узелки являются наиболее частой находкой (рис. 105-11A). Менее распространенный вид можно увидеть на раннем этапе заражения и был описан как появление колеса в колесе (т.е., целевой знак). Это вызвано периферической гипоэхогенной зоной фиброза, первым колесом и вторым эхогенным колесом воспалительных клеток вокруг центрального эхогенного очага, содержащего некроз и грибковые элементы (рис. 105-11B). Этот тип поражения может развиться в очаг поражения, который гистологически соответствует воспалительным клеткам, окруженным фиброзом. На поздних стадиях болезни по мере заживления поражения обычно становятся небольшими и гиперэхогенными с различной степенью задней акустической тени, с кальцификацией или без нее, или они могут исчезнуть.Использование более высокочастотных преобразователей с линейной решеткой значительно улучшает обнаружение повреждений.
Рисунок 105-11
Распространенная инфекция Candida у пациента с острым миелогенным лейкозом.
A. Поперечное ультразвуковое изображение показывает множественные небольшие гипоэхогенные поражения в паренхиме селезенки. B. Сонограмма с высокочастотным (5-12 МГц) линейным датчиком демонстрирует небольшой гипоэхогенный узел с центральным эхогенным очагом. C. КТ с контрастным усилением показывает многочисленные субсантиметровые гиподенсные узловые образования по всей печени и селезенке.
На КТ грибковые микроабсцессы обычно представляют собой гиподенсные узелковые образования размером 5–10 мм (рис. 105-11C). Уровень обнаружения низок (30%) на неконтрастных сканированных изображениях. В артериальной фазе (25–35 секунд) большинство поражений (70%) демонстрируют усиление периферического кольца, которое обычно исчезает в фазе воротной вены. В исследовании Metser и соавторов уровень обнаружения около 90% существенно не отличался между артериальной фазой и фазой воротной вены.Подобные результаты характерны для печени, а иногда и для почек.
Рудольф и его коллеги продемонстрировали другое появление примерно у 30% пациентов. В артериальной фазе эти поражения демонстрировали неоднородное центральное усиление, окруженное двойным целевым кольцом, состоящим из гиподенсированного внутреннего кольца, окруженного сверхплотным внешним кольцом. Со временем контрастное усиление происходит в центробежном направлении, и поражения становятся меньше или исчезают в фазе воротной вены.
МРТ превосходит КТ и УЗИ для выявления гепатоспленочной грибковой болезни, с зарегистрированной чувствительностью 100% и специфичностью 96%. МРТ особенно полезна для отслеживания течения инфекции во время противогрибковой терапии и для оценки реакции на лечение.
На МРТ в острой фазе гепатоспленочной грибковой болезни очаги небольшие, менее 1 см в диаметре. Они слегка гипоинтенсивны на T1-взвешенных изображениях и заметно гиперинтенсивны на T2-взвешенных изображениях.
В подострой фазе поражения имеют тенденцию быть умеренно гиперинтенсивными как на T1-, так и на T2-взвешенных последовательностях. Периферическое кольцо с очень низкой интенсивностью сигнала характерно для всех последовательностей в подострой фазе. Центральная область поражений может демонстрировать усиление после введения гадолиния, при этом периферическое кольцо продолжает иметь низкую интенсивность сигнала, что делает их более заметными. Время перехода от острых поражений к подострым составляет от 2 недель до 3 месяцев.
После успешного противогрибкового лечения поражения размером от 1 до 3 см становятся нерегулярными, а центральная область исчезает.Срок до появления заживших очагов грибка на МРТ составляет от 3 месяцев до более 1 года.
99m Коллоид Tc-серы печень-селезенка, сканирование меченных индием In 111 лейкоцитов и галлия Ga 67 обычно не помогает при обнаружении микроабсцессов, поскольку нормальное поглощение радиоактивного индикатора скрывает небольшие очаги поражения. Результаты сканирования 67 Ga варьируются и могут показывать мультифокальные области повышенного или пониженного поглощения в селезенке.
Сканы ПЭТ с ФДГпоказывают повышенное поглощение 18 F-фтордезоксиглюкозы.Это многообещающий метод визуализации у пациентов с высоким риском инфекций, хотя опубликованные данные о грибковых инфекциях все еще ограничены.
Туберкулез
Mycobacterium tuberculosis — важная проблема здравоохранения в развивающихся странах; в западных странах это обычно наблюдается у пациентов с ослабленным иммунитетом. Туберкулез селезенки обычно возникает на фоне диссеминированной милиарной инфекции и проявляется в виде множественных узелков в селезенке между 0.2 и 1 см в диаметре. Макронодулярное предлежание встречается редко. В случаях диссеминированного милиарного туберкулеза легких поражение селезенки при вскрытии обнаруживается в 80–100% случаев. Сопутствующие данные включают лимфаденопатию и гипоэхогенную картину на УЗИ или центральное низкое ослабление на КТ, что чаще наблюдается у пациентов с инфекцией комплекса Mycobacterium avium (рис. 105-12).
Рисунок 105-12
Диссеминированный милиарный туберкулез.
КТ с контрастным усилением демонстрирует множественные гиподензивные узелки.Обратите внимание на связанную парааортальную и ретрокруральную гиподенопатию ( стрелка ).
Mycobacterium Avium Комплексная инфекция
Mycobacterium avium Комплексные инфекции селезенки, также называемые инфекциями Mycobacterium avium-intracellulare , обычно наблюдаются у пациентов с ослабленным иммунитетом, например, больных СПИДом. На изображениях видна спленомегалия с множественными узелками с низким затуханием (рис. 105-13).Сопутствующие данные, такие как выраженное увеличение печени и селезенки, диффузное утолщение стенки тощей кишки и увеличенные лимфатические узлы, позволяют предположить диссеминированную инфекцию комплекса M. avium . Пациенты с комплексной инфекцией M. avium , как правило, имеют более однородные лимфатические узлы по сравнению с пациентами с туберкулезом, но тканевая диагностика является обязательной.
Рисунок 105-13
Комплексная инфекция Mycobacterium avium .
Продольная сонограмма демонстрирует спленомегалию с множественными небольшими гипоэхогенными узелками.
Pneumocystis Jiroveci Пневмония
Pneumocystis jiroveci пневмония, ранее известная как Pneumocystis carinii пневмония, является наиболее распространенной оппортунистической инфекцией у больных СПИДом. Внелегочное поражение вызывает некротические гранулемы. Инфекция P. jiroveci внутри селезенки часто обнаруживается случайно у пациентов со СПИДом, которым проводится диагностическая визуализация для выявления лихорадки неизвестного происхождения. При успешном лечении узелки могут увеличиваться в размерах и постепенно кальцинироваться в виде ободка или точечной формы.На УЗИ обнаруживается спленомегалия с небольшими гипоэхогенными поражениями с кистозными компонентами или крошечные, сильно отражающие, не затемняющие очаги или кальцинированные гранулемы (рис. 105-14). На КТ узелки гиподенсированы или проявляются кальцинированными гранулемами на более поздних стадиях заболевания.
Рисунок 105-14
Pneumocystis jiroveci pneumonia.
Продольное ультразвуковое изображение демонстрирует множественные точечные кальцификаты после успешного лечения.
Болезнь кошачьих царапин
Болезнь кошачьих царапин — это самостоятельно купируемая инфекция, вызванная Bartonella henselae , которая возникает после того, как домашняя кошка поцарапала ее. Ежегодно в Соединенных Штатах от него страдают около 22 000 человек, большинство из которых составляют дети и подростки. Поражение печени и селезенки встречается редко, но инфекцию B. henselae следует рассматривать у пациента с лихорадкой неизвестного происхождения, болями в животе и множественными гиподенсными поражениями печени и селезенки.
Саркоидоз
Саркоидоз — системное заболевание неизвестной причины, характеризующееся образованием неказеозных эпителиоидных гранулем. Саркоидоз чаще всего поражает легкие и внутригрудные лимфатические узлы, но может поражаться любая система органов. Спленомегалия, обычно связанная с гепатомегалией и абдоминальной лимфаденопатией, обычно легкая и наблюдается у 25-60% этих пациентов. Массивная спленомегалия (> 18 см в длину) наблюдается примерно у 6% пациентов с саркоидозом.
Гистологические признаки поражения печени и селезенки наблюдаются в 77% случаев при вскрытии, но это относительно редкая находка при диагностической визуализации. На снимках узелки селезенки видны у 6–33% пациентов с саркоидом. В одном исследовании эти пациенты обычно имели гепатоспленомегалию, абдоминальную лимфаденопатию и такие симптомы, как боль в животе, утомляемость и недомогание. В том же исследовании узелки не были связаны с прогрессирующим заболеванием легких и не указывали на изменение рентгенографической стадии грудной клетки.Инфрадиафрагмальная аденопатия при саркоидозе имеет тенденцию быть небольшой и дискретной, а ретрокруральная аденопатия у этих пациентов нечасто по сравнению с пациентами с лимфомой. Однако существует значительное совпадение внешнего вида и распределения лимфатических узлов при лимфоме и саркоидозе, и эти критерии не могут быть использованы для точной характеристики заболевания.
Узелки при саркоиде составляют от 0,1 до 3,0 см в диаметре. На УЗИ узелки были описаны от гипоэхогенных до слегка гиперэхогенных или неоднородных.На КТ узелки становятся гиподенсированными относительно соседней нормальной селезенки после внутривенного введения контрастного вещества (рис. 105-15). Узелки гипоинтенсивны на всех МР-последовательностях и лучше всего видны на ранней фазе, на изображениях с усилением гадолиния, Т2-взвешенных изображениях с подавленным жиром или на Т1-взвешенных последовательностях. Узелки не увеличиваются после внутривенного введения контрастного вещества на КТ или МРТ.
Рисунок 105-15
Саркоидоз.
КТ с контрастным усилением, полученная в фазе воротной вены, выявляет многочисленные гиподензивные узелки.
Лимфома или метастатическое заболевание
Лимфомы — обычно мелкоклеточные лимфомы и лимфомы из мантийных клеток и, реже, лимфома Ходжкина — могут проявляться множественными узловыми поражениями селезенки или милиарным паттерном. Узелки, похожие на те, что обнаруживаются при саркоидозе, были описаны у пациентов с лимфомой Ходжкина. Эта находка обычно является частью диссеминированного заболевания, включая лимфаденопатию. Изолированная лимфома селезенки встречается редко.
Метастатическое поражение селезенки может проявляться в виде одиночных или множественных узелков, редко по милиарному типу.Обычно это происходит у пациентов с запущенным заболеванием и широко распространенным поражением других органов.
Тела Гамна-Ганди
Тельца Гамна-Ганди представляют собой сидеротические узелки, вызванные очаговыми организованными геморрагическими инфарктами. Обычно они наблюдаются у пациентов с застойной спленомегалией и серповидно-клеточной анемией. Они также были описаны у пациентов с гемолитической анемией, лейкемией, лимфомой или приобретенным гемохроматозом и у пациентов, получавших многократные переливания крови. Сидеротические узелки встречаются у 9–12% пациентов с портальной гипертензией и не связаны со степенью спленомегалии.При гистологическом исследовании узелки представляют собой небольшие фиброзные образования желтого или коричневого цвета, содержащие гемосидерин и кальций, а иногда и гигантские клетки инородных тел.
Тела Гамна-Ганди лучше всего видны при МРТ как множественные, от 3 до 8 мм, заметно гипоинтенсивные узелки на T1-взвешенных и T2-взвешенных изображениях. Последовательность вызванного градиента эхо-сигнала является наиболее чувствительной для обнаружения гемосидерина и этих узелков. Заметность узелков увеличивается после усиления гадолиния на T1-взвешенных, градиентных вызванных эхо-изображениях (рис.105-16). Тела гамна-ганди не улучшаются.
Рисунок 105-16
Тельца Гамна-Ганди у пациента с циррозом печени и портальной гипертензией.
Портальная венозная фаза, аксиальная, T1-взвешенная FAME (быстрое получение с многофазным улучшенным эхо-сигналом с быстрым градиентом и трехмерным преобразованием Фурье) МР-изображение после усиления гадолиния демонстрирует многочисленные небольшие гипоинтенсивные узелки по всей селезенке.
Ультразвук менее точен, чем МРТ.В исследовании, проведенном Чаном и соавторами, УЗИ выявило узелки у 24 из 34 пациентов с чувствительностью 70,6% и специфичностью 78,9%. Тельца гамна-Ганди выглядят как множественные пунктированные гиперэхогенные очаги.
Неулучшенная компьютерная томография может обнаруживать тельца гамна-Ганди как множественные тусклые, сверхплотные узелки, которые проявляются кальцификациями внутри них. Однако узелки часто не обнаруживаются на КТ.
Пиогенный абсцесс
Эпидемиология и патогенез
Изолированный абсцесс селезенки — редкое заболевание, частота встречаемости в серии аутопсий составляет от 0.14% и 0,7%. Однако абсцессы селезенки становятся все более распространенными в результате увеличения числа пациентов с ослабленным иммунитетом, пациентов со СПИДом и лиц, злоупотребляющих инъекционными наркотиками. Пиогенные абсцессы селезенки обычно бывают солитарными и одноглазными или многоячечными, но они также могут быть многоочаговыми.
Большинство абсцессов вызвано диссеминированной инфекцией и наблюдается у пациентов с сепсисом и септическими эмболами. Менее распространенные пути — это непрерывная инфекция (например, инфицированный панкреатит, перинефральный абсцесс) и суперинфекция после основного повреждения селезенки (например, инфицированного панкреатита, перинефрального абсцесса).г., травма, инфаркт). Примерно в 20% случаев источник или причина не обнаруживаются. Примерно у одной трети пациентов есть другие сопутствующие внелезеночные абсцессы. Сообщаемый в литературе уровень смертности от абсцесса селезенки составляет около 10%. Множественные абсцессы селезенки, газосодержащие абсцессы и инфекция, вызванная грамотрицательной палочкой, являются плохими прогностическими факторами. В зависимости от основного заболевания могут встречаться различные микроорганизмы, включая грамотрицательные бациллы (например, Klebsiella pneumoniae ), грамположительные кокки, грибы, полибактерии и микобактерии.
Клинические результаты
Наиболее частыми клиническими проявлениями у пациентов с абсцессами селезенки являются лихорадка (92%), боль в левой верхней части живота (77%) и лейкоцитоз (66%). Другие симптомы включают левый плевральный выпот и спленомегалию. Факторами часто являются диабет, иммуносупрессия или иммунодефицит.
Ранняя диагностика абсцесса селезенки с идентификацией микроорганизмов и определением чувствительности имеет важное значение для эффективного лечения антибиотиками.При небольших абсцессах может выполняться чрескожная диагностическая аспирация. Для более крупных абсцессов предпочтительным методом лечения стали процедуры чрескожного дренирования, позволяющие сохранить селезенку. Спленэктомия применяется в сложных случаях. Осложнения абсцессов селезенки включают разрыв и перитонит с потенциально опасными для жизни последствиями.
Результаты рентгенологического исследования
Внешний вид абсцесса селезенки зависит от стадии развития. На ранней стадии имеется нечеткая масса, которая позже превращается в сложную коллекцию с перегородками и обломками, иногда содержащую газ.Когда капсула сформировалась, поражение становится четко очерченным. Абсцессы селезенки могут быть солитарными и однокамерными, солитарными и множественными или многоочаговыми. Инфекционный организм нельзя предсказать на основе визуализации.
Наиболее частой рентгенологической находкой при абсцессе селезенки является плевральный выпот слева (42%), за которым следует инфильтрат в основании левого легкого (20%) и спленомегалия. Абсцесс селезенки редко идентифицируют по внепросветным уровням газа или воздух-жидкость в левом верхнем квадранте на простых снимках.
Ультразвук имеет чувствительность от 75% до 98% при обнаружении абсцесса селезенки. Сонография особенно полезна в качестве скринингового обследования прикованных к постели пациентов, пациентов с почечной недостаточностью и для оценки небольших поражений селезенки. У некоторых пациентов обследование может быть технически трудным из-за избыточного газа из кишечника или легких. Сонографический вид абсцесса селезенки зависит от стадии развития, и типичная картина встречается только в 44% случаев.На ранней стадии имеется нечеткое гипоэхогенное поражение, имитирующее массу. Позже абсцесс может развиться в анэхогенные кисты или сложное кистозное поражение с перегородками, обломками и акустическим затенением, вызванным газом (рис. 105-17A). Когда капсула образовалась, поражение обычно хорошо определяется с тонким гиперэхогенным ободком.
Рисунок 105-17
Абсцесс селезенки (метициллин-резистентный Staphylococcus aureus ) у пациента с эндокардитом.
А. Ультразвук демонстрирует сложное кистозное поражение с мусором. B. КТ с контрастным усилением показывает большой одноглазный, гиподензивный скопление с мягко усиливающимся краем. C. КТ с контрастированием после успешного чрескожного дренирования косички показывает почти полное разрешение.
(любезно предоставлено HLS Go, MD, Алкмар, Нидерланды.)
На КТ абсцесс селезенки обычно проявляется в виде одногокулярного или мультилокулярного, гиподенсного скопления или сложного кистозного поражения с увеличивающимся краем после внутривенного введения контрастного вещества ( Инжир.105-17Б). КТ может быть диагностическим, если в коллекции есть газ, но это редкая находка.
Преимущества КТ — высокая чувствительность (92% -98%), неинвазивность и скорость. КТ помогает отличить однокамерные абсцессы от многокомпонентных, отлично подходит для точной локализации и обеспечивает лучшую анатомическую информацию о периспленической области. Затем эту информацию можно использовать для дальнейшего управления (рис. 105-17C). КТ может выявить сопутствующие области инфекции и помочь обнаружить основной источник заболевания.
МРТ не часто выполняется при обследовании пациентов с абсцессами селезенки, потому что КТ очень чувствительна, а многие пациенты не являются клинически стабильными. Абсцессы селезенки гипоинтенсивны на T1-взвешенных изображениях и от легкой до умеренной гиперинтенсивности на T2-взвешенных изображениях по сравнению с нормальной селезенкой; они демонстрируют от минимального до интенсивного периферического усиления после внутривенного введения гадолиния.
Ядерная медицина играет ограниченную роль в обнаружении и локализации абсцессов селезенки.Если абсцесс более 2 см в диаметре, сканирование печени и селезенки 99m Tc-серой коллоидом может продемонстрировать неспецифический дефект наполнения селезенки. Сканирование 67 Ga и сканирование лейкоцитов, меченных 111 In, могут показать повышенное накопление радионуклида в селезенке. Однако нормальная, присущая селезенке активность при сканировании 67 Ga и сканировании 111 In-меченных лейкоцитов обычно скрывает очаг воспаления внутри или рядом с селезенкой, что приводит к ложноотрицательному результату обследования.Сканирование 67 Ga неспецифично, потому что поглощение индикатора также наблюдается при неопластических поражениях, особенно при лимфомах. Сканирование 99m Tc-серы коллоидов печени и селезенки перед инъекцией 111 In-меченных лейкоцитов, по-видимому, улучшает обнаружение и характеризацию по сравнению с выполнением только 111 In-меченных сканирований лейкоцитов. ФДГ-ПЭТ / КТ помогает обнаружить очаг инфекции; однако его роль в диагностике фокального абсцесса селезенки не оценивалась.
Ангиография иногда используется для лечения сосудистых осложнений. Микотические аневризмы селезенки встречаются редко и описываются только в клинических случаях. Если выполняется ангиография, абсцесс выглядит как образование с аттенуированными сосудами и гиперваскулярным краем.
Консервативное лечение гигантской кисты селезенки во время беременности; дифференциальный диагноз боли в груди, вызванной забытым органом | Гинекологическая хирургия
Киста селезенки во время беременности встречается крайне редко.В литературе описано шесть случаев, и все они были пролечены хирургическим путем. Мы сообщаем о первом случае успешного консервативного лечения огромной кисты селезенки во время беременности.
Кисты селезенки подразделяются на первичные и вторичные. Основные причины — паразитарные, врожденные и опухолевые. Вторичные кисты могут развиваться вследствие травмы, кровотечения, инфаркта-дегенерации и воспаления. Во время беременности гематома после травмы живота является наиболее частой причиной вторичных кист, поскольку инфаркт селезенки в результате гормональных изменений во время беременности увеличивает уязвимость этого органа и, таким образом, является причиной высокой частоты вторичных кист селезенки [1].
Киста селезенки несет риск инфицирования, кровотечения и разрыва. Поскольку это крайне редко во время беременности, это необычный дифференциальный диагноз для боли в левом верхнем квадранте живота и боли в груди во время беременности. Разрыв селезенки во время беременности известен как синдром экстренной селезенки, который характеризуется появлением сильной боли в левом подреберье или эпигастрии с последующим геморрагическим шоком [2]. Однако истинная частота разрыва кисты селезенки во время беременности неизвестна, поскольку в литературе описано только шесть случаев кисты селезенки при беременности [3].
Разрыв селезенки зарегистрирован у беременных в основном в третьем триместре. Это объясняется гиперволемией, увеличением селезенки и уменьшением объема брюшной полости из-за увеличения матки и мышечных сокращений во время родов [4]. При таком серьезном событии повышается риск гибели плода. Сообщается о высоком уровне материнской смертности (до 70%) [2].
Большинство кист селезенки протекает бессимптомно. Однако растяжение капсулы селезенки с огромной кистой вызовет боль в левом плече, верхнем левом квадранте или боль в груди.Первоначально это может быть диагностировано как тромбоэмболия легочной артерии, как в нашем случае. Давление на левую почку может вызвать протеинурию или даже гипертонию во время беременности. Это может привести к ошибочному диагнозу преэклампсии, особенно если это связано с тромбоцитопенией из-за изменений кровообращения в селезенке [3]. По этой причине важно провести полное обследование брюшной полости, чтобы поставить правильный диагноз для этого необычного клинического состояния. Наш диагноз кисты селезенки был поставлен после CTPA и был пропущен при первичном осмотре, поскольку в настоящее время селезенка кажется «забытым органом».
Для исключения паразитарной этиологии необходимо серологическое исследование. Разрыв эхинококковой кисты может привести к анафилактическому шоку. Визуализация с использованием ультразвука, компьютерной томографии или магнитно-резонансной томографии (МРТ) поможет определить размер кисты и ее отношение к окружающим структурам в случае необходимости хирургического вмешательства. Визуализация также может помочь в исключении злокачественных новообразований [5]. Предполагалось, что у этого пациента первичная врожденная киста. Другие типы были исключены на основании анамнеза и лабораторных исследований.
Было высказано предположение, что хирургическое вмешательство должно быть идеальным лечением кисты селезенки, если ее диаметр превышает 5 см, чтобы снизить риск осложнений [6]. Все шесть случаев кисты селезенки во время беременности, описанные в литературе, лечились хирургическим путем либо лапаротомией, либо лапароскопией, со спленэктомией или без нее. В идеале кисту селезенки следует лечить во втором триместре, чтобы избежать повышенного риска разрыва селезенки в третьем триместре или послеродовом периоде [3].
Решение отложить аспирацию в случае, если она приведет к операции, было принято из-за того, что пациентка поступила на 24-й неделе, когда ребенок находился на границе жизнеспособности.Диагностика и лечение любого заболевания, требующего хирургического вмешательства во время беременности, часто вызывает вопросы о безопасности анестезии и хирургического вмешательства у таких пациенток [7]. Спленэктомия во время беременности считается процедурой с высоким риском для матери и плода. Он несет в себе риск инфицирования, тромбоза и кровотечения. Сообщается о материнской смертности 10% и высокой неонатальной смертности из-за преждевременных родов после операции [8]. Эти риски учитывались нашим менеджментом.
Когда визуализирующие исследования указывают на доброкачественную кисту, аспирация чрезвычайно полезна. Мы представляем первый случай большой кисты селезенки во время беременности, успешно вылеченной с помощью аспирации и сохранения селезенки, чтобы избежать хирургических и анестезиологических рисков. Аспирация является простой процедурой и считается более безопасной, чем хирургическое вмешательство, поскольку она проводится под местной анестезией под контролем ультразвука, даже в амбулаторных условиях. Однако это может увеличить риск спаек и усложнить спленэктомию, если она понадобится в будущем.Аспирация не подходит для лечения злокачественной или эхинококковой кисты или рецидивирующей симптоматической кисты после аспирации.
